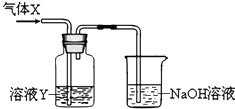
请回答:(1)实验室制取氨气的化学方程式为
2NH
4Cl+Ca(OH)
22NH
3↑+2H
2O+CaCl
22NH
4Cl+Ca(OH)
22NH
3↑+2H
2O+CaCl
2.
(2)某同学用镊子夹取湿润的红色石蕊试纸靠近收集氨气的试管口,可观察到试纸变蓝,该现象说明氨气溶于水,溶液呈
碱性
碱性
性.
(3)干燥氨气可选用的试剂是
①
①
(填序号).
①碱石灰 ②浓硫酸
(4)围绕不活泼金属能否与硝酸反应,进行了如下实验探究:在两支试管中各放入一小块铜片,分别加入稀硝酸和浓硝酸,立即塞上带导管的胶塞,并将导管通入另一只盛有NaOH溶液的试管中.请回答:
①实验中观察到,其中一支试管中反应较缓慢,产生的一种气体是
NO
NO
(填化学式),产生该气体的化学方程式是
3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O
3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O
.
②另一支试管中反应剧烈,产生的一种红棕色气体是
NO2
NO2
(填化学式),产生该气体的化学方程式是
Cu+4HNO3=Cu(NO3)2+2NO2↑+2H2O
Cu+4HNO3=Cu(NO3)2+2NO2↑+2H2O
(5)工业上由氨气合成硝酸这一过程涉及的化学方程式①
②
2NO+O2=2NO2;
2NO+O2=2NO2;
③
3NO2+H2O=2HNO3+NO;
3NO2+H2O=2HNO3+NO;
.

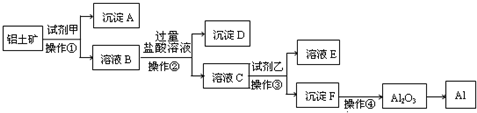
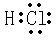
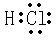
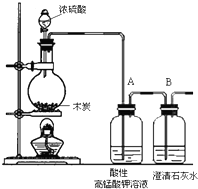 某同学用木炭和浓硫酸反应,研究浓硫酸的性质,检验气体产物.
某同学用木炭和浓硫酸反应,研究浓硫酸的性质,检验气体产物.