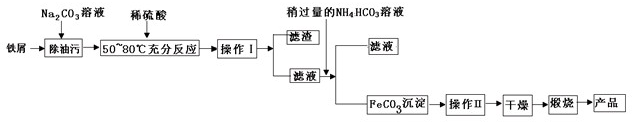
(2013?黄山一模)氯化铜是一种广泛用于生产颜料、木材防腐剂等的化工产品.某研究小组用粗铜(含杂质Fe)按下述流程制备氯化铜晶体(CuCl
2?2H
2O).

(1)实验室采用如图所示的装置,可将粗铜与Cl
2反应转化为固体1(加热仪器和夹持装置已略去).

①仪器A的名称是
分液漏斗
分液漏斗
.
②装置B中发生反应的离子方程式是
MnO
2+4H
++2Cl
-Mn
2++Cl
2↑+2H
2O
MnO
2+4H
++2Cl
-Mn
2++Cl
2↑+2H
2O
.
③如果浓盐酸不能顺利滴下,可能的原因是
没有打开分液漏斗活塞,或玻璃塞上凹槽与漏斗口侧面的小孔没有对齐.
没有打开分液漏斗活塞,或玻璃塞上凹槽与漏斗口侧面的小孔没有对齐.
④装置Ⅳ中盛装的试剂是
NaOH溶液
NaOH溶液
,其作用是
吸收多余的氯气
吸收多余的氯气
.
(2)在CuCl
2溶液转化为CuCl
2?2H
2O的操作过程中,发现溶液颜色由蓝色变为黄绿色.小组同学欲探究其原因.
已知:在氯化铜溶液中有如下转化关系:
Cu(H
2O)
42+(aq)+4Cl
-(aq)?CuCl
42-(aq)+4H
2O(l)
蓝色 黄色
①上述反应的化学平衡常数表达式是K=
| c(CuCl 42- ) |
| c[Cu(H2O) 42+ ]?c4(Cl-) |
| c(CuCl 42- ) |
| c[Cu(H2O) 42+ ]?c4(Cl-) |
.
②现欲使溶液由黄色变成蓝色,请写出两种可采用的方法
a.
加水稀释
加水稀释
b.
加硝酸银溶液
加硝酸银溶液
.
(3)由CuCl
2溶液得到CuCl
2?2H
2O的过程中要加入盐酸的目的是
防止Cu2+水解
防止Cu2+水解
.