
科目: 来源: 题型:
 有硫酸和盐酸的混合液共20mL,在此溶液中滴入0.025mol?L-1的Ba(OH)2溶液,生成BaSO4的量和溶液pH的变化如图,求:
有硫酸和盐酸的混合液共20mL,在此溶液中滴入0.025mol?L-1的Ba(OH)2溶液,生成BaSO4的量和溶液pH的变化如图,求:查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
 在20L恒容的密闭容器中,加入3molSO3(g)和1mol氧气,在某温度下使其反应,反应至4min时,氧气的浓度为0.06mol/L,当反应到8min时,反应到达平衡.
在20L恒容的密闭容器中,加入3molSO3(g)和1mol氧气,在某温度下使其反应,反应至4min时,氧气的浓度为0.06mol/L,当反应到8min时,反应到达平衡.| A | B | C | D | |
| SO3 | 1mol | 3mol | 3mol | 0mol |
| SO2 | 2mol | 1.5mol | 0mol | 6mol |
| O2 | 2mol | 1mol | 0mol | 5mol |
查看答案和解析>>
科目: 来源: 题型:
| 实验次数编号 | 待测盐酸体积(mL) | 滴入碳酸钠溶液体积(mL) |
| 1 | 20.00 | 18.80 |
| 2 | 20.00 | 16.95 |
| 3 | 20.00 | 17.05 |
| 2×C(Na2CO3) |
| 20.00 |
| (16.95+17.05) |
| 2 |
| 2×C(Na2CO3) |
| 20.00 |
| (16.95+17.05) |
| 2 |
查看答案和解析>>
科目: 来源: 题型:
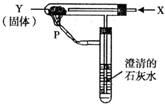 按图装置持续通入气体X,并在管口P处点燃,实验结果使澄清石灰水变浑浊,则X、Y可能是( )①H2和NaHCO3 ②CO和Na2CO3 ③CO和CuO ④H2和Fe2O3.
按图装置持续通入气体X,并在管口P处点燃,实验结果使澄清石灰水变浑浊,则X、Y可能是( )①H2和NaHCO3 ②CO和Na2CO3 ③CO和CuO ④H2和Fe2O3.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com