
科目: 来源: 题型:
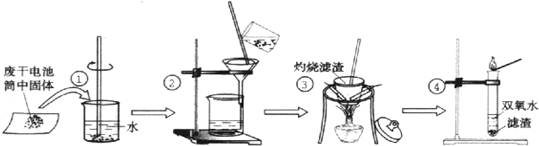
| 实验目的 | 操作 | 实验现象 | 结论 |
| 1.检验Cl- | 取少许滤液于试管中, |
含有Cl- | |
| 2.检验NH4+ | 取少许滤液于试管中, |
含有NH4+ | |
| 3.检验Zn2+ | 取少许滤液于试管中,加入稀氨水 | 先产生白色沉淀,继续加入氨水,沉淀又溶解 | 含有Zn2+ |
查看答案和解析>>
科目: 来源: 题型:
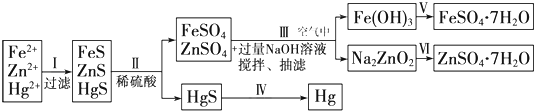
2- 2 |
查看答案和解析>>
科目: 来源: 题型:
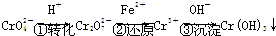
2- 4 |
2- 7 |
2- 7 |
2- 4 |
2- 7 |
2- 4 |
查看答案和解析>>
科目: 来源: 题型:
| 实 验 步 骤 | 预期现象和结论 |
| 步骤1:取适量酸雨于A、B两支洁净试管中,待用 | / |
| 步骤2:往A试管中加入过量的Ba(OH)2溶液,静置,过滤 | / |
| 步骤3:取少量步骤2得到的滤渣加入盐酸 | |
| 步骤4: |
|
| 步骤5: |
查看答案和解析>>
科目: 来源: 题型:
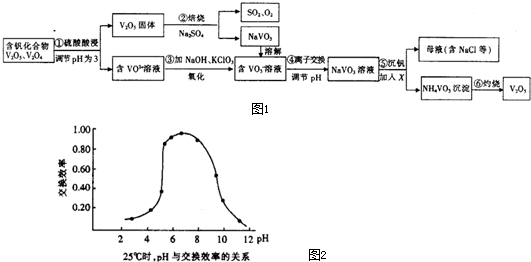
查看答案和解析>>
科目: 来源: 题型:
 氨硼烷是一种有效、安全的固体储氢材料.氨硼烷的结构和乙烷相似,如图.
氨硼烷是一种有效、安全的固体储氢材料.氨硼烷的结构和乙烷相似,如图.查看答案和解析>>
科目: 来源: 题型:
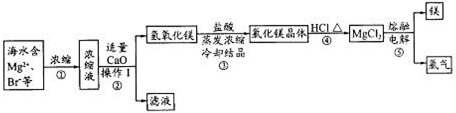
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
| ||
查看答案和解析>>
科目: 来源: 题型:
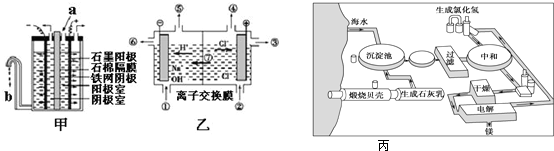
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com