
科目: 来源: 题型:阅读理解
| 实验方法 | 实验现象 | 结 论 |
| 分别向A、B溶液中加 KSCN溶液 |
固体物质中有FeCl3 | |
| 分别向KMnO4溶液中 加适量A、B溶液 |
KMnO4溶液颜色无明显变化 | 固体物质中不含 |
| 氢氧化物 开始沉淀时的pH |
氢氧化物 沉淀完全时的pH | |
| Fe3+ | 1.9 | 3.2 |
| Fe2+ | 7.0 | 9.0 |
| Cu2+ | 4.7 | 6.7 |
| 提供的药品:Cl2、浓H2SO4、NaOH溶液、CuO、Cu | ||
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
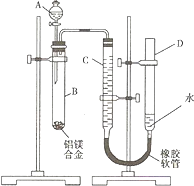 某学习小组用如图装置测定铝镁合金中铝的质量分数和铝的相对原子质量.A中为NaOH溶液.
某学习小组用如图装置测定铝镁合金中铝的质量分数和铝的相对原子质量.A中为NaOH溶液.查看答案和解析>>
科目: 来源: 题型:阅读理解
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
| 第1组(两种有机物结构简式) | 第2组(两种有机物结构简式) | 第3组(两种有机物结构简式) | 第4组(两种有机物结构简式) |
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com