
科目: 来源: 题型:
下列叙述正确的是( )
A.电解质溶液导电属于物理变化
B.电泳现象说明Fe(OH)3胶体带正电
C.配制FeCl3溶液时,常将FeCl3固体溶于较浓的盐酸中,再稀释到所需的浓度
D.水蒸汽、液态水、冰分子之间都存在氢键
查看答案和解析>>
科目: 来源: 题型:
设NA为阿伏加德罗常数的数值,下列说法正确的是( )
A.同温同压下,同体积的氢气和氨气具有相同数目的分子
B.常温下,电解食盐水若产生22.4L H2,则转移的电子数目为2NA
C.常温下,1L0.1mol/L (NH4)2SO4溶液中含0.2 NA NH4+
D.120克的NaHSO4固体中含有的离子数为3 NA
查看答案和解析>>
科目: 来源: 题型:
据最新报道,科学家最近开发一种生物活性吸附剂,可以吸附水中的几乎所有微生物和噬菌体。这种新的吸附剂由成本低廉、环保性能好的棉纤维素和主要成分为氢氧化铝的勃姆石制造而成。下列有关说法中不正确的是( )
A.Al(OH)3既能与盐酸反应又能与NaOH溶液反应
B.纤维素和淀粉互为同分异构体
C.纤维素能与醋酸发生酯化反应
D.实验室中可以用可溶性的偏铝酸盐与足量的CO2反应制取Al(OH)3
查看答案和解析>>
科目: 来源: 题型:
下列物质分类正确的是 ( )
A.非电解质:NH3、C2H5OH、H2
B.混合物:水玻璃、水银、漂白粉
C.极性分子:H2O2、H2O、NH3
D.弱电解质:HF、CO2、CH3COOH
查看答案和解析>>
科目: 来源: 题型:阅读理解
为了测定某种含有Na2O杂质的Na2O2试样的纯度,3个课外活动小组分别设计了如下三个实验方案。首先准确称量出要进行反应的样品的质量m g,然后,将按照以下方案进行实验:
方案一:将样品与水充分反应,使产生的气体与加热的铜粉充分反应,测定反应后生成的氧化铜的质量为n g,通过计算求出试样中的含量。
(1)按照此方案,则试样中Na2O2的含量为 (用含 m、n的式子表示)
a(Na2O2)% ==
(2)此方案测定的结果误差较大,主要原因是:
方案二:将样品与实验生成的二氧化碳反应,通过测定反应产生的气体的体积,计算求出试样中Na2O2的含量。
(1)按照此方案,以下制取二氧化碳和进行反应使用的仪器的连接次序是
(填写仪器的编号)
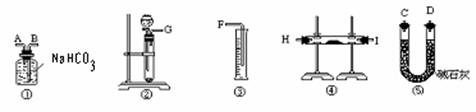
(2)通过①仪器的气体从流向上看,次序为 进 出(填写导管的字母)
方案三:将样品与水充分反应,测定出反应后的溶液的准确体积VL,因为体积较大,再从反应后的溶液中,取一定的准确的体积为V1ml溶液,装入锥形瓶中,用标准浓度的盐酸进行滴定,测定出样品与水反应后所得到的溶液的浓度,再计算求出试样中Na2O2的含量。
(1) 按照此方案,进行酸碱中和滴定时,最后一步操作应该选择的下列仪器中的
(填写仪器的编号)


(2)选择甲基橙做指示剂,确定终点的现象应该是溶液颜色由 变 并且半分钟内不变你认为方案二、方案三中测定结果最准的是
查看答案和解析>>
科目: 来源: 题型:
某化学兴趣小组的同学为模拟工业制造硫酸的生产过程,设计了如图所示的装置,请根据要求回答问题:
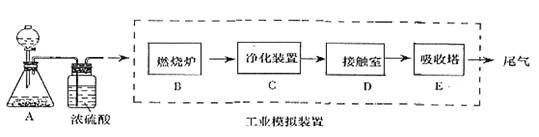
(1)装置A用来制取氧气,写出相应的化学方程式__________________________;
(2)燃烧炉内放一定量黄铁矿粉末,在高温条件下和A装置制出的氧气充分反应,其化学方程式为 ,在该反应中____________做氧化剂,若消耗了12gFeS2有_________mol电子发生了转移;
(3)C装置为净化装置,若无该装置,将混合气体直接通入D装置,除对设备有腐蚀外,还会造成的后果是___________________________________;
(4)如果D装置的温度是400℃~500℃,回答在工业中不采取加压措施的原因_______
______________________________________ ;
(5)为检验从接触室出来的气体成分,甲同学设计如下实验:
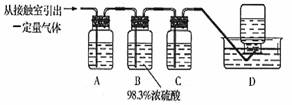
①A中盛放的试剂是____________________;
②B中盛放98.3%浓硫酸的作用是_______________________________________,乙同学提出可用饱和NaHSO3溶液代替98.3%的浓硫酸,请你判断乙同学的方案_ _____(填“可行”或“不可行”)说明理由___________ ;
③C中盛放的试剂是________________,其作用是 。
查看答案和解析>>
科目: 来源: 题型:
甲、乙两池电极材料如图所示,请按要求回答下列问题:

(1)若两池中均为Cu(NO3)2溶液,反应一段时间后
①有红色物质析出的是甲池中的________棒(铁、炭);乙池中的_____极(阴、阳)。
②乙池中阳极上发生的电极反应方程式是_________________。
(2)若两池中均为饱和NaCl溶液
①写出乙池中总反应的化学方程式_________________________。
②甲池中碳极上电极反应方程式是_________________,乙池碳极上电极反应属
___________(填氧化反应、还原反应)。
③将湿润的淀粉KI试纸放在乙池碳极附近,发现试纸变蓝,待一段时间后又发现蓝色褪去。这是因为过量的Cl2将生成的![]() 又氧化。若反应的
又氧化。若反应的![]() 和
和![]() 物质的量之比为5:1,且生成HCl和另一种强酸,该强酸的化学式为_______________。
物质的量之比为5:1,且生成HCl和另一种强酸,该强酸的化学式为_______________。
④若乙池转移0.1mol![]() 后停止实验,池中溶液体积是1L,则溶液混匀后的pH=___。(不考虑所生成的气体溶解在溶液中的情况)
后停止实验,池中溶液体积是1L,则溶液混匀后的pH=___。(不考虑所生成的气体溶解在溶液中的情况)
查看答案和解析>>
科目: 来源: 题型:
下表是元素周期表的一部分。表中所列的字母分别代表某一化学元素。

回答下列问题
⑴以上元素中原子半径最大的是 (填写元素符号)最小的是 (填写元素名称)
⑵以上元素中,属于金属的:①在地壳中含量最高的是 ,(填写字母代号)②单质的工业年产量最高的是 (填写周期表中的具体位置)
⑶h和g的最高价氧化物比较,熔点高的是 (填写氧化物化学式);j和k的氢化物比较,熔点高的是 (填写氢化物化学式)
⑷以上元素两两形成的中学中常见的化合物中①既有离子键,又有非极性共价键的有_________(写一种)(填写化学式)
⑸按要求写①c的氧化物与l的氢化物反应的化学方程式
②都是由abjk四种元素形成的两种化合物反应的离子方程式
⑹b i l三元素形成的化合物的电子式为
查看答案和解析>>
科目: 来源: 题型:
在反应:11P+15CuSO4+24H2O=5Cu3P+6H3PO4+15H2SO4 中15molCuSO4氧化的P原子的物质的量为( )
A.3mol B.11mol C.6mol D.5mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com