
科目: 来源: 题型:
下列说法不正确的是 ( )
A.用碱石灰吸收氨气中的水蒸气
B.金属单质只能与非金属氧化物反应,不能与金属氧化物反应
C.乙醇燃烧生成物总能量低于反应物总能量
D.Cu2S、Na2O2、H2SO4、Fe(OH)3均可通过化合反应生成
查看答案和解析>>
科目: 来源: 题型:
A、B、C是短周期ⅠA和ⅡA族元素形成的碳酸盐,它们的质量分别为![]() 、
、![]() 、
、![]() ,与足量盐酸完全反应,消耗盐酸的物质的量分别为
,与足量盐酸完全反应,消耗盐酸的物质的量分别为![]() (HCl)、
(HCl)、![]() (HCl)、
(HCl)、![]() (HCI)。
(HCI)。
已知:![]() =
=![]() +
+ ![]() ,
,![]() (HCl)=
(HCl)= ![]() (HCI)+
(HCI)+ ![]() (HCI),那么A可能是( )
(HCI),那么A可能是( )
A.Li2CO3或MgCO3 B.Li2CO3或Na2CO3
C.BeCO3 D.Na2CO3
查看答案和解析>>
科目: 来源: 题型:
下列说法不正确的是 ( )
A.铜在潮湿的环境中比在干燥的环境中更容易生成铜锈
B.实验室用锌制氢气,滴加少量硫酸铜溶液可增加反应速率
C.铁在化学腐蚀和电化腐蚀的过程中都有电流产生
D.将被保护的铁制品和外加直流电源负极相连的方法叫做阴极电保护法
查看答案和解析>>
科目: 来源: 题型:
目前,人类已经发现的非金属元素除稀有气体元素外共有16种,下列对这16种非金属元素的判断正确的有 ( )
A.都是主族元素,最外层电子数都大于或等于3
B.部分非金属单质在发生反应时既可被氧化也可被还原
C.氢化物常温下都是气态,所以又叫做气态氢化物
D.氧化物常温下都可以与水反应生成酸
查看答案和解析>>
科目: 来源: 题型:
以下说法正确的是 ( )
A.原子是化学变化中的最小微粒,即化学变化不产生新元素。核反应产生了新元素不属于化学变化
B.某阴离子的结构示意简图为![]() 则该元素位于第三周期、VIA族
则该元素位于第三周期、VIA族
C.非金属元素的原子间只能存在共价键,金属元素的原子和非金属元素的原子间只形成离子键
D.某物质的化学式为XY3,则X的化合价只能为+3或+6价
查看答案和解析>>
科目: 来源: 题型:
下列叙述中,正确的是 ( )
A.变质的油脂有特殊难闻的气味,是由于油脂发生了水解反应
B.除去苯中的少量乙醇,加浓硫酸、乙酸加热,通过发生酯化反应而除去乙醇
C.将乙烯通入溴水中,溴水退色,是因为发生了加成反应
D.高分子材料、盐酸、水煤气、沼气、石油等是混合物,而C5H12一定是纯净物
查看答案和解析>>
科目: 来源: 题型:
金属镁是银白色,但镁带表面呈现灰黑色。用砂纸磨下镁带表面固体粉末,隔绝空气加强热,有水气生成;另取粉末,加入稀酸,产生气体导入澄清石灰水中,产生混浊。
(1)为确定其组成,将镁带表面固体粉末2.84g隔绝空气加强热,产物先用浓硫酸吸收,再用碱石灰吸收,剩余白色固体。浓硫酸增重0.36g,碱石灰增重0.88g,请通过计算确定该组成的化学式。
(2)如果将这种灰黑色的镁条在纯氧中点燃,燃烧产物有黑色物质生成,这种黑色物质的成份是什么?并说明形成的原因?
查看答案和解析>>
科目: 来源: 题型:
下图中,P为一可自由滑动的活塞。关闭K ,分别向容器A、B中各充入2molX、2molY,起始时,VA=aL:VB=0.8 aL(连通管的体积忽略不计),在相同温度和有催化剂存在的条件下,两容器中各自发生下述反应:3X(g)+3Y(g) ![]() 2Z(g)+2W(g),达到平衡时,VB=0.6aL。
2Z(g)+2W(g),达到平衡时,VB=0.6aL。
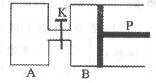 试回答下列问题;
试回答下列问题;
(1)A、B两容器达到平衡的时间:tA ___tB(填“大于”、“小于”或“等于”)
(2)平衡时,B中Y的转化率为_________:反应的平衡常表达式K(B)=_______;当A、B分别达到平衡时,两容器中物质W的百分含量关系是:A ____ B(填“大于”、“小于”或“等于”)。
(3)如果要计算出平衡时B的混合气体的密度,则至少还需要知道的数据是_______ (MX、MY、MZ、MW分别代表X、Y、Z、W的摩尔质量)
①MX ②MY ③MZ ④MWw
A.②和④ B. ①和② C. ①和③ D. ②和③
(4)打开K,一段时间后反应可再次达到平衡,则此时B的体积为________________L。
查看答案和解析>>
科目: 来源: 题型:
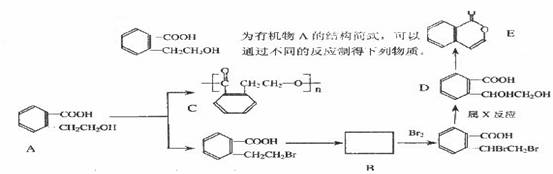 (1)写出A→C的化学方程式:____________________________________________________
(1)写出A→C的化学方程式:____________________________________________________
(2)推断B物质的结构简式:_________________________________________。X反应类型是___________;由D→E所需的试剂是______________________
(3)R物质属于A的同分异构体,其性质如下:
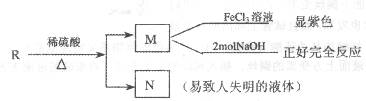
试写出符合条件的R的同分异构体的结构简式(任写两种):______________________;________________________________。
查看答案和解析>>
科目: 来源: 题型:
某研究性学习小组为研究铜与浓硫酸的反应,设计了如下图所示的实验探究方案(装置中的固定仪器和酒精灯均未画出)。
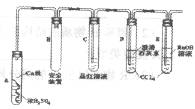
以下是该学习小组部分交流记录及后续探究实验的记录。
实验1:加热后,液面下铜丝变黑,产生气泡,一段时间后液面以上的铜丝也发黑,而且试管上部内壁有少量淡黄色硫固体凝聚,持续加热浓硫酸(沸腾)时,淡黄色固体物质又慢慢地消失。
实验2:截取浓硫酸液面上方变黑的铜丝,插入稀硫酸中无变化,将浓硫酸液面下方变黑的铜丝,插入稀硫酸,黑色明显变浅,溶液呈蓝绿色。
实验3:将浓硫酸液面下方铜丝的黑色物质刮下后,经稀硫酸洗、蒸馏水洗、过滤、干燥后放入氧气流中加热,然后冷却,用电子天平称重发现质量比加热前减少。
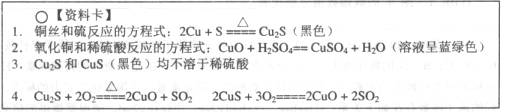
【问题探究】
(1)A试管上方的长导管的作用是______;D、E两试管中CCl4的作用是________。
(2)写出淡黄色固体物质消失的化学方程式_________________________________。
(3)试管D中的澄清石灰水变浑浊后又变澄清,变澄清的原因是(用方程式表示)________
(4)根据上述研究,结合资料卡上的内容,你认为液面下方铜丝表面的黑色物质成分肯定有___________________________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com