
科目: 来源: 题型:
铝的阳极氧化,是一种常用的金属表面处理技术,它能使铝的表面生成一层致密的氧化膜,该氧化膜不溶于稀硫酸。某化学研究小组在实验室中按下列步骤模拟该生产过程。填写下列空白:
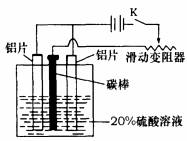
(1)配制实验用的溶液。要配制200mL密度为1.2g?cm-3的溶质质量分数为16%的NaOH溶液,需要称取 g NaOH固体。
(2)把铝片浸入热的16%NaOH溶液中约半分钟左右洗去油污,除去表面的氧化膜,取出用水冲洗。写出除去氧化膜的离子方程式 。
(3)如上图,组装好仪器,接通开关K,通电约25min。在阳极生成氧化铝,阴极产生气体。写出该过程中的电极反应式:
阳极: ;
阴极:
(4)断开电路,取出铝片,用1%稀氨水中和表面的酸液,再用水冲洗干净。写出该过程发生反应的离子方程式 。
查看答案和解析>>
科目: 来源: 题型:
某校化学研究性学习小组要利用已经学过的化学知识制取少量漂白粉,并进一步探究漂白粉的化学性质。他们查阅资料得知:2Cl2+2Ca(OH)2=Ca(ClO)2+CaCl2+2H2O是放热反应,温度稍高时便发生副反应:6Cl2+6Ca(OH)2→Ca(ClO3)2+5CaCl2+6H2O。学生设计出了甲、乙、丙三套装置:
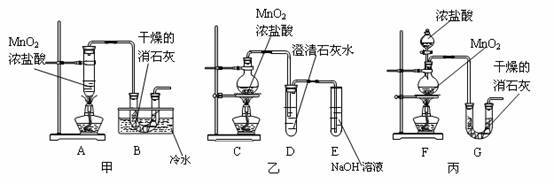
(1)请从甲、乙、丙各套装置中选取合理的部分,按气体从左至右的流向组装成一套较合理的装置,(填各部分仪器的编号)
(2)部分学生认为上述组装仍存在缺点,他们指出在前两个仪器之间应增加如下装置:
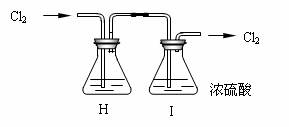
你认为H洗气瓶中所盛液体是 ,其作用是 。
若无此装置,对制漂白粉有什么不利影响 ;
洗气瓶I有无必要 理由是 。
(3)为了研究所制得的漂白粉的化学性质,同学们把少量漂白粉投入到淡绿色的FeCl2溶液,所产生的现象是 。由此可知漂白粉溶液所具有化学性质是 。
查看答案和解析>>
科目: 来源: 题型:
实验室用50 mL 1.0 mol?L-1盐酸跟50 mL 1.1 mol?L-1氢氧化钠溶液在下图装置中进行中和反应,并通过测定反应过程中所放出的热量来计算中和热。试回答下列问题:
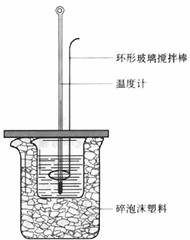
(1)大小烧杯间填满碎泡沫塑料的作用是 。
(2) (填“能”或“不能”)将环形玻璃搅拌棒改为环形金属(如铜)棒。其原因是 。
(3)大烧杯上如不盖硬纸板,对求得中和热数值的影响是 (填“偏高”或“偏低”或“无影响”)。
(4)如果改用60 mL 1.0 mol?L-1盐酸跟50 mL 1.1 mol?L-1氢氧化钠溶液进行反应,则与上述实验相比,所放热量 (“增加”、 “减少”或“不变”),理由是 ;所求中和热数值 (“增加”、 “减少”或“不变”),理由是 。
查看答案和解析>>
科目: 来源: 题型:
下图是一种正在投入生产的大型蓄电系统。左右两侧为电解质储罐,中央为电池,电解质通过泵不断在储罐和电池间循环;电池中的左右两侧为电极,中间为离子选择性膜,在电池放电和充电时该膜可允许钠离子通过;放电前,被膜隔开的电解质为Na2S2和NaBr3,放电后,分别变为Na2S4和NaBr。下列说法正确的是( )
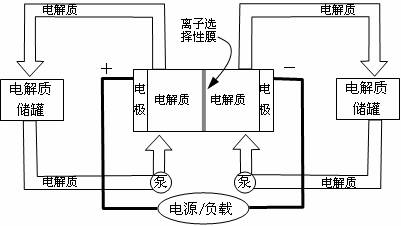
A.电池充电时,阳极电极反应式为:3Br――2e―=Br3―
B.电池放电时,负极电极反应方程式为:2S22―+2e―=S42―
C.电池放电时,电池的总反应方程式为:Na2S4+3NaBr=2 Na2S2+ NaBr3
D.在充电过程中钠离子通过膜的流向为从左到右
查看答案和解析>>
科目: 来源: 题型:
恒温下,固定容积的密闭容器中有可逆反应2SO3(气)=2SO2+O2(气) 可用确定该反应已达到平衡状态的是:( )
A.容器内压强不随时间改变
B.SO3的消耗速率与SO2的生成率相等
C.正反应生成SO2的速率与逆反应生成SO3的速率相等
D.容器内混和气体的密度不随时间改变
查看答案和解析>>
科目: 来源: 题型:
科学家发现,不管化学反应是一步完成或分几步完成,该反应的热效应是相同的。已知在25℃,105Pa时,石墨、一氧化碳的燃烧热分别是393.5 kJ?mol-1和283.0 kJ?mol-1,下列说法或方程式正确的是( )
A.在相同条件下:2C(石墨)+O2(g)=2CO(g);ΔH=-110.5 kJ?mol-1
B.1 mol石墨不完全燃烧,生成CO2和CO混合气体时,放热504.0 kJ
C.在相同条件下:C(石墨)+CO2(g)=2CO(g); ΔH=+172.5 kJ?mol-1
D.若金刚石燃烧热大于石墨的燃烧热,则石墨转变为金刚石需要吸热
查看答案和解析>>
科目: 来源: 题型:
如图是某公司批量生产的笔记本电脑所用的甲醇燃料电池的构造示意图。
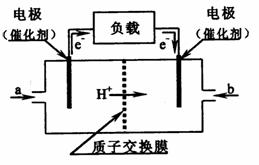
甲醇在催化剂作用下提供质子(H+)和电子,电子经外电路、质子经内电路到达另一极与氧气反应,该电池总反应式为:2CH3OH+3O2=2CO2+4H2O。下列有关该电池的说法错误的是( )
A.右边的电极为电池的负极,b处通入的是空气
B.左边的电极为电池的负极,a处通入的是甲醇
C.电池负极的反应式为:2CH3OH+2H2O-12e-=2CO2+12H+
D.电池正极的反应式为:3O2+12H++12e-=6H2O
查看答案和解析>>
科目: 来源: 题型:
镁粉与一定量某浓度的盐酸反应,但反应速度太快,为减慢反应速度,且不影响产生H2的总量,可向盐酸中加入的物质是( )
A.H2O B.CH3COONa C.NaOH D.NaHCO3
查看答案和解析>>
科目: 来源: 题型:
化学用语是学习化学的重要工具。下列用来表示物质变化的化学用语中,错误的是( )
A.钢铁腐蚀时可能发生的正极反应:2H2O+ O2+ 4e-=4OH一
B.明矾水解的离子方程式: Al3++3 H2O![]() Al(OH)3+3H+
Al(OH)3+3H+
C.少量氢氧化钙溶液与碳酸氢钠溶液混合:OH-+ HCO3一=H2O+ CO32-
D.表示氢气燃烧的热化学方程式:
2H2(g)+O2(g)=2H2O(l)△H=+571.6kJ?mol-1
查看答案和解析>>
科目: 来源: 题型:
在容积不变的密闭容器中存在如下反应:2SO2(g)+O2(g)![]() 2SO3(g);△H<0某研究小组研究了其他条件不变时,改变某一条件对上述反应的影响,下列分析正确的是:( )
2SO3(g);△H<0某研究小组研究了其他条件不变时,改变某一条件对上述反应的影响,下列分析正确的是:( )
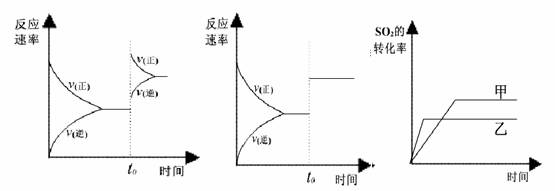
Ⅰ Ⅱ Ⅲ
A.图I研究的是t0时刻增大O2的浓度对反应速率的影响
B.图II研究的是t0时刻加入催化剂后对反应速率的影响
C.图III研究的是催化剂对平衡的影响,且甲的催化效率比乙高
D.图III研究的是温度对化学平衡的影响,且乙的温度较高
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com