
科目: 来源: 题型:
NA为阿佛加德罗常数的数值,下列选项中正确的是( )
A.1molH2O2与MnO2充分作用后,转移2NA个电子
B.标准状况下,28gN2 和C2H4的混合物所含分子数为NA
C.标准状况下,22.4LCHCl3含 NA个分子
D.1mol白磷分子中所含共价键数为4NA
查看答案和解析>>
科目: 来源: 题型:
下列有关能源及化学反应能量变化的说法错误的是( )
A.在即将到来的新能源时代,核能、太阳能、氢能将成为主要能源
B.月球土壤中含有丰富的质量数为3的氮,它可以作为未来核能的重要原料
C.乙醇汽油是多种烃的混合物
D.反应物和生成物所具有的总能量决定了反应是放热还是吸热
查看答案和解析>>
科目: 来源: 题型:
图表法、图象法是常用的科学研究方法。
I.短周期某主族元素M的电离能情况如图(A)所示。则M元素位于周期表的第 族。
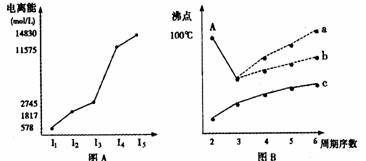
II.图B是研究部分元素的氢化物的沸点变化规律的图像,折线c可以表达出第 族元素氢化物的沸点的变化规律。不同同学对某主族元素氢化物的沸点的变化趋势画出了两条折线――折线a和折线b,你认为正确的是: ,理由是: 。
III.人类在使用金属的历史进程中,经历了铜、铁、铝之后,第四种将被广泛应用的金属则被科学家预测为是钛(Ti)。钛被誉为“未来世纪的金属”。试回答下列问题:
(1)22Ti元素基态原子的价电子层排布式为 。
(2)在Ti的化合物中,可以呈现+2、+3、+4三种化合价,其中以+4价的Ti最为稳定。偏钛酸钡的热稳定性好,介电常数高,在小型变压器、话筒和扩音器中都有应用。偏钛酸钡晶体中晶胞的结构示意图如下图,则它的化学式是 。
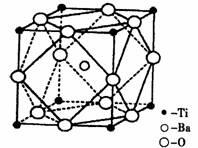
查看答案和解析>>
科目: 来源: 题型:
2006年5月15日国家食品药品监督管理局通报了齐齐哈尔第二制药有限公司假药案的情况。“齐二药”违反规定,购入工业用“二甘醇”(化学式为C4H10O3)代替医用丙二醇(化学式为C3H8O3)作辅料,用于“亮菌甲素”注射液的生产,导致病人肾功能急性衰竭,造成多人死亡。二甘醇又称乙二醇醚,分子式C4H10O3 (HO-CH2-CH2-O-CH2-CH2-OH)。以二甘醇为原料,可制取醚、酸、酯、胺等多种化工产品,其主要产品有吗啉及其衍生物1,4-二恶烷(1,4-二氧环已烯),二甘醇单(双)醚,二甘醇酯类(饱和酯和不饱和酯)等,被广泛应用于石油化工、橡胶、塑料、纺织、涂料、粘合剂、制药等行业,用途十分广泛。二甘醇一般的合成路线为:

请回答下列问题:
(1)过程1是石油加工中常用步骤,其名称为 。
(2)从物质B到物质C的过程如果条件控制不好会生成另一种物质E,E可用于金属的气割和氧气焊,则为了能得到二甘醇D,物质B到物质C的反应条件是 ;该反应属于 (填有机反应类型)。
(3)物质D就是二甘醇,则合成路线中的物质A、B、C的结构简式分别为:
A: ,B: ,
C: 。
(4)反应1的化学方程式为: 。
查看答案和解析>>
科目: 来源: 题型:
CO不仅是家用煤气的主要成分,也是重要的化工原料。美国近年来报导了一种低温低压催化工艺,把某些简单的有机物经“羰化”反应后可以最后产生一类具有优良性能的装饰性高分子涂料、粘合剂等。如下图所示:
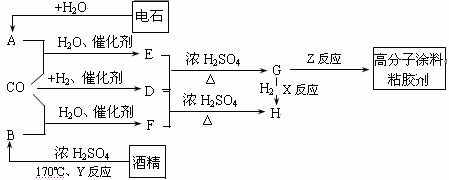
图中G(RCOOR,)的一种同分异构体是E的相邻同系物;而H的一种同分异构体则是F的相邻同系物。已知D由CO和H2按物质的量之比为1∶2完全反应而成,其氧化产物可发生银镜反应;H是含有4个碳原子的化合物。试写出:
(1)结构简式:E 、G 、R,基 。
(2)G的两个同类别同分异构体的结构简式(不带R字母)
及 。
(3)反应类型:X 、Y 、Z 。
(4)写出下列转化的化学方程式:
![]()
① ;
② 。
查看答案和解析>>
科目: 来源: 题型:
从海水中可提取各种化工原料,下图是工业上对海水的几项综合利用的示意图:

(1)在实验室进行过滤所需要玻璃仪器为______________。
(2)在粗盐中含有Ca2+、Mg2+、SO42-等杂质,精制时所用的试剂为:
A.盐酸 B.氯化钡溶液 C.氢氧化钠溶液 D.碳酸钠溶液。
则加入试剂的顺序是(填编号)______
(3)电解饱和食盐水时,与电源正极相连的电极上发生的反应为_______;与电源负极相连的电极附近溶液的pH_______(填“变大”、“变小”和“不变”)
(4)Mg(OH)2中加入盐酸后,要获得MgCl2?6H2O晶体,需要进行的实验操作依次为_____
A.蒸馏 B.灼烧 C.过滤 D.蒸发 E.冷却结晶
(5)用相同电量分别电解无水MgCl2和饱和食盐水时,当生成1molMg的同时,生成NaOH的物质的量是________mol。
查看答案和解析>>
科目: 来源: 题型:
A、B、C、D是四种短周期元素,它们的原子序数依次增大,其中A与C,B与D分别是同主族元素;已知B、D二元素原子核中质子数之和是A、C二元素原子核中质子数之和的2倍;四种元素形成的单质中有两种是气体;两种是固体。
回答:
(1)写出由B、C二元素所形成的原子个数比为1∶1的化合物的电子式__________,其晶体中存在的化学键有____________________(填化学键名称)。
(2)写出均由A、B、C、D四种元素组成的两种化合物的水溶液发生反应的离子方程式为____________________ 。
(3)用A元素的单质与B元素的单质可制成新型的化学电源,已在宇宙飞船中使用。其构造如图所示。两个电极均由多孔性碳制成,通入的气体由孔隙中逸出,并在电极表面放电。则a是 ___极,电极反应式为___________________。
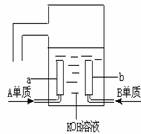
查看答案和解析>>
科目: 来源: 题型:
对于弱酸,在一定温度下达到电离平衡时,各微粒的浓度存在一种定量的关系。若25℃时有HA![]() H++A―,则K=
H++A―,则K=![]() 。式中:K为电离平衡常数,只与温度有关,c为各微粒的平衡浓度。下表是几种常见弱酸的电离平衡常数(25℃)。
。式中:K为电离平衡常数,只与温度有关,c为各微粒的平衡浓度。下表是几种常见弱酸的电离平衡常数(25℃)。
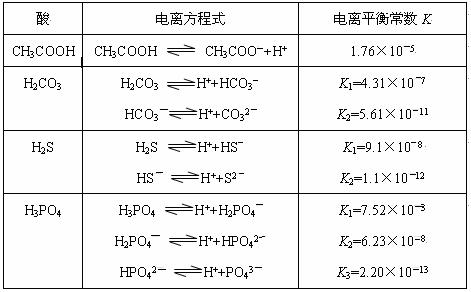
回答下列各题:
(1)K只与温度有关,当温度升高时,K值__________(填“增大”、“减小”、“不变”)。
(2)在温度相同时,各弱酸的K值不同,那么K值的大小与酸性的相对强弱有何关 系?_____________________________。
(3)若把CH3COOH、H2CO3、HCO3-、H2S、HS-、H3PO4、H2PO4-、HPO42-都看作是酸,其中酸性最强的是_______,最弱的是_____________。
(4)多元弱酸是分步电离的,每一步都有相应的电离平衡常数,对于同一种多元弱酸的K1、K2、K3之间存在着数量上的规律,此规律是________________,产生此规律的原因是___________________________________。
查看答案和解析>>
科目: 来源: 题型:
某校化学兴趣小组的同学在进行研究性学习时,对“NO2能否支持燃烧”这个问题很感兴趣,他们决定自己动手设计实验进行探究。

(1)甲组同学设计的实验方案:向烧瓶中加入适量浓硝酸并加热,当烧瓶中有红棕色气体产生之后,将燃着的木条伸入烧瓶中,发现木条火焰熄灭。由此他们得出“NO2不能支持燃烧”的结论。
甲组同学所得的结论一定正确吗?请你说明理由:
。
(2)乙组同学通过查阅资料得知,一些不活泼金属的硝酸盐受热时也能产生NO2气体,如:2Cu(NO3)2![]() 2CuO+4NO2↑+O2↑,2AgNO3
2CuO+4NO2↑+O2↑,2AgNO3![]() 2Ag+2NO2↑+O2↑。他们根据此原理设计了如右图所示的实验装置(加热、夹持仪器未画出),并分别用Cu(NO3)2和AgNO3进行实验,实验中发现当红棕色气体进入集气瓶后,带火星的木炭均能复燃,乙组同学由此得出“NO2能支持燃烧”的结论。
2Ag+2NO2↑+O2↑。他们根据此原理设计了如右图所示的实验装置(加热、夹持仪器未画出),并分别用Cu(NO3)2和AgNO3进行实验,实验中发现当红棕色气体进入集气瓶后,带火星的木炭均能复燃,乙组同学由此得出“NO2能支持燃烧”的结论。
①老师认为上述两个实验中,有一个实验所得结论是不可靠的,你认为该实验中选用的反应物是 ,其结论不可靠的原因是 。
②运用该实验装置进行实验时,造成的不良后果是 。
(3)丙组同学拟设计一个用较为纯净的NO2气体(无O2产生)来探究“NO2能否支持燃烧”的实验。

①丙组同学制取NO2的化学方程式是 。
②如图是该组同学设计的制取并收集NO2气体的实验装置,请在方框中将该装置补充完整,并注明补充装置中所用试剂。
查看答案和解析>>
科目: 来源: 题型:
为测定碳酸钙纯度(设含杂质SiO2),某学生研究性学习小组设计了如下几个实验方案:
[方案Ⅰ](1)称取碳酸钙样品m g(2)加入过量盐酸;(3)收集并测定生成的气体体积V mL。[方案Ⅱ](1)称取碳酸钙样品m g;(2)用c mol/L盐酸VmL(过量)溶解样品;(3)取溶解后的溶液![]() mL,用c′mol/L NaOH溶液滴定,恰好用去V′Ml
mL,用c′mol/L NaOH溶液滴定,恰好用去V′Ml
[方案Ⅲ](1)称取碳酸钙样品m g;(2)高温(1000℃)煅烧直至质量不再发生变化,冷却后称量,质量为m′g。
[方案Ⅳ] (1)称取碳酸钙样品m g;
(2)加入足量c mol / L盐酸V mL使之完全溶解;
(3)过滤并取滤液;
(4)在滤液中加入过量c′mol/L Na2CO3溶液V′mL;
(5)将步骤(4)中的沉淀滤出、洗涤、干燥、称重为m′g。
回答下列问题:
(1)你认为上述4个方案中,最好的方案是 ,其他方案的缺点分别是:
方案 。
方案 。
方案 。
(2)为减少方案Ⅳ实验误差,必要的操作是 (填选项编号)。
A.精确测定Na2CO3溶液体积V′mL
B.精确配制浓度为c′mol/L Na2CO3溶液
C.将步骤(3)所得沉淀洗涤,洗涤液也应并入(4)中
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com