
科目: 来源: 题型:
化合物A相对分子质量为86,碳的质量分数为55.8%,氢为7.0%,其余为氧。A的相关反应如下图所示:

已知R―CH=CHOH(烯醇)不稳定,很快转化为R―CH2CHO。
根据以上信息回答下列问题:
(1)A的结构简式是 。
(2)反应②的化学方程式是 。
(3)反应①的化学方程式是 。
(4)A有多种同分异构体,写出四个同时满足两个条件的同分异构体的结构简式:(i)能发生水解反应(ii)能使溴的四氯化碳溶液褪色。
、 、 、 ;
(6)A的另一种同分异构体,其分子中所有碳原子在一条直线上,它的结构简式为 。
查看答案和解析>>
科目: 来源: 题型:阅读理解
过氧化氢是重要的氧化剂、还原剂,它的水溶液又称为双氧水,常用作消毒、杀菌、漂白等。某化学兴趣小组取一定量的过氧化氢溶液,准确测定了过氧化氢的含量,并探究了过氧化氢的性质。
Ⅰ.测定过氧化的含量
请填写下列空白:
(1)移取10.00 mL密度为ρ g/mL的过氧化氢溶液至250mL (填仪器名称)中,加水稀释至刻度,摇匀。移取稀释后的过氧化氢溶液25.00mL至锥形瓶中,加入稀硫酸酸化,用蒸馏水稀释,作被测试样。
(2)用高锰酸钾标准溶液滴定被测试样,其反应的离子方程式如下,请将相关物质的化学计量数及化学式填写在括号里。
( )MnO4-+( )H2O2+( )H+=( )Mn2++( )H2O+( )( )![]()
(3)滴定时,将高锰酸钾标准溶液注入 (填“酸式”或“碱式”)滴定管中。滴定到达终点的现象是 。
(4)重复滴定三次,平均耗用c mol/L KMnO4标准溶液V mL,则原过氧化氢溶液中过氧化氢的质量分数为 。
(5)若滴定前滴定管尖嘴中有气泡,滴定后气泡消失,则测定结果 (填“偏高”或“偏低”或“不变”)。
Ⅱ.探究过氧化氢的性质
该化学举小组根据所提供的实验条件设计了两个实验,分别证明了过氧化氢的氧化性和不稳定性。(实验条件:试剂只有过氧化氢溶液、氯水、碘化钾淀粉溶液、饱和硫化氢溶液,实验仪器及用品可自选。)
请将他们的实验方法和实验现象填入下表:
| 实 验 内 容 | 实 验 方 法 | 实 验 现 象 |
| 验证氧化性 | ||
| 验证不稳定性 |
查看答案和解析>>
科目: 来源: 题型:
下表为元素周期表的一部分,请参照元素①-⑧在表中的位置,用化学用语回答下列问题:
| 族 周期 | IA | 0 | ||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ||||
Ⅰ.(1)④、⑤、⑥的原子半径由大到小的顺序为 。
(2)①、④、⑤、⑧中的某些元素可形成既含离子键又含极性共价键的化合物,写出其中一种化合物的电子式: 。
(3)由表中两种元素的原子按11组成的常见液态化合物的稀液易被催化分解,其结构式为 ,它非常容易被一种日常常见过渡金属离子还原,在酸性条件的离子反应方程式为 。
(4)由表中元素形成的常见物质X、Y、Z、M、N可发生以下反应:
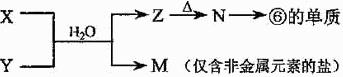
X溶液与Y溶液反应的离子方程式为 。常温下,为使0.1 mol/L M 溶液中由M电离的阴、阳离子浓度相等,应向溶液中加入一定量的Y溶液至 ;若Y与M混合则可使溶液呈碱性,此时溶液中离子浓度大小顺序为 。(填一种合理即可)
Ⅱ实验室制取③的氢化物的方程式为 ,已知该氢化物与灼热的氧化铜反应得到氮气和金属铜,用示意图中的装置可以实现该反应。
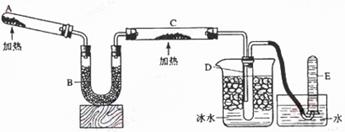
回答下列问题:
(1)B中加入的物质是 ,其作用是 。
(2)实验时在C中观察到得现象是 ,发生反应的化学方程式是 。
(3)D中收集到的物质是 ,检验该物质的方法和现象是 。
查看答案和解析>>
科目: 来源: 题型:
在一体积可变的密闭容器中,发生反应:mX(g)![]() nY(g) ;△H=QkJ?mol-1。加入一定量的X、Y,反应达到平衡时,Y的物质的量浓度与温度、气体体积的关系如下表所示:
nY(g) ;△H=QkJ?mol-1。加入一定量的X、Y,反应达到平衡时,Y的物质的量浓度与温度、气体体积的关系如下表所示:
|
积 温度℃ | 1 | 2 | 3 |
| 100 | 1.00 | 0.75 | 0.53 |
| 200 | 1.20 | 0.09 | 0.63 |
| 300 | 1.30 | 1.00 | 0.70 |
下列说法正确的是
A.m>n
B.Q<0
C.温度不变,压强增大,Y的质量分数减少
D.体积不变,温度升高,平衡向逆反应方向移动
查看答案和解析>>
科目: 来源: 题型:
迷迭香酸是从蜂花属植物中提取得到的酸性物质,其结构如右图。下列叙述正确的是

A.迷迭香酸属于芳香烃
B.1mol迷迭香酸最多能和8mol氢气发生加成反应
C.迷迭香酸可以发生水解反应、取代反应和酯化反应
D.1mol迷迭香酸最多能和含5mol NaOH的水溶液完全反应
查看答案和解析>>
科目: 来源: 题型:
对于常温下pH为1的硝酸溶液,下列叙述正确的是
A.该溶液中硝酸电离出的c(H+)与水电离出的c(H+)之比值为10―12。
B.向该溶液中加入等体积、pH为13的氢氧化钡溶液恰好完全中和
C.该溶液lmL稀释至100mL后,pH等于3
D.该溶液中水电离出的c(H+)是pH为3的硝酸中水电离出的c(H+)的100倍
查看答案和解析>>
科目: 来源: 题型:
向m g镁和铝的混合物中加入适量的稀硫酸,恰好完全反应生成标准状况下的气体b L。向反应后的溶液中加入c mol/L氢氧化钾溶液V mL,使金属离子刚好沉淀完全,得到的沉淀质量为n g。再将得到的沉淀灼烧至质量不再改变为止,得到固体p g。则下列关系不正确的是
A.![]() B. n = m+17Vc
B. n = m+17Vc
C.![]() D.
D.![]() <p<
<p<![]()
查看答案和解析>>
科目: 来源: 题型:
下列离子方程式与所述事实相符且正确的是
A.漂白粉溶液在空气中失效:ClO-+CO2+H2O=HClO+HCO3-
B.等体积、等浓度的Ba(OH)2稀溶液与NH4HCO3稀溶液混合:
Ba2++2OH-+NH4++HCO3―=BaCO3↓+NH3?H2O+H2O
C.向NaAlO2溶液中通入过量CO2制Al(OH)3:
AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-
D.在强碱溶液中次氯酸钠与Fe(OH)3反应生成Na2FeO4:
3ClO-+2Fe(OH)3=2FeO42-+3Cl-+H2O+4H+
查看答案和解析>>
科目: 来源: 题型:
![]() 是制备硫酸的重要反应。下列叙述正确的是
是制备硫酸的重要反应。下列叙述正确的是
A.催化剂V2O5不改变该反应的逆反应速率
B.增大反应体系的压强、反应速度一定增大
C.该反应是放热反应,降低温度将缩短反应达到平衡的时间
D.在t1、t2时刻,SO3(g)的浓度分别是c1,c2,则时间间隔t1~t2内, O2(g)消耗的平均速率为![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com