
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
K2CO3+6H2O![]() 2CH3OH+3O2+4KOH。请填空:
2CH3OH+3O2+4KOH。请填空:

图5
(1)充电时,①原电池的负极与电源____________极相连。②阳极的电极反应为________。
(2)放电时,负极的电极反应式为____________。
(3)在此过程中若完全反应,乙池中A极的质量升高648 g,则甲池中理论上消耗O2________L(标准状况下)。
(4)若在常温常压下,1 g CH3OH燃烧生成CO2和液态H2O时放热22.68 kJ,表示该反应的热化学方程式为_______________。
查看答案和解析>>
科目: 来源: 题型:
图3
(1)根据实验的需要,请从图4的A—E中选择合适的装置,将其序号填入以下空格内。
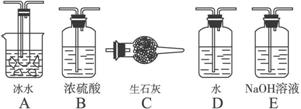
图4
图中I、Ⅱ、Ⅲ处所连接的装置分别为_______________________________。
(2)实验时,浓硫酸顺利地滴入烧瓶中,甲仪器所起作用的原理是________________________。
(3)从乙处均匀通入O2,为使SO2有较高的转化率,实验时,在加热与滴加浓硫酸过程中应采取的操作是____________________________。
(4)用大火加热烧瓶时,SO2的转化率会_____________(填“增大”“不变”或“降低”)。
(5)用a mol Na2SO3粉末与足量浓硫酸进行此实验,当反应结束时,继续通入O2一段时间后,称得Ⅲ装置质量增加b g,则本实验中SO2的转化率为__________。
查看答案和解析>>
科目: 来源: 题型:
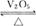
(1)写出下列物质的化学式:
A____________,E____________,F____________,Y____________。
(2)反应⑤的化学方程式为___________________。
(3)1 mol B通过反应②得到1 mol F,B中F的质量分数为72%,则B的化学式为____________。
查看答案和解析>>
科目: 来源: 题型:
(1)各取适量固体试剂分别加入6支试管中,加入适量蒸馏水,振荡试管,观察到的现象是_____________,被检出的物质的化学式(分子式)是________________。
(2)分别取未检出的溶液,往其中加入上述已检出的溶液,观察到的现象和相应的离子方程式是1支试管中有白色沉淀生成____________________,2支试管中有蓝色沉淀生成________________,被检出的物质的化学式(分子式)是___________。
(3)鉴别余下未检出物质的方法和观察到的现象是:
(i)______________________________________________________;
(ii)______________________________________________________。
查看答案和解析>>
科目: 来源: 题型:
(1)配平制取铁酸钠的化学方程式:
□Fe(NO3)3+□NaOH+□Cl2====Na2FeO4+□NaNO3+□NaCl+□_________
反应中______元素被氧化;每生成0.5 mol铁酸钠时,转移的电子为________mol。
(2)铁酸钠在消毒杀菌时本身被还原为Fe3+,Fe3+和水反应生成的氢氧化铁可吸附水中的悬浮杂质而沉降,写出Fe3+在水中生成氢氧化铁的离子方程式____________。
查看答案和解析>>
科目: 来源: 题型:
H2(g)+1/2O2(g)====H2O(l);ΔH=-285.8 kJ·mol-1
CO(g)+1/2O2(g)====CO2(g);ΔH=-283 kJ·mol-1
C8H18(l)+25/2O2(g)====8CO2(g)+9H2O (l);ΔH=-5518 kJ·mol-1
CH4(g)+2O2(g)====CO2(g)+2H2O(l);ΔH=-890.3 kJ·mol-1
相同质量的H2、CO、C8H18、CH4完全燃烧时,放出热量最少的是( )
A.H2(g) B.CO(g) C.C8H18(l) D.CH4(g)
查看答案和解析>>
科目: 来源: 题型:
Al2O3+N2+3C![]() 2AlN + 3CO
2AlN + 3CO
下列叙述正确的是( )
A.在氮化铝的合成反应中,N2是还原剂,Al2O3是氧化剂
B.上述反应中每生成2 mol AlN,N2得到3 mol电子
C.氮化铝中氮元素的化合价为-3
D.氮化铝晶体属于分子晶体
查看答案和解析>>
科目: 来源: 题型:
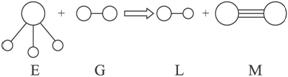
图2
A.G是最活泼的非金属单质 B.L是极性分子
C.E能使紫色石蕊试液变蓝色 D.M化学性质活泼
查看答案和解析>>
科目: 来源: 题型:
A.电解时在阳极得到氯气,在阴极得到金属钠
B.若在阳极附近的溶液中滴入KI溶液,溶液呈棕色
C.若在阴极附近的溶液中滴入酚酞试液,溶液呈无色
D.电解一段时间后,将全部电解液转移到烧杯中,充分搅拌后溶液呈中性
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com