
科目: 来源: 题型:
将乙醛和乙酸分离的正确方法是
A.加热蒸馏
B.先加入烧碱溶液,之后蒸馏出乙醛;再加入浓硫酸,蒸馏出乙酸
C.加入Na2CO3后,通过萃取的方法分离
D.利用银镜反应进行分离
查看答案和解析>>
科目: 来源: 题型:
通常情况下,多个羟基连在同一个碳原子上的分子结构是不稳定的,容易自动失水,生成碳氧双键的结构:![]()
下面是9个化合物的转变关系:
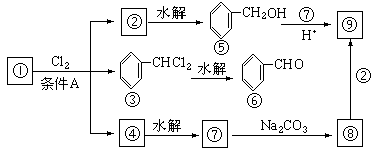
(1)化合物①是__________,它跟氯气发生反应的条件A是__________。
(2)化合物⑤跟⑦可在酸的催化下去水生成化合物⑨, ⑨的结构简式是:_______;名称是______________________________________。
(3)化合物⑨是重要的定香剂,香料工业上常用化合物⑧和②直接合成它。写出此反应的化学方程式。
查看答案和解析>>
科目: 来源: 题型:
有①、②、③、④、⑤、⑥、⑦、⑧、⑨、⑩十种元素,原子序数依次增大,⑨、⑩处于第四周期,其余均为短周期元素。
(1)若②、⑦、⑧三种元素在周期表中相对位置如下:
| ② | |||
| ⑦ | ⑧ |
②与⑦、②与⑧形成的液体化合物是常见的重要溶剂,则②、⑦、⑧三种元素最高价氧化物对应的水化物酸性由强到弱的顺序是:_________________________________(用化学式表示)。

|
|
换反应,反应b为化合反应。见右图示转化关系
推测:
戊可能为:__________________、___________________(列举合适的两例)。
若甲是O2、乙是N2H4,反应a是在强碱性溶液中进行的的原电池反应,则负极发生的电极反应式为:_______________________________________。
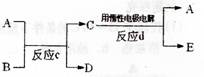 (3)若右下图中A、B、C、D、E分别是上述10种元素中的某些元素组成的单质或其中两种元素组成的化合物.已知:A是常见的金属
(3)若右下图中A、B、C、D、E分别是上述10种元素中的某些元素组成的单质或其中两种元素组成的化合物.已知:A是常见的金属
单质,反应C为置换反应类型。
若反应c是用A作电极,在B的水溶液中进
行电解反应,它们有如右图示转化关系。则反
应d中阴极的电极反应式为:________________________________________
若反应c是在高温下进行的,且为工业上有重要应用价值的放热反应,当物质C是一种两性化合物,则反应c的化学方程式为:________________________________________
查看答案和解析>>
科目: 来源: 题型:
重铬酸钠(Na2Cr2O7·2H2O)俗称红矾钠,在工业方面有广泛用途。我国目前主要是以铬铁矿(主要成份为FeO·Cr2O3,还含有Al2O3、MgO、SiO2等杂质)为主要原料进行生产,其主要工艺流程如下:

①中涉及的主要反应有:
主反应:4FeO·Cr2O3+8Na2CO3+7O2 ![]() 8Na2CrO4+2Fe2O3+8CO2
8Na2CrO4+2Fe2O3+8CO2
副反应:SiO2+Na2CO3![]() Na2SiO3+CO2↑、Al2O3+Na2CO3
Na2SiO3+CO2↑、Al2O3+Na2CO3![]() 2NaAlO2+CO2↑
2NaAlO2+CO2↑
部分阳离子以氢氧化物形式完全沉淀时溶液的pH:
| 沉淀物 | Al(OH)3 | Fe(OH)3 | Mg(OH)2 | Cr(OH)3 |
| 完全沉淀时溶液pH | 4.7 | 3.7 | 11.2 | 5.6 |
试回答下列问题:
⑴ “①”中反应是在回转窑中进行,反应时需不断搅拌,其作用是 ▲ 。两个副反应均为吸热反应,但在高温下均能自发进行,其原因是 ▲ 。
⑵ “③”中调节pH至4.7,目的是 ▲ 。
⑶ “⑤”中加硫酸酸化的目的是使CrO42-转化为Cr2O72-,请写出该平衡转化的离子方程式: ▲ 。
⑷ “⑦”中采用冷却结晶的方法析出红矾钠,依据是 ▲ 。
查看答案和解析>>
科目: 来源: 题型:
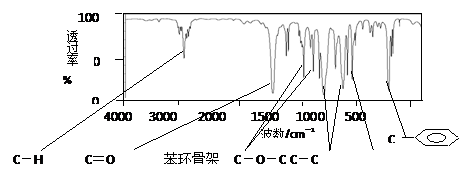
某酯A的化学式为C9H10O2,且A分子中只含有1个苯环,苯环上只有一个取代基。现测出A的1H-NMR谱图有5个峰,其面积之比为1︰2︰2︰2︰3。利用红外光谱仪可初步检测有机化合物中的某些基团,现测得A分子的红外光谱如下图:
 |
、
试回答下列问题。
(1)A的结构简式可为C6H5COOCH2CH3 C6H5CH2OOCCCH3、 。
(2)A的芳香类同分异构体有多种,请按要求写出其中不含甲基且属于芳香酸的B的结构简式: 。
(3)已知C是A的同分异构体,分子中不含甲基,且遇FeCl3溶液显紫色,苯环上只有两个对位取代基的芳香醛,且有如下转化关系。
 |
![]() ① 写出D E的化学方程式 。
① 写出D E的化学方程式 。
② 请用合成反应流程图表示出由C合成F的最合理的合成方案(注明反应条件)。
![]()
![]() 提示:合成反应流程图表示方法示例如下:
提示:合成反应流程图表示方法示例如下:
查看答案和解析>>
科目: 来源: 题型:
请仔细观察两种电池的构造示意图,回答下列问题:

(1)碱性锌锰电池的总反应式:Zn+2MnO2+2H2O=2MnOOH+Zn(OH)2,则负极的电极反应式:
(2)碱性锌锰电池比普通锌锰电池(干电池)性能好,放电电流大。试从影响反应速率的因素分析
其原因是
(3)某工厂回收废旧锌锰电池,其工艺流程如下:

已知:生成氢氧化物的pH如下表:
| 物质 | Fe(OH)3 | Fe(OH)2 | Zn(OH)2 | Mn(OH)2 |
| 开始沉淀pH | 2.7 | 7.6 | 5.7 | 8.3 |
| 完全沉淀pH | 3.7 | 9.6 | 8.0 | 9.8 |
①经测定,“锰粉”中除含少量铁盐和亚铁盐外,主要成分应是MnO2、Zn(OH)2 。
②第一次加入H2O2后,调节pH=8.0。目的
是 。
③试列举滤液4的应用实
例 。
查看答案和解析>>
科目: 来源: 题型:
过碳酸钠是一种有多用途的新型氧系漂白剂,化学式可表示为aNa2CO3·bH2O2。现将一定质量的过碳酸钠粉末溶于水配成稀溶液,再向其中加入适量MnO2粉末,充分反应后生成672mL气体(标准状况)。反应后的混合物经过滤、洗涤后,将滤液和洗涤液混合并加水配成100mL溶液A。现向三份体积为10mL、浓度为cmol/L的稀硫酸中分别逐滴滴入溶液A,边滴边振荡,充分反应后,测得实验数据如下表所示:
| 实验序号 | Ⅰ | Ⅱ | Ⅲ |
| 滴加溶液A的体积/mL | 5.0 | 10.0 | 15.0 |
| 生成气体的体积/mL(标准状况) | 44.8 | 89.6 | 112 |
⑴稀硫酸的物质的量浓度c= mol/L。
⑵计算确定过碳酸钠的化学式。
⑶工业上常以所含活性氧的质量分数[w(活性氧)=![]() ]来衡量过碳酸钠产品的优劣,13%以上者为优等品。
]来衡量过碳酸钠产品的优劣,13%以上者为优等品。
现将0.2g某厂家生产的过碳酸钠样品(所含杂质不参与后面的氧化还原反应)溶于水配成溶液,加入15.0mL 1mol/L硫酸,再加入足量KI,摇匀后置于暗处,充分反应后,加入少量淀粉试液,用0.1mol/L Na2S2O3溶液滴定到蓝色恰好消失时,共消耗33.00mL,试计算判断该样品是否为优等品。(已知:2Na2S2O3+I2=Na2S4O6+2NaI)
查看答案和解析>>
科目: 来源: 题型:
(2008年四川延考区卷)A和B是具有相同碳原子数的一氯代物,A-I转换关系如图所示:

根据框图回答下列问题;
(1)B的结构简式是 ;
(2)反应③的化学方程式是 ;
(3)上述转换中属于取代反应的是 ;(填写反应序号)
(4)图中与E互为同分异构体的是 ;(填化合物代号)。图中化合物带有的含氧官能团有 种。
(5)C在硫酸催化下与水反应的化学方程式是 ;
(6)I的结构简式是 ;名称是 。
查看答案和解析>>
科目: 来源: 题型:阅读理解
A.《物质结构与性质》
(1)前三周期元素中第一电离能最小的是 _______ (填元素符号),其基态原子的电子排布式为 _______ 。第二周期非金属元素形成的氢化物中化学键极性最大的是 _______
(填分子式),该物质在CCl4中的溶解度比在水中的溶解度 _______ (填“大”或“小”)。
 |
(3)晶格能的大小:MgO _______ NaCl,键能的大小:HBr _______ HI。(填“>”、“=”或“<”)
(4)下列物质的熔点高低顺序,正确的是 _______
A.金刚石>晶体硅>二氧化硅>碳化硅
B.CI4 > CBr4 > CCl4 > CH4
C.SiF4 > NaF > NaCl > NaBr
B《实验化学》
七水硫酸镁(MgSO4·7H2O)在印染、造纸和医药等工业上都有广泛的应用,利用化工厂生产硼砂的废渣-一硼镁泥可制取七水硫酸镁。硼镁泥的主要成分是MgCO3,还含有其他杂质(MgO、SiO2、Fe2O3、FeO、CaO、Al2O3、MnO等)。
表1 部分阳离子以氢氧化物形式完全沉淀时溶液的pH
| 沉淀物 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 | Mn(OH)2 | Mg(OH)2 |
| pH值 | 5.2 | 3.2 | 9.7 | 10.4 | 11.2 |
表2 两种盐的溶解度(单位为g/100g水)
| 温度 / ℃ | 10 | 30 | 40 | 50 | 60 |
| CaSO4 | 0.19 | 0.21 | 0.21 | 0.20 | 0.19 |
| MgSO4·7H2O | 30.9 | 35.5 | 40.8 | 45.6 | / |
硼镁泥制取七水硫酸镁的工艺流程如下:

根据以上流程图并参考表格pH数据和溶解度数据,试回答下列问题:
(1)过滤I的滤液中加入硼镁泥,调节溶液的pH=5~6,再加入NaClO溶液加热煮沸,将溶液中的Mn2+氧化成MnO2,反应的离子反应方程式为 _______ 。加热煮沸的主要目的是_ _______ 。
(2)沉淀B中除MnO2、SiO2外还含有 _______ (填化学式)等物质。
(3)检验过滤Ⅱ后的滤液中是否含有Fe3+的实验方法是 _______ ;
(4)沉淀C的化学式是 _______ 。过滤II需趁热过滤的理由是 _______
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com