
科目: 来源: 题型:
用NA表示阿伏加德罗常数,下列说法正确的是 ( )
① 18g D2O含有电子数为10 NA;
② 1 mol Na2O2与水完全反应时转移电子数为2NA ;
③ 1 mol C10H22分子中共价键总数为31NA ;
④在标准状况下,22.4 LSO3的物质的量为1 mol;
⑤7.8 g过氧化钠中含有的离子数为0.3NA;
⑥28 g 硅晶体中含有2 NA个Si—Si键 ;
⑦ 200 mL,1 mol / LFe2(SO4)3溶液中,Fe3+和SO42-离子数的总和是NA;
⑧在常温常压下,0.1mol铁与0.1mol Cl2充分反应,转移的电子数为0.3 NA;
⑨标准状况下,22.4 L NO和11.2 LO2混合后气体的分子总数为1.5 NA;
⑩ S2和S8的混合物共6.4g,其中所含硫原子数一定为0.2 NA
A.③⑤⑥⑩ B.①③⑤⑧ C.②④⑥⑦ D.③④⑤⑨
查看答案和解析>>
科目: 来源: 题型:
铝土矿(主要成分为Al2O3,还含有SiO2、Fe2O3)是工业上制备氧化铝的主要原料。工业上提取氧化铝的工艺流程如下:
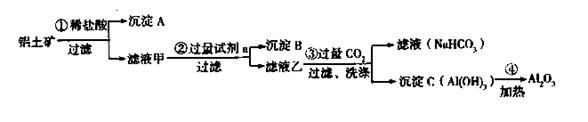
(1)沉淀A、B的成分分别是 、 ;
(2)步骤②中的试剂a是 ;
(3)试写出步骤③中发生反应的离子方式 ;
(4)在实验室模拟上述实验过程中,需要用到一定浓度的盐酸溶液。在配制250mi。该盐酸溶液时,某同学转移溶液的操作如图所示,图中的主要错误是:
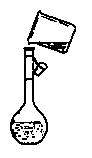
① ;
② 。
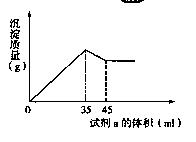
(4)准确称取6g铝土矿样品,加入100mL盐酸溶液,充分反应后向滤液中加入10 mol·L-1试剂a的溶液,产生沉淀的质量与加入试剂a的体积关系如图所示,则所用盐酸溶液的物质的量浓度为 ,样品中Al2O3的百分含量为 。
查看答案和解析>>
科目: 来源: 题型:
将2.5g碳酸钠、碳酸氢钠和氢氧化钠固体混合物完全溶解于水,制成稀溶液,然后向该溶液中逐滴加入1mol/L的盐酸,所加入盐酸的体积与产生CO2的体积(标准状况)关系如下图所示:
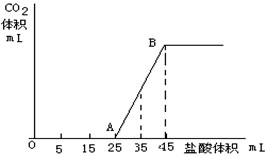
(1)写出OA段所发生反应的离子方程式 [来源:学_科_网]
(2)当加入35mL盐酸时,产生二氧化碳的体积为 mL(标准状况)
(3)原混合物中Na2CO3的质量分数为???? 。
查看答案和解析>>
科目: 来源: 题型:
青海昆仑玉被定为2008年北京奥运会奖牌用玉,昆仑玉主要成分是由“透闪石”和“阳起石”组成的纤维状微晶结合体,透闪石(Tremolite)的化学成分为Ca2Mg5Si8O22(OH)2.下列有关说法不正确的是 ( )
A.透闪石的化学式写成氧化物的形式为:2CaO·5MgO·8SiO2·H2O
B.透闪石中Mg元素的质量分数是Ca元素质量分数的1.5倍
C.1 mol Ca2Mg5Si8O22(OH)2与足量的盐酸作用,至少需要14 mol HCl
D.透闪石是一种新型无机非金属材料,难溶于水
查看答案和解析>>
科目: 来源: 题型:
在100 mL某混合溶液中,c(HNO3) = 0.4 mo/lL、c(H2SO4) = 0.1 mol/L,向其中加入1.92 g Cu粉,微热充分反应后溶液中的c(Cu2+)为 ( )
A.0.15mol/L B.0.225mo1/L C.0.3mo1/L D.无法计算
查看答案和解析>>
科目: 来源: 题型:
.定温度、压强和有铁触媒的条件下,在密闭容器中充入N2、H2和NH3 。若起始时n(N2)=x mol、n(H2)=y mol、n(NH3)=z mol (x、y、z均不为0 ),平衡时,n(N2)=0.1mol、n(H2)=0.3mol、n(NH3)=0.08mol。下列有关判断不合理的是( )
A.x : y =1 : 3
B.N2、H2的转化率不相等
C.平衡时,H2与NH3的生成速率之比为3 : 2
D.x的取值范围为0<x<0.14
查看答案和解析>>
科目: 来源: 题型:
取17.4 g MnO2固体粉末与一定体积的浓盐酸(含溶质0.4 mol)共热制取氯气(假设HCl挥发损失不计),下列叙述中正确的是
A.反应过程中MnO2作催化剂 B.盐酸未完全反应
C.被还原的HCl少于0.2 mol D.反应产生2.24 L氯气(标准状况)
查看答案和解析>>
科目: 来源: 题型:
下图表示在密闭容器中反应:
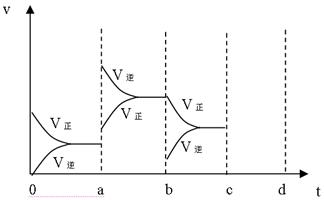
2SO2+O2![]() 2SO3 △H<0,达到平衡时,由于条件改变而引起反应速度和化学平衡的变化情况,a~b过程中改变的条件可能是 ;b~c过程中改变的条件可能是 ; 若增大压强时,反应速度变化情况画在c~d处.
2SO3 △H<0,达到平衡时,由于条件改变而引起反应速度和化学平衡的变化情况,a~b过程中改变的条件可能是 ;b~c过程中改变的条件可能是 ; 若增大压强时,反应速度变化情况画在c~d处.
查看答案和解析>>
科目: 来源: 题型:
单斜硫和正交硫转化为二氧化硫的能量变化图如右,回答下列问题:
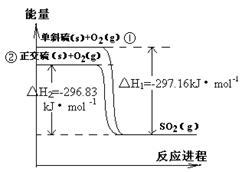
(1)正交硫的稳定性比单斜硫 (填“好”或“差”), 相同物质的量的正交硫比单斜硫所含有的能量 (填“高”或“低”),
①式表示断裂lmol单斜硫和 lmol O2中的共价键所吸收的能量比形成1mol SO2中的共价键所放出的能量 (填“多”或“少”297.16kJ。
(2)写出单斜硫转化为正交硫的热化学方程式:
查看答案和解析>>
科目: 来源: 题型:
2001年1月6日,我国525名两院院士投票评选出1999年中国十大科技进步奖,其中一项是:储氢碳纳米管研究获重大进展。电弧法合成的碳纳米管,常伴有大量杂质——纳米颗粒。这种碳纳米颗粒可用氧化汽化法提纯。
![]() 其反应式是3C+2 K2Cr2O7+ 8H2SO4 3CO2↑+2K2SO4+2Cr2(SO4)3+8H2O
其反应式是3C+2 K2Cr2O7+ 8H2SO4 3CO2↑+2K2SO4+2Cr2(SO4)3+8H2O
(1)单线法标出电子转移的数目和方向。
(2)此反应的氧化剂是 氧化产物是 。
(3)H2SO4在上述反应中表现出来的性质是 (填选项编号)
A、酸性 B、氧化性 C、吸水性 D、脱水性
(4)上述反应中若产生0.1mol气体物质,则转移电子的物质的量是 mol.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com