
科目: 来源: 题型:
下列有关元素化合物的说法正确的是( )
A.将饱和的FeCl3溶液加热至沸腾,出现红褐色液体时,停止加热,制得Fe(OH)3胶体。
B.将SO2通入BaCl2溶液,有白色沉淀生成,再加入硝酸,白色沉淀仍不消失
C.实验室检验氨气的方法是将湿润的蓝色石蕊试纸靠近瓶口或管口,观察试纸是否呈红色
D.在含Fe2O3、FeO、SiO2、Al2O3的矿石中,制备Fe2O3方法:可先用稀盐酸浸取炉渣,过滤;再将滤液先氧化,再加入过量NaOH溶液,再过滤,将沉淀洗涤、干燥、煅烧得Fe2O3。
查看答案和解析>>
科目: 来源: 题型:
化学与生活能源、环境等存在着密切的关系,下列有关说法中正确的是( )
A.厨房中使用液化天然气的过程都是化学变化
B. 多数合金的熔点一般比组成合金的各成分金属高
C.光导纤维的主要成分是二氧化硅,可广泛用于通信和医疗领域
D.二氧化硫、二氧化碳、二氧化氮、一氧化氮都是酸性气体,都属于大气污染物
查看答案和解析>>
科目: 来源: 题型:
有Wn+、Xm+、Ym-、Zn-四种离子(m>n),且W、X、Y、Z四种原子的M电子层上的电子数均为奇数。下列说法中正确的是
A.Wn+、Xm+、Ym-、Zn-的离子半径依次增大
B.Y、Z的气态氢化物的热稳定性:YHm>HnZ
C.W、X、Y、Z的最高价氧化物对应的水化物都是强电解质
D.W、X、Y、Z的最高价氧化物对应的水化物的碱性依次减弱,酸性依次增强
查看答案和解析>>
科目: 来源: 题型:
有机物A由碳、氢、氧三种元素组成。现取2.3 g A与2.8 L氧气(标准状况)在密闭容器中燃烧,燃烧后生成二氧化碳、一氧化碳和水蒸气(假设反应物没有剩余)。将反应生成的气体依次通过浓硫酸和碱石灰,浓硫酸增重2.7 g,碱石灰增重2.2 g。回答下列问题:
(1)2.3 g A中所含氢原子、碳原子的物质的量各是多少?
(2)通过计算确定该有机物的分子式。
查看答案和解析>>
科目: 来源: 题型:
要使饱和H2S溶液pH增大的同时,[S2─]减小,可向溶液中加入适量 ①NaOH溶液;②水;③SO2;④CuSO4固体;⑤盐酸 ( )
A.①③⑤ B.②④⑤ C.②③ D.③④⑤
查看答案和解析>>
科目: 来源: 题型:
近来,我国利用生产磷铵排放的废渣磷石膏制取硫酸并联产水泥的技术研究获得成功。具体生产流程如下:
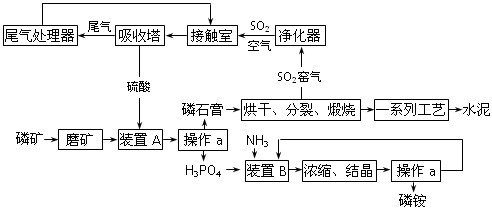
试填空:
⑴ 操作a的名称是 。制硫酸工艺中净化SO2窑气的目的是 。
⑵ 装置B中生成两种酸式盐,它们的化学式分别是 。
⑶ 制硫酸所产生的尾气除了含有N2、O2外,还含有SO2、微量的SO3和酸雾。能用于测定硫酸尾气中SO2含量的是 (选填字母序号)。
A.NaOH溶液、酚酞试液 B.氨水、酚酞试液
C.碘水、淀粉溶液 D.KMnO4溶液、稀硫酸
⑷ 将一定体积的SO2通入100mL 3.00mol/L的NaOH溶液,使其完全反应(加少量对苯二胺作抗氧化剂),得到钠盐23.0g,计算钠盐的成分及其物质的量。
查看答案和解析>>
科目: 来源: 题型:
“空气质量日报”中空气污染指数的项目包含:SO2、CO、NO2、O3和可吸入颗粒物等。
(1)血红蛋白中含有Fe2+,CO易与血红蛋白结合成稳定的配合物而使人中毒。
①写出亚铁离子的基态电子排布式 。
②根据等电子体原理,1个CO分子中含有的π键数目为 。
(2)为减轻SO2污染,火力发电厂生产中常在燃煤中加入CaO以“固硫”。科学家通过X射线探明,NaCl、KCl、MgO、CaO晶体结构相似,其晶格能数据如下表:
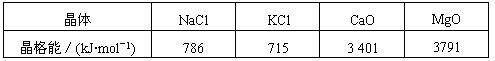
①4种晶体NaCl、KCl、MgO、CaO熔点由高到低的顺序是 。
②4种晶体的配位数均为 。
(3)随着人们生活质量的提高,不仅室外的环境安全为人们所重视,室内的环境安全和食品安全也越来越为人们所关注。
甲醛(HCHO)是室内主要空气污染物之一(其沸点是-19.5℃),甲醇(CH3OH)是“假酒”中的主要有害物质(其沸点是64.65℃),甲醇的沸点明显高于甲醛的主要原因
是: 。甲醛分子中碳原子的杂化方式是 。
查看答案和解析>>
科目: 来源: 题型:
根据表中提供的数据,判断下列说法正确的是
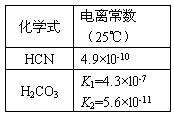 AB电离理论
AB电离理论
A、等浓度的NaCN、NaHCO3、Na2CO3溶液中,
pH(Na2CO3)>pH(NaCN)>pH(NaHCO3)
B、a mol/L HCN溶液与b mol/L NaOH溶液等体积混合后,
所得溶液中c(Na+)=c(CN-),则a一定大于b
C、等浓度的NaCN、NaHCO3混合溶液中,
c(Na+)+ c(H+) =c(CN-) + c(HCO3-) + c(OH-)
D、NaCN溶液中通入少量CO2,发生的反应可表示为
2NaCN + H2O + CO2 →2HCN + Na2CO3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com