
科目: 来源: 题型:
天然维生素P(结构如图)存在于槐树花蕾中,它是一种营养增补剂。关于维生素P的叙述错误的是 ( )
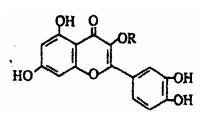
A.可以和溴水反应
B.可用有机溶剂萃取
C.分子中有三个苯环
D.1mol维生素P可以和4molNaOH反应
查看答案和解析>>
科目: 来源: 题型:
下列反应的离子方程式书写不正确的是 ( )
A.硫酸铜溶液和氢氧化钡溶液混合:Cu2+ + SO42-+ Ba2++2OH- Cu(OH)2↓+ BaSO4↓
B.Na2CO3溶液中加入醋酸:CO32-+2H+ CO2↑+H2O
C.澄清石灰水与少量小苏打溶液混合:Ca2+ + OH-+ HCO3- CaCO3↓+H2O
D.将金属Al加入强碱溶液中:2Al+2OH-+2H2O 2AlO2-+3H2↑
查看答案和解析>>
科目: 来源: 题型:
铅蓄电池是典型的可充型电池,它的正负极板是惰性材料,电池总反应式为:
![]() Pb+PbO2+4H++2SO42- 2PbSO4+2H2O
Pb+PbO2+4H++2SO42- 2PbSO4+2H2O
回答下列问题(不考虑氢、氧的氧化还原)
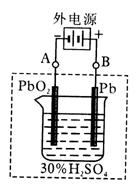
(1)放电时:正极的电极反应式是 ;电解液中H2SO4的浓度将变________,当外电路通过1.5mol电子时,理论上负极板的质量增加_______________g。
(2)在完全放电耗尽PbO2和Pb时,若按右图连接,电解一段时间后,则在A电极上生成__________,B电极上生成________,此时铅蓄电池的正负极的极性将____________。
查看答案和解析>>
科目: 来源: 题型:
某溶液既能溶解Al(OH)3,又能溶解H2SiO3,在该溶液中可以大量共存的离子组是
A.K+、Na+、HCO![]() 、NO
、NO![]() B.Na+、SO
B.Na+、SO![]() 、Cl—、ClO—
、Cl—、ClO—
C.H+、Mg2+、SO![]() 、NO
、NO![]() D.Ag+、K+、NO
D.Ag+、K+、NO![]() 、Na+
、Na+
查看答案和解析>>
科目: 来源: 题型:
重铬酸铵(NH4)2Cr2O7是一种受热易分解的盐,若是发生氧化还原反应而分解,下列各组对重铬酸铵受热分解产物的判断,可能符合事实的是:……………………( )
A.CrO3+NH3+H2O B.Cr2O3+ NH3+H2O
C.CrO3+N2+H2O D.Cr2O3+N2+H2O
查看答案和解析>>
科目: 来源: 题型:阅读理解
(1)已知可逆反应:M(g)+N(g)![]() P(g)+Q(g) ΔH>0,
P(g)+Q(g) ΔH>0,
若要增大Q的浓度,在其它条件不变的情况下可以采取的措施为 (填序号)。
A.加入一定量M B.降低反应温度 C.升高反应温度
D.缩小容器体积 E.加入催化剂 F.分离出一定量P
(2)盖斯定律在生产和科学研究中有很重要的意义。有些反应的反应热虽然无法直接测得,但可通过间接的方法测定。现根据下列3个热化学反应方程式:
Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g) △H=-24.8 kJ·mol-1
3Fe2O3(s)+ CO(g)==2Fe3O4(s)+ CO2(g) △H=-47.2 kJ·mol-1
Fe3O4(s)+CO(g)==3FeO(s)+CO2(g) △H=+640.5 kJ·mol-1
写出CO气体还原FeO固体得到Fe 固体和CO2气体的热化学反应方程式:
_________________ 。
(3)在体积为1 L的密闭容器中,充入1 mol CO2和3 mol H2,一定条件下发生反应: CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) ΔH=-49.0 kJ/mol, 测
CH3OH(g)+H2O(g) ΔH=-49.0 kJ/mol, 测
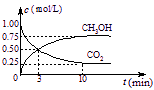 得CO2和CH3OH(g)的浓度随时间变化如右图所示。
得CO2和CH3OH(g)的浓度随时间变化如右图所示。
①从3 min到10 min,v(H2)= mol/(L·min)。
②能说明上述反应达到平衡状态的是 (选填编号)。
A.反应中CO2与CH3OH的物质的量浓度之比为1︰1(即图中交叉点)
B.混合气体的密度不随时间的变化而变化
C.单位时间内每消耗3 mol H2,同时生成1 mol H2O
D.CO2的体积分数在混合气体中保持不变
③下列措施中能使n (CH3OH)/n (CO2)增大的是 (选填编号)。
A.升高温度 B.恒温恒容充入He(g)
C.将H2O(g)从体系中分离 D.恒温恒容再充入1 mol CO2和3 mol H2
查看答案和解析>>
科目: 来源: 题型:
将铜片和铝片用导线连接后插入盛有浓硝酸的烧杯中组成原电池,此原电池的负极及其电极反应分别是
A. Al, Al- 3e-=Al3+ B. Cu, Cu-2e-=Cu2+
C. Al, 2H++2e-=H2↑ D. Cu, 2H++NO3-+e-=NO2↑+H2O
查看答案和解析>>
科目: 来源: 题型:
下列说法正确的是
A.将AgCl放入水中不能导电,故AgCl不是电解质
B.CO2溶于水得到的溶液能导电,所以CO2是电解质
C.金属能导电,所以金属是电解质
D.固态的NaCl不导电,熔融态的NaCl能导电,NaCl是电解质
查看答案和解析>>
科目: 来源: 题型:
在密闭容器中加入等浓度的CO与H2O,T ℃时发生如下反应:CO(g)+H2O(g) ![]() CO2(g)+H2(g) ΔH <0已知CO的浓度变化如图所示。
CO2(g)+H2(g) ΔH <0已知CO的浓度变化如图所示。

⑴从0~4 min,该反应的平均速率v(CO)= mol/(L·min)。该反应的平衡为 。
⑵为了增大CO的转化率,可以采取的措施有 。
a.增大反应物中CO的浓度
b.降低反应温度
c.将密闭容器体积压缩至一半
d.加入适宜的催化剂
⑶若不改变反应温度和反应物中CO的起始浓度,使CO的转化率达到90%,则水蒸气的起始浓度至少为 mol/L。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com