
科目: 来源: 题型:
关于下列四个图象的说法中正确的是( )
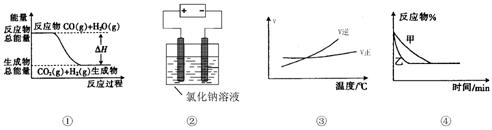
A.图①表示可逆反应“![]()
![]()
![]() ”中的
”中的![]() 小于0
小于0
B.图②是在电解氯化钠稀溶液的电解池中,阴、阳极能收集到的气体体积之比一定为1:1
C.图③表示可逆反应![]()
![]()
![]() 的
的![]() 大于0
大于0
D.图④表示压强对可逆反应![]()
![]()
![]() 的影响,乙的压强大
的影响,乙的压强大
查看答案和解析>>
科目: 来源: 题型:
用铁片稀H2SO4反应制取氢气时,下列措施不能使氢气生成速率加大的是
A.加热 B.不用稀H2SO4改用98%的浓H2SO4
C.滴加少量CuSO4溶液 D.不用铁片,改用铁粉
查看答案和解析>>
科目: 来源: 题型:
下列关于甲苯的实验事实中,能说明侧链对苯环性质有影响的是:
A.甲苯通过硝化反应生成三硝基甲苯 B.甲苯能使酸性高锰酸钾溶液褪色
C.甲苯燃烧时产生浓烈的黑烟 D.1mol甲苯可与3mol氢气发生加成反应
查看答案和解析>>
科目: 来源: 题型:
实验目的:探究(一)同周期元素性质的递变规律
探究(二)影响化学反应速率的因素
供选试剂:锌片、锌粉、铁片、铁粉、镁条、铝条、新制Na2S溶液、新制氯水、
0.5mol/L盐酸、3mol/L盐酸等试剂(实验仪器自选)。
现有A同学设计的部分实验方案,请你帮他填写完整,并作出评价。
【实验探究一】同周期元素金属性和非金属性的递变规律
| 实验步骤 (画图表示,参照下图) | 实验现象 | 实验结论 | |
| 非金属性递变 | |||
| 金属性递变 |
【实验探究二】影响化学反应速率的因素
实验步骤 | 实验现象 | 实验结论 |
|
(锌片和锌粉的质量相同,盐酸均过量) | 均有气体生成,锌粉比锌片消失快。 | 反应物接触面积越大,反应速率越快 |
A同学在[实验探究二]中所得结论不够严谨。原因是___________________________。
在不改变实验探究二所做实验的前提下,再补充一些实验即可完成有关探究,补充实验是(写最简方案,可不填满,也可增加):
①_________________________________;
②_________________________________;
③_________________________________。
查看答案和解析>>
科目: 来源: 题型:
胡椒粉是植物挥发油的成分之一。它的结构式为HO—![]() —CH2CH=CH2,下列叙述中不正确的是( )
—CH2CH=CH2,下列叙述中不正确的是( )
A.1mol胡椒粉最多可与4mol氢气发生反应
B.1mol胡椒粉最多可与4mol溴发生反应
C.该化合物不属于芳香烃
D.分子中至少有7个碳原子处于同一平面
查看答案和解析>>
科目: 来源: 题型:
苯的含氧衍生物A的相对分子质量为180,其中碳元素的质量分数为60%,A完全燃烧消耗O2的物质的量与生成CO2的物质的量相等。A的苯环上取代基彼此相间,A能发生银镜反应,也能与NaHCO3溶液反应产生CO2 ,还能与FeCl3溶液发生显色反应。
(1)A的分子式为__________。
(2)A含有的官能团名称是_____ , , 。
写出A可能的一种结构简式: _____ ________ _____。
(3)A的一种同分异构体B是邻位二取代苯,其中一个取代基是羧基,B能发生图示转化:
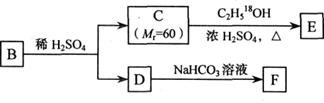
写出下列反应的化学方程式:
①C→E____________________________________
②D与浓溴水反应__________________________________________________
③B与足量NaOH溶液共热________________________________________
查看答案和解析>>
科目: 来源: 题型:
设NA为阿伏加德罗常数,下列叙述中正确的是
A.在含有4mol Si—O键的石英晶体中,氧原子的数目为2NA
B.常温常压下,2.24L 氯气与过量的氢氧化钠溶液完全反应转移的电子数为0.1NA
C.标准状况下,1L辛烷完全燃烧后,所生成气体产物的分子数为8NA/22.4
D.0.1L 2mol??L-1的(NH4)2S溶液中含有的S2-数目为0.2 NA
查看答案和解析>>
科目: 来源: 题型:
 一定质量的甲烷燃烧后得到的产物为CO、CO2和水蒸气,此混合气体质量为49.6g,当其缓慢经过无水CaCl2时,CaCl2增重25.2g。原混合气体中CO2的质量为( )
一定质量的甲烷燃烧后得到的产物为CO、CO2和水蒸气,此混合气体质量为49.6g,当其缓慢经过无水CaCl2时,CaCl2增重25.2g。原混合气体中CO2的质量为( )
A.12.5g B.13.2g C.19.7g D.24.4g
查看答案和解析>>
科目: 来源: 题型:
A.氢气是重要而洁净的能源,要利用氢气作能源,必须安
全有效地储存氢气。
(1)某种铜镍合金材料有较大的储氢容量,
其晶体结构如图所示。这种合金中La与Ni
的原子个数比为 ;其中基态Ni
原子的核外电子排布式为 。
(2)氢元素可与其他四种短周期元素a、b、c、d、e、f、g等七种微粒,它们都有10个电子,其填结构特点如下表:
| 微粒 | a | b | c | d | e | f | g |
| 原子核数 | 双核 | 双核 | 三核 | 四核 | 四核 | 五核 | 五核 |
| 所带单位电荷 | 0 | -1 | 0 | 0 | +1 | +1 |
①与c互为等电子体的一种阴离子是 (填化学式);
②微粒中中心原子的杂化方式为 杂化。
③比较相同条件下a与f在水中的溶解度:a f(填“>”、“=”或“<”)
 ④Ni2+可与d形成配位数为6的配离子,该配离子的化学式为 。
④Ni2+可与d形成配位数为6的配离子,该配离子的化学式为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com