
科目: 来源: 题型:
蓄电池是一种可反复充电、放电的装置。它放电时起原电池的作用,将化学能转变为电能;而充电时电解池的作用,将电能转变为化学能贮存起来。某蓄电池充电和放电时发生的反应为:Fe + NiO2 + 2H2O![]() Fe(OH)2 + Ni(OH)2关于此蓄电池有下列说法:
Fe(OH)2 + Ni(OH)2关于此蓄电池有下列说法:
放电时,NiO![]() 为正极;
为正极;
②充电时,阳极反应式为:Fe(OH)![]() +2e-→ Fe+2OH
+2e-→ Fe+2OH![]() ;
;
③放电时,电解质溶液中的阳离子向正极方向移动;
④充电时,Ni(OH) ![]() 的反应式为:Ni(OH)
的反应式为:Ni(OH) ![]() →NiO
→NiO![]() +2H
+2H![]() +2e-;
+2e-;
⑤蓄电池的电极必须浸在碱性电解质溶液中;错误的是
A。 ③ B。② C。①③⑤ D。 ②和④
查看答案和解析>>
科目: 来源: 题型:
以钛铁矿(主要成分是FeTiO3 ,钛酸亚铁)为主要原料冶炼金属钛,生产的工艺流程图如下,其中钛铁矿与浓硫酸反应的化学方程式为:
FeTiO3 + 2 H2SO4 == TiOSO4 + FeSO4 + 2 H2O
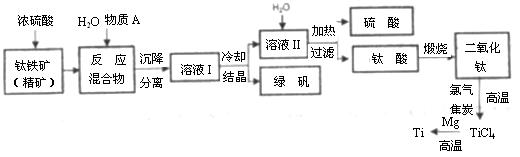
试回答下列问题:
(1)钛铁矿和浓硫酸反应属于 (选填“氧化还原反应”或“非氧化还原反应”)。
(2)上述生产流程中加入物质A的目的是防止Fe2+被氧化,物质A是 ;上述制备TiO2的过程中,所得到的副产物和可回收利用的物质分别是 。
(3)反应TiCl4 + 2 Mg == 2 MgCl2 + Ti 在Ar气氛中进行的理由是:
。
(4)如果取钛铁矿A吨,生产出钛B吨,(不考虑损耗),计算钛铁矿中钛的含量(用A、B字母表示) 。
查看答案和解析>>
科目: 来源: 题型:
某种存在于茶叶中的有机物A(C9H8O3),其分子中所含的苯环上有2个取代基,取代基上不含支链,且苯环上的一氯代物只有2种;A遇FeCl3溶液发生显色反应。F分子中除了2个苯环外,还有一个六元环。它们的转化关系如下图:
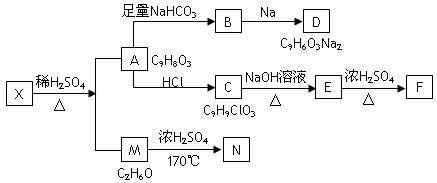
请回答下列问题:
(1)有机物A中含氧官能团的名称是__________________________________;
(2)写出X、F的结构简式X 、F
(3)写出下列反应的化学方程式
A→B:__________________________________________________________;
M→N:_________________________________________________________;
(4)A→C的反应类型为____________,E→F的反应类型为_______________;
(5)1mol A可以和___________mol Br2反应;
(6)某营养物质的主要成分(分子式为C16H14O3)是由A和一种芳香醇R发生酯化反应生成的,则R的同分异构体中含有苯环的有___________种(不包括R);
(7)A→C的过程中还可能有另一种产物C1,请写出C1在NaOH水溶液中反应的化学方程式_____________________________________________________________。
查看答案和解析>>
科目: 来源: 题型:
下列五种物质中,①H2O ②CO2 ③Na2O2 ④NaOH ⑤NaBr,只存在共价键的是__________,只存在离子键的是__________,既存在离子键又存在共价键的是_________,含有极性键的是__________,是非极性分子的是________。(填编号)^S*5U.C#O%下
查看答案和解析>>
科目: 来源: 题型:
下列各组表述中,两个微粒不属于同种元素原子的是( )
A.3p能级有一个空轨道的基态原子和核外电子的排布为1s22s22p63s23p2的原子
B.2p能级无空轨道,且有一个未成对电子基态原子和原子的最外层电子排布为2s22p5的原子
C.最外层电子数是核外电子总数的1/5的原子和价电子排布为4s24p5的原子
D.M层全充满而N层为4s2的原子和核外电子排布为1s22s22p63s23p63d64s2
查看答案和解析>>
科目: 来源: 题型:
A、B、C、D、E是同一周期的五种主族元素,A和B的最高价氧化物对应的水化物均呈碱性,且碱性B>A,C和D的气态氢化物的稳定性C>D;E是这五种元素中原子半径最小的元素,则它们的原子序数由小到大的顺序是( )
A.A、B、C、D、E B.E、C、D、B、A
C.B、A、D、C、E D.C、D、A、B、E
查看答案和解析>>
科目: 来源: 题型:
下图所涉及的物质均为中学化学中的常见物质,其中C为气体单质一种主要成分、D在常温下是黄绿色气体、E为Fe单质,其余为化合物。它们存在如下转化关系,反应中生成的水及次要产物均已略去。
(1)写出有关物质的化学式

F ,G ,H 。
(2)指出MnO2在相关反应中的作用,反应①中是 剂,反应②中是 剂。
(3)若反应①是在加热条件下进行,则A是 ;若反应①是在常温条件下进行,则A的电子式为 。
(4)写出B与MnO2共热获得D的离子方程式
。
(5)写出B与F反应的化学方程式 。
查看答案和解析>>
科目: 来源: 题型:
元素在周期表中的位置,反映了元素的原子结构和元素的性质。下列说法正确的是
A.同一元素不可能既表现金属性,又表现非金属性
B.第三周期元素的最高正化合价等于它所处的主族序数
C.短周期元素形成离子后,最外层都达到8电子稳定结构
D.同一主族的元素的原子,最外层电子数相同,化学性质完全相同
查看答案和解析>>
科目: 来源: 题型:
某100mL混合酸中,HNO3物质的量浓度为0.4mol/L,H2SO4物质的量浓度为0.2mol/L。向其中加入2.56克Cu粉,待充分反应后,溶液中Cu2+物质的量浓度为
A. 0.15mol/L B. 0.3mol/L C.0.225mol/L D. 无法计算
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com