
科目: 来源: 题型:
下列叙述不正确的是
A.工业上可用碳在高温下还原二氧化硅制取硅。
B.工业上可用氯气和石灰乳为原料制造漂白粉。
C.镁条不能在二氧化碳气体中燃烧。
D.将盛有氢氧化铁胶体的烧杯置于暗处,用一束光照射,从垂直于光线的方向可以观察到一条光亮的通路。
查看答案和解析>>
科目: 来源: 题型:阅读理解
理论上,SO2能发生类似CO2与澄清石灰水作用的反应,但在通常实验中,将SO2通入澄清石灰水却没有看到类似CO2那样先浑浊后澄清的现象。针对这一问题,研究性学习小组开展了探究性实验。
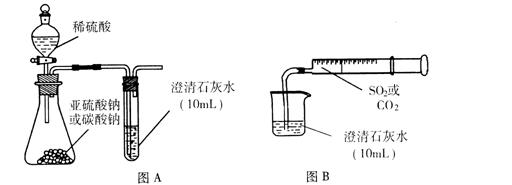
I.用图A所示的装置来分别做CO2、SO2与澄清石灰水的反应实验,结果通人CO2可看到先浑浊后澄清的现象,但通入SO2没看到浑浊现象。
Ⅱ.用图B的装置,将气体收集在注射器里,缓慢地将气体一个气泡一个气泡地通入澄清石灰水中,无论CO2还是SO2都能看到“先变浑再澄清”的现象。当以相同速率分别通人CO2或SO2,通入SO2产生现象明显比通入CO2产生现象快。
回答下列问题:
(1)通过上述I、Ⅱ实验,可以确定,将足量SO2缓慢通人澄清石灰水,依次发生的反应有:(用离子方程式表示) ; 。
(2)实验I中,通人SO2不能出现浑浊的原因可能是: 。
(3)实验Ⅱ中,同速率分别通入CO2或SO2,SO2产生现象比CO2快的相关因素有 。
①SO2在水中溶解度比CO2大。
②相同状态下,SO2的密度比CO2的密度大。
③亚硫酸酸性比碳酸强,在同温度、同体积的溶液中,l mol亚硫酸电离产生的H+离子浓度大于l mol碳酸电离产生的H+离子浓度。
④SO2有毒和刺激性气味,CO2无毒和无刺激性气味。
⑤相同条件下,1 mol SO2与足量石灰水反应生成CaSO3的速率大于1 mol CO2与足量石灰水反应生成CaCO3的速率。
⑥相同条件下,1 molCaSO3被1mol SO2(形成的H+离子)溶解形成可溶性Ca(HSO3)2
的速率大于1molCaCO3被1molCO2(形成的H+离子)溶解形成可溶性Ca(HCO3)2的速率。
查看答案和解析>>
科目: 来源: 题型:
氮化硅(Si3N4)是一种新型陶瓷材料,它可由石英与焦炭在高温的氮气流中,通过以下反应制得:3SiO2+6C+2N2 ![]() Si3N4+6CO。下列叙述正确的是
Si3N4+6CO。下列叙述正确的是
A.在氮化硅的合成反应中,N2是还原剂,SiO2是氧化剂
B.上述反应中每生成1molSi3N4,N2得到12mol电子
C.若已知上述反应为放热反应,升高温度,上述平衡向正反应方向移动
D.若使压强增大,上述平衡向正反应方向移动
查看答案和解析>>
科目: 来源: 题型:
(1)工业上以粗铜为原料采取如图所示流程制备硝酸铜晶体:
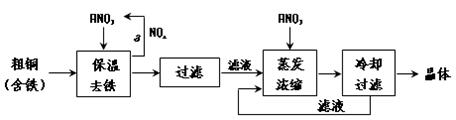
①在步骤a中,还需要通入氧气和水,其目的是 。
②在保温去铁的过程中,为使Fe3+沉淀完全,可以向溶液中加入CuO,调节溶液的pH,根据下表数据,溶液的pH应保持在 范围。
| 氢氧化物开始沉淀时的pH | 氢氧化物沉淀完全时的pH | |
| Fe3+ Cu2+ | 1.9 4.7 | 3.2 6.7 |
不用加水的方法调节溶液pH的原因是 。
③进行蒸发浓缩时,要用硝酸调节溶液的pH=1,其目的是(结合离子方程式说明) 。
(2)工业上常利用硝酸铜溶液电镀铜,电镀时阴极的电极反应式是 。
(3)图-2是某小组同学查阅资料所绘出的硝酸铜晶体[ Cu(NO3)2·nH2O ]的溶解度曲线(温度在30℃前后对应不同的晶体),下列说法正确的是 (填字母)。

a. A点时的溶液为不饱和溶液
b. B点时两种晶体可以共存
c. 按上述流程最终得到的晶体是Cu(NO3)2·3H2O
d. 若将C点时的溶液降温至30℃以下,可以析出Cu(NO3)2·6H2O晶体
查看答案和解析>>
科目: 来源: 题型:
关于下列各装置图的叙述中,不正确的是
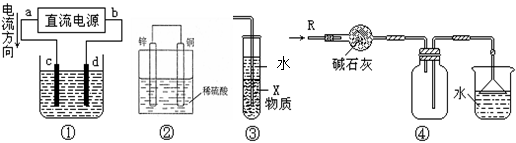
A.若采用装置①精炼铜,则d极为粗铜,c极为纯铜,电解质溶液为CuSO4溶液。
B.装置②是原电池,能将化学能转化为电能,锌电极发生氧化反应
C.装置③中X若为四氯化碳,可用于吸收氨气或氯化氢,并防止倒吸
D.装置④可用于干燥、收集氨气,并吸收多余的氨气
查看答案和解析>>
科目: 来源: 题型:
NaH是一种离子化合物,它跟水反应的方程式:NaH + H2O=NaOH + H2↑,它跟液氨、乙醇等发生类似反应,并都产生氢气。下列有关NaH的叙述错误的是
A、跟水反应时,水作氧化剂 B、NaH 中H- 半径比Li+ 半径小
C、跟液氨反应时,有NaNH2生成 D、跟乙醇反应时,NaH被氧化
查看答案和解析>>
科目: 来源: 题型:
下表中的实线表示元素周期表的部分边界。①-⑥分别表示元素周期表中对应位置的元素。
| ① | ] | ||||||||||||||||
| ] | ③ | ④ | ⑤ | ||||||||||||||
| ② | ⑥ | ||||||||||||||||
| |||||||||||||||||
(1)请在表中用粗实线补全元素周期表边界。
(2)②号元素位于第 周期 族。
(3)写出由①、③两种元素组成的摩尔质量最小的化合物的电子式 ,上述元素中能和⑤号元素形成的原子晶体的化学式是
(4)上述元素中的一种元素其气态氢化物和该元素的最高价氧化物的水化物能发生化合反应,该反应的化学反应方程式为_____________,该生成物质含有的化学键类型是 。
查看答案和解析>>
科目: 来源: 题型:
下列对分子结构叙述不正确的是
A.H2O2分子中,两个O之间形成1对共用电子对
B.SiO2晶体中,1个Si原子与2个O原子形成两个共价键
C.有机化合物CH3—CH2—NO2和H2N—CH2—COOH是同分异构体
D. 分子晶体溶于水时,分子中的化学键可能被破坏
查看答案和解析>>
科目: 来源: 题型:
某FeSO4、Fe2(SO4)3、H2SO4的混合溶液100mL,已知溶液中阳离子的浓度相同(不考虑水解),且SO42—的物质的量浓度为6mol/L,则此溶液最多可溶解铁粉的质量为
A.11.2 g B.16.8 g C.19.6 g D.22.4 g
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com