
科目: 来源: 题型:
下列叙述正确的是
A.在原电池的负极和电解池的阴极上都发生失电子的氧化反应
B.用惰性电极电解Na2SO4溶液,阴阳两极产物的物质的量之比为1∶2
C.用惰性电极电解饱和NaCl溶液,若有1 mol电子转移,则生成1 mol NaOH
D.镀层破损后,镀锡铁板比镀锌铁板更耐腐蚀
查看答案和解析>>
科目: 来源: 题型:
下列说法正确的是 ( )
A.离子化合物一定为离子晶体
B.同周期主族元素的原子半径或离子半径都是从左至右减小
C.氢氧化铁胶体带正电荷,加入电解质会产生红褐色沉淀
D.两个非金属元素的原子之间形成的化学键只能是共价健
查看答案和解析>>
科目: 来源: 题型:
有8种物质:①甲烷;②苯;③聚乙烯;④苯乙烯;⑤丁炔;⑥环己醇;⑦邻二甲苯;⑧二氧化硫。既能使酸性高锰酸钾溶液褪色又能与溴水反应使之褪色的是( )
A.③④⑤⑧ B.④⑤⑧ C.④⑤⑦⑧ D. ③④⑤⑦⑧
查看答案和解析>>
科目: 来源: 题型:
A、B、C三种短周期元素在元素周期表中的相对位置如图所示,已知A、C可分别与B形成化合物X和Y,A与B的质子数之和为C的质子数,现有以下说法,其中判断正确的组合是 ( )

①B与C均存在同素异形体
②X的种类比Y的多
③沸点:A的氢化物小于C的氢化物
④C的最高价氧化物对应水化物能与A的氢化物形成三种盐
A.①②③④ B.②③ C.①②④ D.①④
查看答案和解析>>
科目: 来源: 题型:
能源短缺是人类社会面临的重大问题。甲醇是一种可再生能源,具有广泛的开发和应用前景。
(1)工业上一般采用下列两种反应合成甲醇:
反应I:CO(g) + 2H2(g) ![]() CH3OH(g) ΔH1
CH3OH(g) ΔH1
反应II: CO2(g) + 3H2(g) ![]() CH3OH(g) + H2O(g) ΔH2
CH3OH(g) + H2O(g) ΔH2
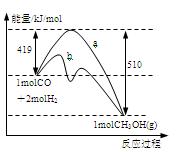
右图是反应I反应过程中的能量变化曲线。
(1)由右图可知反应I为 反应(选填”吸热、放热”),反应热△H1=
(2)反应I在一定体积的密闭容器中进行,能判断其是否达到化学平衡状态的依据是 。
A.容器中压强不变 B.混合气体中c(CO)不变
C.v正(H2)=v逆(CH3OH) D.c(CO)=c(CH3OH)
(3)图中曲线 表示使用催化剂时反应的能量变化。
(4)一定条件下,向体积为2 L的密闭容器中充入2 mol CO2和6 mol H2,一段时间后达到平衡状态,测得CH3OH(g)的物质的量为1mol,则此条件下该反应的化学平衡常数数
K值= (用分数表示),若开始时充入2 mol CH3OH(g) 和2 mol H2O(g)达到相同平衡时CH3OH的转化率为 ,若平衡后在充入4 mol的N2,则C(CO2)是 。
(5)从绿色化学的角度比较上述两种方法,符合原子经济的是 。(填“I” 或“II”)
查看答案和解析>>
科目: 来源: 题型:
在NaCl溶液中滴加AgNO3溶液,再滴加KI溶液,下列描述正确的是:
A.先产生白色沉淀后产生黄色沉淀
B.先产生白色沉淀后无明显现象
C.先产生黄色沉淀后产生白色沉淀
D.实验证明AgCl溶解度小于AgI溶解度。
查看答案和解析>>
科目: 来源: 题型:阅读理解
阅读分析材料,据此完成下列要求:
短周期元素A.B.C.D.E.F,它们的原子序数依次增大,其中B和C为同一周期;D.E.F为同一周期;A和D.C和F分别为同一主族;C元素原子的最外层电子数是次外层电子数的3倍;D是所在周期原子半径最大的元素(除稀有气体外);E是非金属元素,其单质在电子工业中有重要用处。
⑴A元素与碳元素按质量比1:3可以形成化合物X,将C2.X和23.4gD2C2置于密闭容器中,用电火花引起化学反应,反应结束后,容器内的气压为零(250℃),将残留物溶于水中,无气体产生,则C2与X的物质的量之比为 。根据其反应方程式分析,若反应中有4mol电子转移,则消耗C2的物质的量为 mol。
⑵工业上生产单质E的化学方程式为: ;指出E的氧化物在通讯中的一种用途 。
⑶一定条件下,A2气体与B2气体充分反应可生成6.8g空间构型三角锥形的气体,放出18.44kJ热量,则该反应的热化学方程式为为: ;A与B按原子个数比1:2可形成相对原子质量为32的化合物,写出该化合物与足量盐酸反应的离子方程式 。
⑷A2与C2在KOH的浓溶液中可以形成原电池。如果以Pt为电极,在电池的两极分别通入A2和C2,则通入的A2一极的电极反应式为: 。
⑸在10L的密闭容器中,通入2molFC2和3molC2气体,一定条件下反应后生成FC3气体,当反应达到平衡时,C2的浓度为0.21mol/L,则平衡时FC2的转化率为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com