
科目: 来源: 题型:
在一无色未知液中已检出有Al3+存在,在此溶液中能大量共存的离子组是
A.Na+、NH4+、NO3-、Cl- B.K+、Na+、HCO3-、B-
C.Na+、H+、NO3-、S- D.K+、Fe2+、NO3-、Cl-
查看答案和解析>>
科目: 来源: 题型:
某无色溶液,由Na+、Ba2+、Al3+、AlO2-、Fe3+、CO32-、SO42-中的若干种组成。取适量该溶液进行如下实验:
①加入过量盐酸,有气体生成;
②在上面所得的溶液中再加入过量碳酸氢铵溶液,有气体生成,同时析出白色沉淀甲;
③在②所得溶液中再加入过量Ba(OH)2溶液,也有气体生成,并有白色沉淀乙析出。
(1)则原溶液中一定不能大量存在的离子是 ,可能存在的离子是 。
(2)实验①中发生反应的离子方程式为 , 。
(3)实验②中气体成分是 ,沉淀甲的成分是 。
(4)实验③中气体成分是 ,沉淀乙的成分是 。
查看答案和解析>>
科目: 来源: 题型:
A、B、C、X均为中学常见的纯净物,它们之间有如下转化关系(副产物已略去)。
试回答:
![]()
(1)若X是强氧化性单质,则A不可能是 。
a.Mg b.C c.N2 d.S
(2)若X是金属单质,向C的水溶液中滴加AgNO3溶液,产生不溶于稀HNO3??的白色沉淀,则B的化学式为 ;C溶液在贮存时应加入少量X,理由是(用 必 要的文字说明和离子方程式表示) , 。
(3)若A、B、C为含金属元素的无机化合物,X为强电解质,A溶液与C溶液反应生成B,则A与C的反应的离子方程式为 ,X的化学式可能为(写出一种即可) 。
查看答案和解析>>
科目: 来源: 题型:阅读理解
硫酸铵是一种常用的铵态氮肥。下表是硫酸铵化肥品质的主要指标。
| 项目 | 指 标 | ||
| 优等品 | 一等品 | 合格品 | |
| 外观 | 白色结晶,无可见机械杂质 | 无可见机械杂质 | |
| 氮(N)含量 | ≥21.0﹪ | ≥21.0﹪ | ≥20.5﹪ |
新华中学化学研究性学习小组为本地农业生产服务,对某农用品商店出售的一等品硫酸铵化肥的品质进行探究。
[观察外观]该硫酸铵化肥无可见机械杂质。
[实验探究]按右图所示装置进行实验。
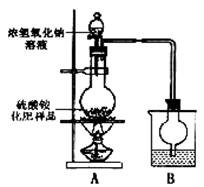
(1)①盛放浓氢氧化钠溶液的仪器名称是
②烧瓶内发生反应的离子方程式为:
______ __________
③烧杯中最适宜盛放的试剂是__________
A.浓硫酸 B.稀硫酸
C.盐酸 D.氨水
④B装置中为何不将导管直接插入试剂中
(2)实验过程中,需往烧瓶中加入足量浓氢氧化钠溶液并充分加热的原因是
_____________________________
[交流讨论]甲同学:根据此实验测得的数据,计算硫酸铵化肥的氮含量可能偏高,因为实验装置A和B间存在一个明显缺陷是:________________________ 乙同学:根据甲同学改进后计算硫酸铵化肥的氮含量又可能偏低,因为实验装置中还存在另一个明显缺陷是:____________________________
经过大家充分讨论一致认为:针对甲、乙两位同学指出的实验装置中存在的明显缺陷,需改进实验装置,重新进行实验。
[探究结论] 称取13.5g硫酸铵化肥样品,用改进后的实验装置重新进行实验,测得实验前后B装置增重3.40g。该化肥______ ___(填“是”或“不是”)一等品。
查看答案和解析>>
科目: 来源: 题型:
下图所示装置中,甲、乙、丙三个烧杯依次分别盛放100g5.00%的NaOH溶液、足量的CuSO4溶液和100gl0.00%的K2SO4溶液,电极均为石墨电极。
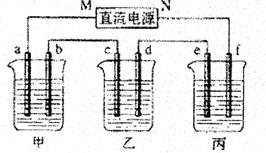
(1)接通电源,经过一段时间后,测得丙中K2SO4浓度为10.47%,乙中c电极质量增加。据此回答问题:
①电源的N端为 极;
②电极b上发生的电极反应为 ;
③列式计算电极b上生成的气体在标准状况下的体积: ;
④电极c的质量变化是 g;
⑤电解前后个溶液的酸,碱性大小是否发生变化,简述其原因:
甲溶液 ;
乙溶液 ;
丙溶液 ;
(2)如果电解过程中铜全部析出,此时电解能否继续进行,为什么?
查看答案和解析>>
科目: 来源: 题型:
菜温度下将氯气通入氢氧化钾溶液里,反应后得到KCI、KClO、KClO3的混合溶液。经测定ClO和ClO3的浓度之比为11:l,则氯气和氢氧化钾溶液反应时,被还原的氯元素和被氯化的氧元素的物质的量之比为 ( )
A.1:3 B.4:3 C.2:l D.3:l
查看答案和解析>>
科目: 来源: 题型:
含有a mol FeBr2的溶液中,通入x mol C12。下列各项为通Cl2过程中,溶液内发生反应的离子方程式,其中不正确的是 ( )
A.x=0.4a,2Fe2++C12=2Fe3++2C1-
B.x=0.6a, 2Br-+Cl2=Br2+2Cl-
C.x=a, 2e2++2Br-+2Cl2=Br2+2Fe3++4Cl-
D.x=1.5a,2Fe2++4Br-+3Cl2=2Br2+2Fe3++6Cl-
查看答案和解析>>
科目: 来源: 题型:
下列有关化学实验的操作或说法中,正确的是(填字母序号) 。
A.过滤、蒸发操作过程中都需要用玻璃棒不断搅拌液体。
B.检验红砖中的氧化铁成分时,向红砖粉末中加入盐酸,放置至充分沉淀后,取上层清液于试管中,滴加KSCN溶液2滴~3滴即可
C.中和滴定实验中,锥形瓶内有少量蒸馏水会造成测定结果偏低。
D.在进行硫酸铜晶体里结晶水含量的测定实验中,称量操作至少要进行4次。
E.制备硫酸亚铁晶体时,向稀硫酸中加入废铁屑至有少量气泡发生时,过滤,然后加热蒸干滤液即可得硫酸亚铁晶体。
F.向2mLl0%NaOH溶液中滴入2%CuSO4溶液的4—6滴,振荡后加入乙醛溶液0.5mL,加热至沸腾,则有红色沉淀出现。
查看答案和解析>>
科目: 来源: 题型:
一定物质的量的SO2与NaOH溶液反应,所得产物中含Na2SO3和NaHSO3物质的量之比为3∶5,则参加反应的SO2与NaOH物质的量之比为? ( )
A.8∶11 B.3∶5 C.1∶2 D.18∶8
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com