
科目: 来源: 题型:
要证明氯乙烷中氯元素的存在可以进行如下操作,其中顺序正确的是
①加入AgNO3溶液 ②加入NaOH溶液
③加热④加蒸馏水 ⑤冷却后加入HNO3后酸化 ⑥加入NaOH的乙醇溶液
A.④③①⑤ B.②③⑤① C.④③① D.⑥③①
查看答案和解析>>
科目: 来源: 题型:
下列有关物质的表达式不正确的是
A.二甲醚的分子式: C2H6O C.葡萄糖的结构简式: CH2OH(CHOH)4CHO
B.醛基的结构简式:—CHO D.溴乙烷的电子式: ![]()
查看答案和解析>>
科目: 来源: 题型:
有关天然产物水解的叙述不正确的是
A.油脂水解可得到丙三醇
B.可用碘检验淀粉水解是否完全
C.蛋白质水解的最终产物均为氨基酸
D.纤维素水解与淀粉水解得到的最终产物不同
查看答案和解析>>
科目: 来源: 题型:
下列各组混合物中,都能用分液漏斗分离的是
A.乙酸乙酯和水 酒精和水、苯酚和水 B.二溴乙烷和水 溴苯和水 硝基苯和水
C.甘油和水 己烷和水 甲酸和水 D.苯和甲苯 乙醛和水 乙酸和乙醇
查看答案和解析>>
科目: 来源: 题型:
由沸点数据:甲烷-146℃,乙烷-89℃,丁烷-0.5℃,戊烷36℃,可以判断丙烷的沸点可能是
A 高于-0.5℃ B 约是+30℃ C 约是-40℃ D 低于-89℃
查看答案和解析>>
科目: 来源: 题型:
在一定温度下将2 mol A和2 mol B两种气体混合于某2L密闭容器中,发生如下反应:3A(g)+B(g) ![]() 2C(g)+2D(g),2 min末反应达到平衡状态,生成了0.8 mol D,请填写下列空白:
2C(g)+2D(g),2 min末反应达到平衡状态,生成了0.8 mol D,请填写下列空白:
(1)2min内B的反应速率为_________________
(2)此温度下该反应的平衡常数K=_________________________
(3)如果缩小反应容器的体积,使压强增大,平衡体系中C的物质的量浓度_____________,C的质量分数___________,容器内气体的平均密度________________,平均相对分子质量________________。(填“增大”、“减小”或“不变”)
(4)如果上述反应在相同条件下从逆反应开始进行,开始加C和D各4/3 mol,要使平衡时各物质的物质的量与原平衡相等,则还应加入__________物质___________mol。
查看答案和解析>>
科目: 来源: 题型:
在一定条件下,CH4和CH3OH的燃烧的热化学方程式分别为:
CH4(g)+2O2(g)=CO2(g) + 2H2O(g) ΔH=-890kJ/mol
CH3OH(g)+1.5O2(g)=CO2(g) + 2H2O(g) ΔH=-750kJ/mol
如果有CH4和CH3OH的混合气体充分燃烧,放出的热量为806kJ,将生成的气体通过浓硫酸,浓硫酸增重36g。则混合气体中CH4和CH3OH的体积比________。
查看答案和解析>>
科目: 来源: 题型:
自然界的矿物、岩石的成因和变化受到许多条件的影响。地壳内每加深1km,压强增大约25000~30000 kPa。在地壳内SiO2 和HF存在以下平衡:SiO2 (s) + 4HF(g) ![]() SiF4 (g) + 2H2O(g)
SiF4 (g) + 2H2O(g)
△H=-148.9 kJ/mol,根据题意完成下列填空:
(1)在地壳深处容易有__________气体逸出,在地壳浅处容易有________沉积
(2)如果上述反应在体积不变的密闭容器中发生,当反应达到平衡时,____________(选填编号)。
a.2v正(HF)=v逆(H2O) b.混合气体的密度保持不变
c.SiO2的质量保持不变 d.反应物不再转化为生成物
(3)如果上述反应的平衡常数K值变大,该反应_________(选填编号)。
a.一定向正反应方向移动 b.在平衡移动时正反应速率先增大后减小
c.一定向逆反应方向移动 d.在平衡移动时逆反应速率先减小后增大
(4)若反应的容器容积为2.0L,反应时间8.0 min,容器内气体的密度增大了0.12g/L,在这段时间内HF的平均反应速率为 __________________________ 。
查看答案和解析>>
科目: 来源: 题型:
科学家利用太阳能分解水生成的氢气在催化剂作用下与二氧化碳反应生成甲醇,并开发出直接以甲醇为燃料的燃料电池。已知H2(g)、CO(g)和CH3OH(l)的燃烧热△H分别为-285.8 kJ·mol-1、-283.0 kJ·mol-1和-726.5 kJ·mol-1。请回答下列问题:
(1)用太阳能分解10mol水消耗的能量是_____________kJ;
(2)甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式为________________________;
 (3)在容积为2 L的密闭容器中,由CO2和H2合成甲醇(CO2+3H2
(3)在容积为2 L的密闭容器中,由CO2和H2合成甲醇(CO2+3H2 ![]() CH3OH + H2O)
CH3OH + H2O)
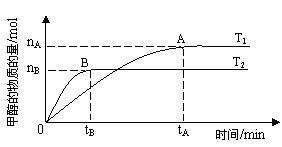
在其他条件不变得情况下,考察温度对反应的影响,实验结果如下图所示(注:T1、T2均大于300℃);下列说法正确的是______(填序号)
①温度为T1时,从反应开始到平衡,
生成甲醇的平均速率为v(CH3OH) =nA/tA mol·L-1·min-1
②该反应在T1时的平衡常数比T2时的小
③该反应为放热反应
④处于A点的反应体系从T1变到T2,
达到平衡时n(H2)/n(CH3OH)增大
(4)在T1温度时,将1mol CO2和3mol H2充入一密闭恒容器中,充分反应达到平衡后,若CO2转化率为a,则容器内的压强与起始压强之比为_________________________。
查看答案和解析>>
科目: 来源: 题型:
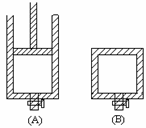 有两只密闭容器A和B,A容器有一个可移动的活塞能使容器内保持恒压,B容器能保持恒容。起始时间这两只容器中分别充入等量的体积比为2∶1的SO2和O2的混合气体,并使A和B容积相等,如右图。在保持400℃的条件下使之发生如下反应:2SO2+O2
有两只密闭容器A和B,A容器有一个可移动的活塞能使容器内保持恒压,B容器能保持恒容。起始时间这两只容器中分别充入等量的体积比为2∶1的SO2和O2的混合气体,并使A和B容积相等,如右图。在保持400℃的条件下使之发生如下反应:2SO2+O2![]() 2SO3。请填写下列空白:
2SO3。请填写下列空白:
(1)达到平衡时所需的时间A容器比B容器 (多、少),A容器中SO2的转化率比B容器中 (大、小)。
(2)达到(1)所述平衡后,若向两容器中通入数量不多的等量的He,
A容器中化学平衡_____________移动(向左、向右、不移动)。
B容器中化学平衡 移动(向左、向右、不移动)。
(3)达到(1)所述平衡后,若向两容器中再通入等量的原反应气体,达到平衡时,A容器中SO3的百分含量 。B容器中SO3的百分含量 。(增大、减小、不变。)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com