
科目: 来源: 题型:
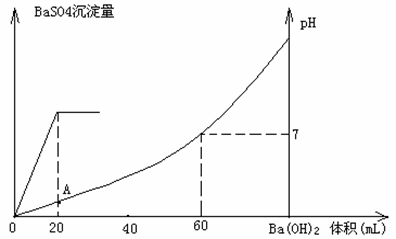
(12分).硫酸和盐酸混合溶液20mL,加入0.05mol/L的Ba(OH)2溶液时,生成BaSO4
沉淀量及溶液pH发生如下图所示的变化。
⑴开始时混合溶液中硫酸和盐酸的物质的量浓度各是多少?
⑵在A点溶液的pH是多少
查看答案和解析>>
科目: 来源: 题型:
(11分)硫酸和盐酸混合溶液20mL,加入0.05mol/L的Ba(OH)2溶液时,生成BaSO4
沉淀量及溶液pH发生如下图所示的变化。
⑴开始时混合溶液中硫酸和盐酸的物质的量浓度各是多少?
 ⑵在A点溶液的pH是多少
⑵在A点溶液的pH是多少
查看答案和解析>>
科目: 来源: 题型:
为了除去MgCl2酸性溶性中的Fe3+,可在加热搅拌的条件下加入一种试剂,过滤后再加入适量盐酸.这种试剂是
A.NH3·H2O B.NaOH C.Na2CO3 D.MgCO3
查看答案和解析>>
科目: 来源: 题型:
某温度时,BaSO4在水中的沉淀溶解平衡曲线如图所示。
下列说法正确的是
A.加入Na2 SO4可以使溶液由a点变到b点
B.通过蒸发可以使溶液由d点变到c点
C.d点无BaSO4沉淀生成
D.a点对应的Ksp大于c点对应的Ksp
查看答案和解析>>
科目: 来源: 题型:
以MnO2为原料制得的MnCl2溶液中常含有少量Cu2+、Pb2+、Cd2+等金属离子,通过添加过量难溶电解质MnS,可使这些金属离子形成硫化物沉淀,经过滤除去包括MnS在内的沉淀,再经蒸发、结晶,可得纯净的MnCl2。根据上述实验事实,可推知MnS具有的相关性质是
A.具有吸附性 B.溶解度与CuS、PbS、CdS等相同
C.溶解度大于CuS、PbS、CdS D.溶解度小于CuS、PbS、CdS
查看答案和解析>>
科目: 来源: 题型:
(10分)工业上通常把溶液中存在的CO32- 和HCO3-的总浓度称为总碱度。水中碱度的控制成为碳酸钠软化水处理法的关键。碳酸在水中一般以3种形态存在,即H2CO3(CO2)、CO32- 和HCO3-。当溶液的pH发生变化时,其中任一种形态的物质的量占三种形态总物质的量的分数δ也可能发生变化,下图是碳酸溶液中碳酸的各种形态的δ随pH的变化曲线。

(1)从图中推断NaHCO3溶液呈 (填“酸”、“碱”、或“中”)性,其原因是
(用离子方程式表示)。
(2)正常情况下,人体血液的pH维持在7.35~7.45之间,则溶于血液中的二氧化碳的主要存在形式是 。(填写微粒化学式)
(3)根据上图,下列叙述中正确的是 。
A.HCO3-既能与强酸反应又能与强碱反应。
 B.盐酸逐滴滴入碳酸钠溶液至恰好完全反应时溶液呈中性
B.盐酸逐滴滴入碳酸钠溶液至恰好完全反应时溶液呈中性
C.pH小于7的雨水称为酸雨
D.在pH为6.37时,溶液中的c (H2CO3)= c (HCO3-)
(4)工业用循环冷却水中常含有Ca2+等杂质离子,在循环过程中易结垢,可通过控制溶液的总碱度使Ca2+等离子形成沉渣除去。已知某温度下Ksp(CaCO3)=3.03×10-9,当水中的c(Ca2+)≤3×10-4 mol·L-1时,不会出现结垢现象,则该水中的c(CO32-)应至少为 mol·L-1。
查看答案和解析>>
科目: 来源: 题型:
下表是五种银盐的溶度积常数(25℃):
| 化学式 | AgCl | Ag2SO4 | Ag2S | AgBr | AgI |
| 溶度积 | 1.8×10-10 | 1.4×10-5 | 6.3×10-50 | 7.7×10-13 | 8.51×10-16 |
下列说法错误的是
A.五种物质在常温下溶解度最大的是Ag2SO4
B.将氯化银溶解于水后,向其中加入Na2S,则可以生成黑色沉淀
C.对于氯化银、溴化银和碘化银三种物质在常温下的溶解度随着氯、溴、碘的顺序增大
D.沉淀溶解平衡的建立是有条件的,外界条件改变时,平衡也会发生移动
查看答案和解析>>
科目: 来源: 题型:
(8分)
某科研小组设计出利用工业废酸(10%H2SO4)来堆浸某废弃的氧化铜锌矿的方案,实现废物综合利用,方案如下图所示。

已知:各离子开始沉淀及完全沉淀时的pH如下表所示。
| 离子 | 开始沉淀时的pH | 完全沉淀时的pH |
| Fe2+ | 6.34 | 9.7 |
| Fe3+ | 1.48 | 3.2 |
| Zn2+ | 6.2 | 8.0 |
请回答下列问题:
⑴氧化铜锌矿中含有少量的CuS和ZnS,在H2SO4的作用下ZnS可以溶解而CuS不溶,则相同温度下:Ksp(CuS) ▲ Ksp(ZnS)(选填“>”“<”或“=”)。
⑵物质A可使用下列物质中的 ▲ 。
A.KMnO4 B.O2 C.H2O2 D.Cl2
⑶除铁过程中加入氨水的目的是调节溶液的pH,pH应控制在 ▲ 范围之间。
⑷物质B可直接用作氮肥,则B的化学式是 ▲ 。
查看答案和解析>>
科目: 来源: 题型:
(8分)水煤气 (主要成分:CO、H2 ) 是重要燃料和化工原料,可用水蒸气通过炽热的炭层制得。
己知:C (s) + H2O(g) ![]() CO (g) +H2 (g);△H =+131.3kJ•mol-1
CO (g) +H2 (g);△H =+131.3kJ•mol-1
C (s) + O2(g)=CO (g); △H = -110.5kJ·mo1-1
CO(g) + O2(g) =CO2 (g);△H =-283.0 kJ·mo1-1
H2 (g) + O2 (g) =H2O (g);△H = -241.8kJ·mo1-1
H2 (g) + O2 (g) =H2O (l); △H = -285.8kJ·mo1-1
⑴将2.4 g 炭转化为水煤气,再完全燃烧,整个过程的△H = kJ·mo1-1。
⑵最近有科学家提出“绿色自由”构想:把空气吹入碳酸钾溶液,然后再把CO2从溶液中
 提取出来,经化学反应后使之变为可再生燃料甲醇。“绿色自由”构想技术流程如下:
提取出来,经化学反应后使之变为可再生燃料甲醇。“绿色自由”构想技术流程如下:
在合成塔中,若有4.4kg CO2与足量H2恰好完全反应,可放出4947kJ的热量,试写出合成塔中发生反应的热化学方程式 。
⑶小亮同学拟用沉淀法测定空气中CO2的体积分数,他查得CaCO3、BaCO3的溶度积(Ksp)分别为4.96×10-9、2.58×10-9。小亮应该选用的试剂是 ,实验时测定的数据除空气的体积外,还需要测定 。
查看答案和解析>>
科目: 来源: 题型:
在溶液中有浓度均为0.01mol·L-1的Fe3+、Cr3+、Zn2+、Mg2+等离子,已知:
Ksp[Fe (OH)3]=2.6×10-39;Ksp[Cr(OH)3]=7.0×10-31
Ksp[Zn(OH)2]=1.0×10-17;Ksp[Mg(OH)2]=1.8×10-11
当氢氧化物开始沉淀时,下列哪一种离子所需溶液的pH最小
A.Fe3+ B.Cr3+ C.Zn2+ D.Mg2+
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com