
科目: 来源: 题型:
某学生的实验报告所列出的下列数据中合理的是
A.用10mL量筒量取7.13mL稀盐酸
B.用托盘天平称量25.20g NaCl
C.用广泛pH试纸测得某溶液的pH为2.3
D.用25mL滴定管做中和滴定时,用去某浓度的碱溶液21.70mL
查看答案和解析>>
科目: 来源: 题型:
25℃时,pH=a的氨水与pH =b的盐酸等体积混合,恰好完全反应,则该氨水的电离度可表示为
A. 10(12-a-b)% B.10(a+b-14)% C. 10(a+b-12)% D.10(14-a-b)%
查看答案和解析>>
科目: 来源: 题型:
下列叙述正确的是
A.95℃纯水的pH<7,说明加热可导致水呈酸性
B.pH=3的醋酸溶液,稀释至10倍后pH=4
C.0.2mol/L的盐酸,与等体积水混合后pH=1(忽略混合前后体积的变化)
D.pH=3的醋酸溶液,与pH=11的氢氧化钠溶液等体积混合后pH=7
查看答案和解析>>
科目: 来源: 题型:
在由水电离产生的H+浓度为1×10-13mol·L-1的溶液中,一定能大量共存的离子组是
① K+、Cl-、NO3-、ClO- ② K+、Al3+、I-、NO3- ③ Na+、Cl-、NO3-、SO42-
④Na+、Ca2+、Cl-、HSO3- ⑤ K+、Ba2+、Cl-、NO3-
A.①③ B.③⑤ C.③④ D.②⑤
查看答案和解析>>
科目: 来源: 题型:
(12分)过氧化氢是重要的氧化剂、还原剂,它的水溶液又称为双氧水,常用作消毒、杀菌、漂白等。某化学兴趣小组取一定量的过氧化氢溶液,准确测定了过氧化氢的含量,并探究了过氧化氢的性质。请填写下列空白:
(1)取10.00 mL密度为dg/mL的过氧化氢溶液,稀释至250 mL后,取出25.00 mL溶液至锥形瓶中,加入稀硫酸酸化,作被测试样。
(2)用高锰酸钾标准溶液滴定被测试样,其反应的离子方程式如下,请将相关物质的化学计量数及化学式填写在横线上。
____MnO4- +____H2O2+____H+![]() ____Mn2++____H2O+___ ______
____Mn2++____H2O+___ ______
(3)滴定时,将高锰酸钾标准溶液注入_______(填“酸式”或“碱式”)滴定管中。滴定到达终点的现象是_____________________________________
(4)重复滴定三次,平均耗用c mol/L KMnO4标准溶液V mL,则原过氧化氢溶液中过氧化氢的质量分数为_____________________。
(5)若滴定前滴定管尖嘴中有气泡,滴定后气泡消失,则测定结果_________(填“偏高”或“偏低”或“不变”)。
查看答案和解析>>
科目: 来源: 题型:
下列实验操作合理的是
A.用25 mL滴定管进行滴定实验时,消耗某溶液体积为21.70 mL
B.在托盘天平的托盘上各垫一张洁净的纸片直接称量NaOH固体
C.用广泛pH试纸测得某溶液的pH为2.3
D.中和滴定实验中的锥形瓶使用前应该用待装液洗涤
查看答案和解析>>
科目: 来源: 题型:
25℃时,在某物质的溶液中,由水电离出的c(H+)=1×10-a mol/L,则下列说法中,正确的是
A.a<7时,水的电离受到抑制 B.a>7时,水的电离受到抑制
C.a<7时,溶液的pH一定为a D.溶液的pH=14-a或pH=网a
查看答案和解析>>
科目: 来源: 题型:
(共9分) ⑴用pH试纸测定溶液的pH,正确操作是: ▲
⑵在25℃条件下将pH=11的氨水稀释100倍后溶液的pH为(填序号) ▲ 。
A.9 B.13 C.11~13之间 D.9~11之间
⑶25℃时,向0.1mol/L的氨水中加入少量氯化铵固体,当固体溶解后,测得溶液pH减小,主要(直接的)原因是(填序号) ▲ 。
A.氨水与氯化铵发生化学反应 B.氯化铵溶液水解显酸性,增加了c(H+)
C.氯化铵溶于水,电离出大量铵离子,抑制了氨水的电离,使c(OH-)减小
查看答案和解析>>
科目: 来源: 题型:
(共16分) ⑴现用物质的量浓度为a mol/L的标准盐酸去测定V mL NaOH溶液的物质的量浓度,请填写下列空白:
① 酸式滴定管用蒸馏水洗净后,还应该进行的操作是___▲___。
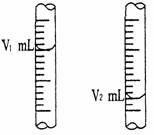 ② 右图是酸式滴定管中液面在滴定前后的读数:
② 右图是酸式滴定管中液面在滴定前后的读数:
试用有关符号表示该待测NaOH溶液的物质的量浓度:c (NaOH) = ___▲___ mol/L。
③ 若在滴定前滴定管尖嘴部分留有气泡,滴定后滴定管尖嘴部分气泡消失,则测定的NaOH物质的量浓度会偏___▲___。
⑵已知空气中含有N2、O2、CO2、H2S等气体。试判断下列滴定操作的终点、分析出现下列现象的原因。(或用有关离子方程式表示)
① 以酚酞为指示剂,碱液滴定酸液,到 ▲ 为终点。30s后导致褪色的原因: ▲ 。
② 以淀粉为指示剂,用Na2S2O3滴定I2(2S2O32—+I2 = S4O62—+2I—)到 ▲ 为终点,约5min后溶液又显色的原因: ▲ 。
查看答案和解析>>
科目: 来源: 题型:
![]() 水的电离过程为H2O
水的电离过程为H2O ![]() ?H++OH-,在不同温度下其平衡常数为K(25℃)=1.0×10-14,K(35℃)=2.1×10-14。则下列叙述正确的是
?H++OH-,在不同温度下其平衡常数为K(25℃)=1.0×10-14,K(35℃)=2.1×10-14。则下列叙述正确的是
A. C(H+)随着温度升高而降低 B.在35℃时,C(H+)>C(OH-)
C.水的电离度?(25℃)>(35℃) D.水的电离是吸热的
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com