
科目: 来源: 题型:
一种“即食即热型”快餐适合外出旅行时使用.它是利用两种物质发生化学反应对食物进行加热,这两种化学物质最适合的选择是
A.浓硫酸与水 B.生石灰与水
C.熟石灰与水 D.氯化钠与水
查看答案和解析>>
科目: 来源: 题型:
关于吸热反应的说法,正确的是
A.凡需要加热的反应一定是吸热反应
B.只有分解反应才是吸热反应
C.使用催化剂的反应是吸热反应
D.若CO2与CaO的化合是放热反应,则CaCO3分解是吸热反应
查看答案和解析>>
科目: 来源: 题型:
已知1g火箭燃料肼(N2H4)气体燃烧生成N2和H2O(g)时,放出16.7kJ的热量,则该反应的热化学方程式正确的是
A.N2H4+O2=N2+2H2O △H = —534.4kJ/mol
B.N2H4(g)+ O2(g)= N2(g)+2H2O(g) △H = —16.7kJ/mol
C.N2H4(g)+O2(g)=N2(g)+2H2O(l) △H = —534.4kJ/mol
D.N2H4(g)+O2(g)=N2(g)+2H2O(g) △H = —534.4kJ/mol
查看答案和解析>>
科目: 来源: 题型:
下列热化学方程式或离子方程式中,正确的是( )
A.甲烷的标准燃烧热为-890.3kJ·mol-1,则甲烷燃烧的热化学方程式可表示为: CH4(g)+2O2(g)=CO2(g)+2H2O(g) △H=-890.3kJ·mol-1
B. 500℃、30MPa下,将0.5mol N2和1.5molH2置于密闭的容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为:N2(g) +3H2 (g) ![]() 2NH3(g) △H=-38.6kJ·mol-1
2NH3(g) △H=-38.6kJ·mol-1
C. 氯化镁溶液与氨水反应:![]()
D. 氧化铝溶于NaOH溶液:Al2O3 + 2OH- == 2AlO2- + H2O
查看答案和解析>>
科目: 来源: 题型:
下列反应既是氧化还原反应,又是吸热反应的是
A.锌粒与稀硫酸的反应 B.甲烷在空气中燃烧的反应
C.Ba(OH)2•8H2O晶体与NH4Cl晶体的反应 D.灼热的木炭与CO2的反应
查看答案和解析>>
科目: 来源: 题型:
关于化学反应与能量的说法正确的是
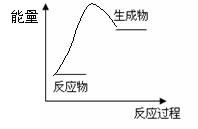
A.根据右图提供的信息,该反应是放热反应
B.化学变化中的能量变化是由化学键变化引起的
C.化学反应中只伴随热量的变化
 D.CaCO3(s)=CaO(s)+CO2(g) ΔH=+178.5 KJ·mol-1 的意义是表示1mol CaCO3完全分解生成1mol CaO和1mol CO2气体要放出178.5 KJ的热量
D.CaCO3(s)=CaO(s)+CO2(g) ΔH=+178.5 KJ·mol-1 的意义是表示1mol CaCO3完全分解生成1mol CaO和1mol CO2气体要放出178.5 KJ的热量
查看答案和解析>>
科目: 来源: 题型:
对于反应中的能量变化,表述正确的是
A.放热反应中,反应物的总能量大于生成物的总能量
B.断开化学键的过程会放出能量
C.加热才能发生的反应一定是吸热反应
D.氧化反应均为吸热反应
查看答案和解析>>
科目: 来源: 题型:
如右图所示,对A生成C的反应,下列所得结论正确的是 ( )
A.该反应为吸热反应
 B.该反应进行时,一定有能量放出
B.该反应进行时,一定有能量放出
C.A物质比C物质稳定
D.该反应肯定很容易,不需要加热就可以进行
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com