
科目: 来源: 题型:
下列反应的离子方程式正确的是 ( )
A.氢氧化铁溶于氢碘酸中:Fe(OH)3 + 3H+ → Fe3+ + 3H2O
B.明矾净水的离子方程式w*w^w.k&s#5@u.c~o*m:Al3+ + 3H2O ![]() Al(OH)3 (胶体) + 3H+
Al(OH)3 (胶体) + 3H+
C.过氧化钠投入重水中:2Na2O2 + 2D2O→4Na+ + O2↑+ 4OD-
D.向氢氧化钡溶液中逐滴加入少量碳酸氢钠溶液:
Ba2++2OH- +2HCO3-→BaCO3↓+2H2O + CO32―
查看答案和解析>>
科目: 来源: 题型:
茶中含有多种有益于人体健康的成分,据测定茶叶中含有450种以上的有机成分与15种以上的元素。某化学研究小组欲探究茶叶中钙元素的含量,设计了探究实验方案如下:(已知茶叶中的铝、铁元素对钙离子的测定有影响)
步骤1:称取500g干燥的茶叶,置于通风橱中,充分灼烧使茶叶灰化,再用研钵磨细后移入烧杯中,然后将200mL 1 mol·L-1盐酸加入灰中搅拌、过滤、洗涤。
步骤2:向步骤1所得滤液中逐滴加入稀氢氧化钠溶液,调节溶液的pH至6~7左右,使铝、铁元素以氢氧化物的形式完全沉淀,再加热煮沸30 min,加入7.95g无水碳酸钠,充分搅拌,待沉淀完全后,过滤,洗涤,过滤后得到滤液和沉淀。
步骤3:将步骤2所得的滤液稀释至500 mL,取其中的20.00 mL溶液以甲基橙作指示剂,用0.100mol·L-1的HCl标准溶液滴定,终点时消耗盐酸的体积为20.00mL,计算结果。
请回答下列问题:
步骤 1中,使茶叶灰化时需要用到三角架、泥三角、酒精喷灯、 ___ 、 ____ 等仪器。
步骤2中,改用试剂 _______ (写试剂名称)来调节pH将更为方便;判断沉淀已经洗净的方法是 。
步骤3中,滴定过程中,眼睛应注视 ______________被滴定的20 mL滤液中含CO32-的物质的量为 __ mol,试计算原500g茶叶中钙离子的质量分数为 _______ .
查看答案和解析>>
科目: 来源: 题型:
(6分)物质A、B、C、D、E、F、G、H、I、J、K有下图转化关系,其中气体D、E为单质,试回答:
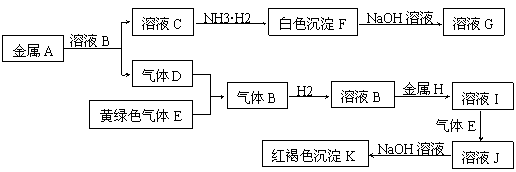
⑴ 组成金属A的元素在周期表的位置是_____________,D的化学式是__________________
⑵ 写出反应“C→F”的离子方程式 ;
⑶ 写出反应“F→G”的化学方程式 ;
⑷ 在溶液I中滴入NaOH溶液,可观察到的现象是 。
查看答案和解析>>
科目: 来源: 题型:
(12分)镁在二氧化碳中能燃烧,钠比镁更活泼,那么钠能在二氧化碳中燃烧吗?某研究性学习小组设计了如下装置进行探究。

(1)写出镁在二氧化碳中燃烧的化学反应方程式 ▲ 。
(2)该装置中饱和碳酸氢钠溶液的作用是 ▲ ,浓硫酸的作用是 ▲ 。
(3)用酒精灯在试管D底部加热,钠在充满二氧化碳气体的试管里剧烈地燃烧,产生大量的白烟。试管底部有黑色物质生成。试管冷却后,试管壁上附着一层白色物质。往试管中加水,白色物质溶解于水,黑色物质不溶。过滤,得到澄清的滤液。往滤液中加澄清石灰水,溶液变浑浊。再滴入稀盐酸,溶液中有气泡出现。则试管壁上附着的白色物质是 ▲ 。将滤纸上的黑色物质移入小试管中,加少量浓硫酸,加热,有刺激性气味的气体生成。则该黑色物质是 ▲ 。试写出钠与二氧化碳反应的化学方程式: ▲ 。
查看答案和解析>>
科目: 来源: 题型:
(10分)已知:![]() H2O2具有较强的氧化性,一些较不活泼金属在稀硫酸存在的情况下,能和H2O2发生氧化还原反应。根据下列框图回答问题:
H2O2具有较强的氧化性,一些较不活泼金属在稀硫酸存在的情况下,能和H2O2发生氧化还原反应。根据下列框图回答问题:
| |

(1)试推断金属M、E分别是(填元素符号): ▲ 、 ▲ 。Z的化学式: ▲ 。
(2)某同学取X的溶液,加入少量稀硫酸酸化后露置于空气中一段时间,颜色变黄,再加入KI、淀粉溶液,又变为蓝色。试判断X、Y中的金属阳离子分别是: ▲ 、 ▲ 。
查看答案和解析>>
科目: 来源: 题型:
(10分)已知:![]() H2O2具有较强的氧化性,一些较不活泼金属在稀硫酸存在的情况下,能和H2O2发生氧化还原反应。根据下列框图回答问题:(M、E等字母用所对应的元素符号表示)
H2O2具有较强的氧化性,一些较不活泼金属在稀硫酸存在的情况下,能和H2O2发生氧化还原反应。根据下列框图回答问题:(M、E等字母用所对应的元素符号表示)

(1)写出M溶于稀H2SO4和H2O2混合液的化学方程式: ▲ 。
(2)某同学取X的溶液,加入少量稀硫酸酸化后露置于空气中一段时间,颜色变黄,再加入KI、淀粉溶液,又变为蓝色。分别写出上述变黄过程和变蓝过程所发生相关反应的离子方程式: ▲ 、 ▲ 。
(3)写出Y到Z变化过程的离子方程式: ▲ 。
(4)写出Cl2将Z氧化为K2EO4的化学方程式: ▲ 。
查看答案和解析>>
科目: 来源: 题型:
 (12分)某同学通过查阅资料得知:铝和氧化铁在高温下反应所得到的熔融物应该是铁铝合金。
(12分)某同学通过查阅资料得知:铝和氧化铁在高温下反应所得到的熔融物应该是铁铝合金。
(1)写出铝和氧化铁在高温下反应的化学方程式: ▲ 。
(2)设计一个最简单的实验方案,证明上述所得的块状熔融物中含有金属铝。写出表示该实验原理的离子方程式: ▲ 。
(3)某同学取一定量上述的熔融物与过量的、且很稀的硝酸充 www..com
分反应,发现反应过程中无气体放出。在反应结束后的溶
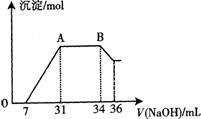
液中,逐滴加入4mo1·L—1的氢氧化钠溶液,所加氢氧化钠溶液的体积(mL)与产生的沉淀的物质的量(mo1)的关系如图所示。在AB段,有刺激性气味的气体产生。试回答下列问题:
①熔融物与稀硝酸充分反应后,还原产物NH4NO3的物质的量为 ▲ mol。
②熔融物中金属铝和金属铁的物质的量的之比为 ▲ 。
查看答案和解析>>
科目: 来源: 题型:
化学与生活密切相关,学好化学有助于提高生活质量。下列关于生活中的一些做法科学的是
A.氢氧化铝可用于治疗胃酸过多
B.废旧电池的回收利用可防止污染环境
C.用米汤检验加碘食盐中的碘酸钾(KIO3)
D.用氢氧化钠的浓溶液洗涤衣服上的油污效果好
查看答案和解析>>
科目: 来源: 题型:
蛇纹石由MgO、A12O3、SiO2、Fe2O3组成。现取一份蛇纹石试样进行实验,首先将其溶于过量的盐酸,过滤后,得到沉淀X和滤液Y。下列叙述正确的是
A.沉淀X的成分是SiO2
B.从蛇纹石组成看,其成分皆是碱性氧化物
C.溶液Y中的阳离子主要是Mg2+、Al3+、Fe3+、H+
D.在溶液Y中加入过量的氨水,过滤得到的沉淀的成分是Fe(OH)3和Mg(OH)2
查看答案和解析>>
科目: 来源: 题型:
(12分)镁能在二氧化碳中燃烧,钠比镁更活泼,那么钠能在二氧化碳中燃烧吗?某研究性学习小组设计了如下装置进行探究。

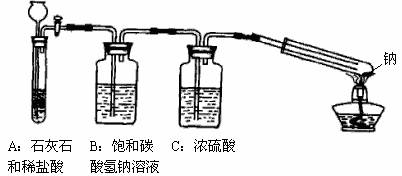
(1)该装置中饱和碳酸氢钠溶液的作用是 ,浓硫酸的作用是
(2)从试剂瓶中取出的金属钠,必须经过必要的操作,方可进行后续的实验,该必要的操作是 ;
(3)放进试管中的金属钠在加热之前,必须进行的操作是
;
(4)用酒精灯在试管底部加热,钠在充满二氧化碳气体的试管里剧烈地燃烧,产生大量的白烟。试管底部有黑色物质生成。试管冷却后,试管壁上附着一层白色物质。往试管中加水,白色物质溶解于水,黑色物质不溶。过滤,得到澄清的滤液。往滤液中加澄清石灰水,溶液变浑浊。再滴入稀盐酸,溶液中有气泡出现,则试管壁上附着的白色物质是 。然后将滤纸上的黑色物质移入小试管中,加少量浓硫酸,加热,有刺激性气味的气体生成。则该黑色物质与浓硫酸共热的化学反应方程式为 。
(5)据(4)中现象,试写出钠与二氧化碳反应的化学方程式:
。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com