
科目: 来源: 题型:
100mL浓度为2mol/L的盐酸跟过量的锌片反应,为加快反应速率,又不影响生成的氢气的总量,可采用的方法是
A.加入适量的6mol/L的盐酸 B.加入数滴氯化铜溶液
C.加入适量蒸馏水 D.加入适量的氯化钠溶液
查看答案和解析>>
科目: 来源: 题型:
据报道,我国拥有完全自主产权的氢氧燃料电池车将在北京奥运会期间为运动员提供腺务。某种氢氧燃料电池的电解液为KOH溶液,下列有关该电池的叙述不正确的是
A.正极反应式为:O2+2H2O+4e-=4OH-
B.工作一段时间后,电解液中KOH的物质的量不变
C.该燃料电池的总反应方程式为:2H2+O2=2H2O
D.用该电池电解CuCl2溶液,产生2.24 L Cl2(标准状况)时,有0.1 mol电子转移
查看答案和解析>>
科目: 来源: 题型:
甲醇-空气燃料电池(DMFC)是一种高效能、轻污染的车载电池,其工作原理如下图。下列有关叙述正确的是
A.H +从正极区通过交换膜移向负极区
B.负极的电极反应式为:CH3OH(l) + H2O(l)-6e-=CO2(g) + 6H +
C.d导出的是CO2
D.图中b、c分别是O2、甲醇

查看答案和解析>>
科目: 来源: 题型:
NaBH4/H2O2燃料电池(DBFC)的结构如下图,有关该电池的说法正确的是
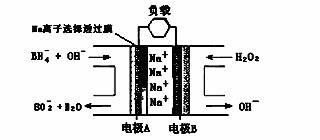
A.电极B是燃料电池的负极
B.电池的电极A反应为:BH4-+8OH--8e-===BO2-+6H2O
C.放电过程中,Na+从正极区向负极区迁移
D.在电池反应中每消耗1 L 6 mol/L H2O2溶液,理论上流过电路中的电子为6NA个
查看答案和解析>>
科目: 来源: 题型:
下列热化学方程式或离子方程式中,正确的是:
A.甲烷的标准燃烧热为-890.3kJ·mol-1,则甲烷燃烧的热化学方程式可表示为:
CH4(g)+2O2(g)=CO2(g)+2H2O(g) △H=-890.3kJ·mol-1
B.500℃、30MPa下,将0.5molN2和1.5mol H2置于密闭容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为:
N2(g)+3H2(g) ![]() 2NH3(g) △H=-38.6kJ·mol-1
2NH3(g) △H=-38.6kJ·mol-1
C.氯化镁溶液与氨水反应:Mg2++2OH-=Mg(OH)2↓
D.氧化铝溶于NaOH溶液:Al2O3+2OH-=2AlO2-+H2O
查看答案和解析>>
科目: 来源: 题型:
甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应原理是:
①CH3OH(g)+H2O(g)=CO2(g)+3H2(g) △H1= + 49.0 kJ·mol -1
②CH3OH(g)+1/2O2(g)=CO2(g)+2H2(g) △H2=-192.9 kJ·mol -1
下列说法正确的是
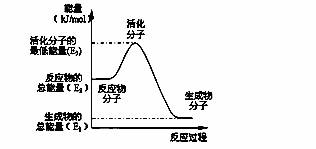
A.反应②中的能量变化如右图所示,则△H2= E1-E3
B.CH3OH的燃烧热△H=-192.9 kJ·mol -1
C.H2燃烧能放出大量的热,故CH3OH转变成H2的过程必须吸收能量
D.根据②推知:在 25℃,101 kPa时,1mol CH3OH(g)燃烧生成CO2和H2O(l)放出的热量应大于192.9 kJ
查看答案和解析>>
科目: 来源: 题型:
X、Y、Z、W、R是5种短周期元素,其原子序数依次增大。X是周期表中原子半径最小的元素,Y原子是外层电子数是次外层电子数的3倍,Z、W、R处于同一周期,R与Y处于同一族,Z、W原子的核外电子数之和与Y、R原子的核外电子数之和相等。下列说法正确的是
A.元素Y、Z、W具有相同电子层结构的离子,其半径依次增大
B.元素X不能与元素Y形成化合物X2Y2
C.元素Y、R分别与元素X形成的化合物的热稳定性:XmY>XmR
D.元素W、R的最高价氧化物的水化物都是强酸
查看答案和解析>>
科目: 来源: 题型:
A、B、C为短周期主族元素,原子序数依次增大,B、C同周期,A与B的最外层电子数之和等于C的质子数,A的最外层电子数是次外层电子数的2倍。下列说法正确的是
A.原子半径大小:A<B<C
B.A、B、C三种元素的非金属性:A>B>C
C.B形成的化合物只能含有共价键
D.A与C所形成的分子可能是非极性分子
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com