
科目: 来源: 题型:
下列各组物质性质的比较中正确的是( )
A 熔点:Na-K合金< Na<氯化钠<金刚石
B 非金属氢化物的稳定性顺序: H2O>H2S>H2Se,HCl<H2S<PH3
C 第一电离能Na<Mg<Al
D 空间利用率:体心立方堆积<六方最密堆积<面心立方最密堆积
查看答案和解析>>
科目: 来源: 题型:
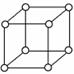
有资料表明,只有钋的晶体中的原子具有如图所示的堆积方式,钋的外围电子排布式是6s26p4。下列关于该元素的说法不正确的是( )
A 右图的堆积方式空间利用率太低,金属极少采取这种堆积方式
B 钋晶体中原子的配位数为6
C 钋基态原子的能层数=周期序数=价电子数
D 钋的常见化合价为+4、+6、-2价
查看答案和解析>>
科目: 来源: 题型:
分别处于元素周期表第2、3周期的主族元素A和B,它们离子的核外电子层相差两层。已知A处于第m族,B处于第n族,且A只有正化合价。则A、B两元素的原子序数分别为( )
A.m、n B.m-2、10-n C.m+2、n+10 D.m+8、n+10
查看答案和解析>>
科目: 来源: 题型:
A、B两主族元素属于同一周期,它们的原子能以共价键结合成化学式为AB2型分子,A、B元素在周期表中的族序数可能为 ( )
A.ⅠA、ⅤA B.ⅢA、ⅦA C.ⅣA、ⅥA D.ⅠA、ⅦA
查看答案和解析>>
科目: 来源: 题型:
NA 表示阿伏加德罗常数的值,下列说法中正确的是( )
A.常温常压下,氧原子总数为0.2NA的SO2和O2的混合气体,其体积为2.24 L
B.0.1mol·L-1的NaHSO4溶液中含有阳离子的物质的量为0.2mol
C.7.8 gNa2S和7.8 gNa2O2中含有的阴离子数目均为0.1 NA
D.l.8 g![]() O2分子与1.8 g
O2分子与1.8 g![]() O3分子中含有的中子数不相同
O3分子中含有的中子数不相同
查看答案和解析>>
科目: 来源: 题型:
下列有关结构和性质的说法中,正确的是 ( )
A.因为酸性:HCl>H2CO3,所以非金属性:Cl>C
B.元素原子的最外层电子数越多,越容易得电子
C.同周期主族元素的原子形成的简单离子电子层结构相同
D.同周期第ⅡA族与第IIIA族的元素原子序数之差不一定为1
查看答案和解析>>
科目: 来源: 题型:
下列说法不正确的是 ( )
A.某微粒空间构型为平面三角形,则中心原子一定是sp2杂化
B.某微粒空间构型为V形,则中心原子一定有孤电子对
C.某微粒空间构型为三角锥形,则该微粒一定是极性分子
D.某微粒空间构型为正四面体,则键角一定是109°28’
查看答案和解析>>
科目: 来源: 题型:
下列关于杂化轨道的叙述中,不正确的是( )
A.分子中中心原子通过sp3杂化轨道成键时,该分子不一定为正四面体结构
B.杂化轨道可用于形成σ键、π键或用于容纳未参与成键的孤电子对
C.杂化前后的轨道数不变,但轨道的形状发生了改变
D.sp3、sp2、sp杂化轨道的夹角分别为109°28′、120°、180°
查看答案和解析>>
科目: 来源: 题型:
下列四种元素中,其单质的氧化性最强的是( )
A.基态原子含有未成对电子最多的第二周期元素
B.某激发态为1s22s12p3的原子
C.基态原子最外层电子排布为2s22p6的元素
D.基态原子最外层电子排布为3s23p5的元素
查看答案和解析>>
科目: 来源: 题型:
下列针对H3O+的说法中正确的是( )
A 中心原子上的孤电子对数为2 B O原子采用sp2杂化, 空间构型为三角锥形
C 离子中存在配位键 D 纯水呈中性, 纯水中不存在H3O+微粒
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com