
1.人们在工作、生活中,为防止事故发生常采用一些安全措施,下列安全措施中正确的是 ( )
A.实验室酒精灯倾倒着火,用湿抹布盖灭 B.冬天用煤取暖时封闭门窗
C.到煤窖中挖煤用火把照明 D.厨房内燃气泄漏打开排气扇电源开关通风
2.不能用排水法收集的气体是( )
A.氢气 B.二氧化碳
C .氮气
D.氧气
.氮气
D.氧气
3.下列现象中能用质量守恒定律解释的是( )
A.化学反应中常伴随热量变化,有的放热,有的吸热
B.100g干冰完全升华成100g二氧化碳气体
C.10gNaCl溶解在90g水中,形成100gNacl溶液
D.一定质量的煤完全燃烧后生成的所有物质的 质量之和大于煤的原质
质量之和大于煤的原质 量
量
4.下列气体等体积混合后,在点燃的条件下不可能发生爆炸的是( )
A.沼气和空气 B.液化石油气和空气 C.天然气和氧气 D.二氧化碳和氧气
5.下列关于燃烧与灭火的说法,正确的是( )
A.放在空气中的木桌椅没有燃烧,是因为木桌椅不是可燃物
B.防止森林大火蔓延,挖开隔离带,是为了将可燃物与火隔离
C.油锅着火,用锅盖盖上,是为了降低可燃物的温度
D.住房失火,消防队员用水扑灭,是为了降低可燃物的着火点
6.古语道:“人要实,火要虚”。此话的意思是说:做人必须脚踏实地,事业才能有成;燃烧固体燃料需要架空,燃烧才能更旺。从燃烧的条件看,“火要虚”的实质是( )
A.增大可燃物的热值 B.增大可燃物与空气的接触面积
 C.提高可燃物的着火点
D.提高空气中氧气的含量
C.提高可燃物的着火点
D.提高空气中氧气的含量
7. 关于化学方程式CH4+2O2
CO2+2H2O的描述正确的是( )
关于化学方程式CH4+2O2
CO2+2H2O的描述正确的是( )
A. 甲烷加氧气在点燃的条件下,反应生成二氧化碳和水
B. 1个甲烷和2个氧气在点燃的条件下,生成1个二氧化碳和2个水
C. 1个甲烷分子和2个氧气分子在点燃的条件下,生成1个二氧化碳分子和2个水分子
D. 1g甲烷和2g氧气在点燃的条件下,生成1g二氧化碳和2g水
8.某化学兴趣小组的同学在老师的指导下,用炉甘石(主要成分是ZnCO3)、赤铜(Cu2O)与木炭粉混合加热到800℃,得到了多种物质。其中不可能得到的物质是 ( )
 A.锌
B.金 C.铜 D.二氧化碳
A.锌
B.金 C.铜 D.二氧化碳
9对于化学反应:4P+5O2 2P2O5 ,下列说法正确的是( )
①参加反应的物质是磷和氧气 ②反应前后分子总数不变
③反应前后元素的种类不变 ④反应前后原子的种类和数目不变
⑤反应前后物质的总质量不变 ⑥反应前后元素的化合价不变
A.①②⑥ B.②③④⑤ C.①②③④⑤ D.①③④⑤
10.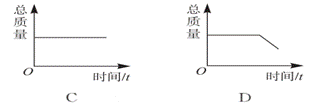 镁带在耐高温的密闭容器中(内含空气)加
镁带在耐高温的密闭容器中(内含空气)加 热发生反应,下列图中能正确表示容器里所盛物质总质量变化的是(
)
热发生反应,下列图中能正确表示容器里所盛物质总质量变化的是(
)

 11.在一密闭容器中加入甲乙丙丁四种物质,在一定条件下发生化学反应,反应前后各种物质的质量变化如图,下列说法正确的是( )
11.在一密闭容器中加入甲乙丙丁四种物质,在一定条件下发生化学反应,反应前后各种物质的质量变化如图,下列说法正确的是( )
A.该化学变化为化合反应
B.丙一定为该反应的催化剂
C.此反应中乙物质和丁物质的质量比为3:2
D.丁的相对分子质量是甲的2倍
12..下列有关物质的用途,既利用物质的物理性质,又利用物质的化学性质的是( )
A.干冰用于人工降雨 B.乙醇用作汽车燃料
C.用酒精降温 D.二氧化碳用于灭火
13.燃烧是人类最早利用的化学反应之一,下列叙述中正确的是 ( )
A.在化学反应中只有燃烧才能放出热量
B.物质与氧气发生的反应都是燃烧
C.煤、石油、天然气燃烧都放出大量的热,都是重要的燃料
D.所有的燃烧 都是化合反应
都是化合反应
14.神州七号飞船成功发射,发射飞船的火箭用偏二甲肼(C2H8N2)和四氧化二氮(N2O4)作常规推进剂,反应的化学方程式为C2H8N2+2N2O4===3X+2CO2+4H2O,则X的化学式为( )
 A.N2
B.H2 C.O2
D.CO
A.N2
B.H2 C.O2
D.CO
15.通常情况下,燃烧需要三个条件,下图所示的实验中,能证明可燃物燃烧与温度有关的是( )

A.②④ B.②③ C.③④ D.①②
16.在“2A+3B===2C+4D”反应中,已知8g物质A完全反应生成11g物质C和9g物质D。若A的相对分子质量为32,则物质B的相对分子质量为( )
A.16 B.32 C.48 D.64
17.(共4分)写出相应的化学符号
钾元素
 硫原子
硫原子  2个镁原子
2个镁原子
煤气中毒的罪魁祸首 (写出物质的化学式)
18. (7分)工业上常用接触法制硫酸(H2SO4),所使用的原料是硫铁矿(主要含FeS)。在高温下,将硫铁矿的粉末与氧气充分反应生成三氧化二铁和二氧化硫,再经过一系列转化可生成硫酸。试配平硫铁矿与氧气反应的化学方程式
(7分)工业上常用接触法制硫酸(H2SO4),所使用的原料是硫铁矿(主要含FeS)。在高温下,将硫铁矿的粉末与氧气充分反应生成三氧化二铁和二氧化硫,再经过一系列转化可生成硫酸。试配平硫铁矿与氧气反应的化学方程式
(
) FeS+ ( ) O2  (
)Fe2O3 + ( ) SO2
(
)Fe2O3 + ( ) SO2
(2)在这个反应中铁由+2价升到+3价,硫元素的化合价由 。
(3)工地施工时,利用乙炔燃烧的火焰焊接钢铁材料。我们可采用碳化钙(CaC2)与水反应制取乙炔(C2H2)气体,同时还有氢氧化钙生成,试写出该反应的化学方程式: 。
19.(共9分)小明同学探究质量守恒定律:他查阅资料,得知①铁和硫酸铜溶液反应生成铜和硫酸亚铁,②碳酸钠和稀盐酸反应生成氯化钠、水和二氧化碳。
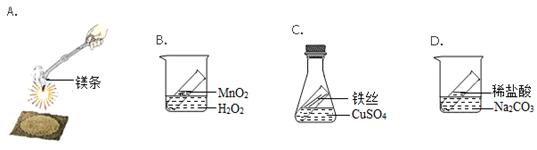
(1)图A中,镁带在空气中燃烧的化学方程式为 ;镁带完全燃烧后,小明称得生成固体的质量大于反应前镁带的质量,请分析造成反应前后固体质量不相等的原因 。
(2)某同学用图B研究质量守恒定律,一段时间后发现指针偏_______(填“左”或“右”),如何改进实验装置________________________________。
(3)写出C装置中发生反应的化学方程式___________________________________________。
(4)根据上述分析, 装置________能用来验证质量守恒定律;装置 能用质量守恒定律来解释。
20. (共7分)在点燃的条件下,A和B反应生成C和D。反应前后分子变化的微观示意图如下:
(共7分)在点燃的条件下,A和B反应生成C和D。反应前后分子变化的微观示意图如下:
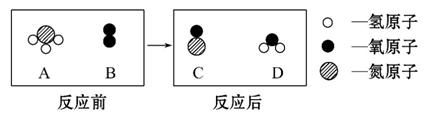
回答下列问题:
(1)从宏观角度看,ABCD四种物质中属于单质的是 .
(2)配平该反应的化学方程式: NH3+ O2=
NO+ H2O ( “1”不能省略不写)
“1”不能省略不写)
(3)参加反应的A、B两物质的质量比为 ;(化简到最简整数比)
(4)该反应说明,在化学反应中不发生变化的微粒是 。
|
|

(1)实验开始前,应该先检查装置A的 。
(2)用装置A来制取CO2 ,所用的药品是 和 (填化学式)。制取的原理是________________________________________。(写化学方程式)
(3)若要用装置B检验CO2 ,在B中盛放的试剂是 。当将标①和②的导管口连接时,B中看到的实验现象是 。该反应的化学方程式为_________
____________________________________。
(4)若用装置C证明CO2能与水反应生成碳酸,C中除有少量的水外,还应该加入的一种试剂是
。当将标①和③的导管口链接时 ,C中看到的实验现象是
。该反应的化学方程式为________________________________。
,C中看到的实验现象是
。该反应的化学方程式为________________________________。
(5)如图所示,烧杯D中放有燃着的蜡烛。当将标①和④的导管口链接时,D中看到的实验现象是 。该实验证明二氧化碳的性质有_____________
____________________________________。
第三题、计算题(共10分)
22.医学上常用过氧化氢溶液(H2O2)来清理伤口和局部抗菌。某同学取该过氧化氢溶液34g放入烧杯中,然后加入0.5g二氧化锰,完全反应后,称得烧杯内剩余物质的总质量为33.7g 。
请回答下列问题
(1)生成的氧气为 g;蒸干烧杯内的液体,所得固体物质质量为 g 。
(2)试通过计算求该过氧化氢溶液中溶质H2O2的质量。(写出规范的计算过程)


邹平双语学校2017—2018第一学期第一次月考
( 四 区) 九 年级 化学(所有班型)试题答题纸
(时间:60分钟,分值:100分)
|
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
|
A |
B |
D |
D |
B |
B |
C |
B |
|
9 |
10 |
11 |
12 |
1 3 3 |
14 |
15 |
16 |
|
D |
C |
C |
D |
C |
A |
A |
B |
二 、填空题(每空1分,化学方程式2分,共42分)
、填空题(每空1分,化学方程式2分,共42分)
17. (共4分) K S
2Mg CO
(共4分) K S
2Mg CO
18.(共7分) (1)( 4) FeS+ (7 ) O2
( 2 )Fe2O3 + ( 4 ) SO2
(1)( 4) FeS+ (7 ) O2
( 2 )Fe2O3 + ( 4 ) SO2
(2) -2价升至+4价
(3) CaC2+2H2O==Ca2H2↑+Ca(OH)2 。
19.(共9分)
(1)
2Mg+O2 2MgO ;
2MgO ;
反应物中有氧气 。
(2)__右_,______改用密闭容器_____。
(3)_____Fe+CuSO4==FeSO4+Cu______________。
(4)_______C____ ;
ABCD 。
;
ABCD 。
20.(共7分)
(1) B .
(2)4 NH3+ 5O2= 4 NO+ 6 H2O (“1”不能省略不写)
(3) 17:40 ;
(4) 原子 。
|
(1) 气密性
。
气密性
。
(2) CaCO3 和 HCl 。___CaCO3+2HCl==CaCl2+H2O+CO2↑_________________________。
(3) 澄清石灰水 。 变浑浊 。
____CO2+Ca(OH)2===CaCO3↓+H2O____。
(4) 紫色石蕊试液 。 变红色 。___CO2+H2O==H2CO3____________。
(5) 蜡烛由低到高依次熄灭 。
二氧化碳密度比空气大,不能燃烧也不支持燃烧___。
22.(1) 0.8 、 0.5 。
(2)1.7