
化学定量实验复习四法
化学定量实验既是中学实验复习的重点,也是高考化学命题的热点。定量实验除了考查实验基本操作外,还可以与化学基本理论有机联系在一起,链接元素化合物知识,考查化学计算。在此以“碳酸钠晶体中结晶水含量的测定”为突破口,进行定量实验的专题复习,以期达到事半功倍的效果。
碳酸钠晶体(Na2CO3?xH2O)中结晶水含量测定的计算依据


定量实验的基本原理是测出某一反应中参加反应的相关两种物质的量,然后根据化学方程式进行计算。因此,设计化学实验方案测定出m(H2O)、m(Na2CO3? xH2O)、m(Na2CO3)、n(H2O)、n(Na2CO3)等相关化学量中的其中两个量,就能计算出w(H2O)、x值。现将复习过程中设计的几种方案推荐给大家。
二、沉淀法
方法:用天平称取Na2CO3?xH2O晶体m1g,在烧杯中加蒸馏水完全溶解,加入CaCl2溶液使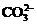 完全沉淀,过滤、洗涤、晾干,称得固体的质量为m2g。
完全沉淀,过滤、洗涤、晾干,称得固体的质量为m2g。
注意(1)如何证明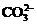 沉淀完全?
沉淀完全?
将反应液静置沉淀后,取少量上层清液,再加入一滴CaCl2溶液看是否有沉淀生成。
(2)怎样洗涤沉淀?如何证明沉淀洗涤干净?
将过滤后的沉淀用蒸馏水在滤纸上轻轻冲洗,收集最后的洗涤液加入AgNO3和稀HNO3看是否有沉淀生成。
(3)列出计算w(H2O)的数学表达式:
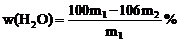
点评 沉淀法是定量实验的重要方法,除了考查相关计算,同时还考查沉淀是否完全、沉淀的洗涤和沉淀是否洗涤干净等实验基本操作。
原理:用酸和碳酸钠晶体反应,收集生成的CO2气体,并测其体积。装置如下图所示。
三、量气法
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com