
2007-2008学年度昌邑第二学期八年级期末考试
化学试卷
(时间90分钟,满分100分)
相对原子质量:H
一、选择题(本题包括20小题,每小题2分,共40分。每小题只有一个答案正确,多选、错选均不得分)
1.“垃圾是放错了位置的资源”,应该分类回收。生活中废弃的铁锅、铝质易拉罐、铜导线等可以归为一类加以回收,它们属于( )
A.纯净物 B.单质 C.金属或合金 D.氧化物
2.收藏家收藏清末铝制品,至今保存十分完好,该艺术品不易锈蚀的主要原因是( )
A.铝不易发生化学反应 B.铝的氧化物容易发生还原反应
C.铝不易氧化 D.铝易氧化,但铝表面的氧化铝具有保护内部的铝的作用
3.下列各组物质中,其成分或主要成分都可以用同一个化学式表示的是( )
A.大理石、方解石、碳酸钙 B.石灰石、生石灰、氧化钙
C.熟石灰、汉白玉、氢氧化钙 D.白垩、草木灰、碳酸钙
4.生活中处处充满化学,以下是日常生活中的一些做法,其中不合理的是( )
A.当发现家中的煤气灶漏气时应关闭进气阀门,开窗通风
B.用金属清洗球擦洗铝壶表面的污物
C.经石灰水浸泡过的鸡蛋能保鲜
D.先用布擦干自行车表面的雨水,再用带油的布擦拭
5.《中学生日常行为规范》中规定,中学生不准吸烟。因为吸烟不仅危害身体健康,而且乱扔烟头容易引起火灾。烟头在火灾中所起的作用是( )
A.提供可燃物 B.提供氧气
C.降低可燃物的着火点 D.使可燃物达到燃烧的温度
6.下列物质不属于合金的是( )
A.生铁 B.不锈钢 C.氧化铁 D.青铜
7.1989年世界卫生组织把铝确定为食品污染源之一应加以控制使用,下列对铝应控制使用的是( )
①制铝合金 ②制电线 ③制餐饮具 ④制银色漆的原料 ⑤制装饮料的易拉罐 ⑥包装糖果和小食品
A.①③④ B.③⑤⑥ C.②⑤⑥ D.全部控制
8.下列各说法正确的是( )
A.在铁板表面镀上一层锌成为白铁,白铁是铁锌合金
B.铁是地壳中含量最多的金属元素
C.炼铁高炉炼出来的是生铁不是钢
D.从高炉排出来的废气,可以直接放到空气中
9.科学合理的使用燃料,可有效地防止环境污染。关于燃料与燃烧的说法错误的是( )
A.在汽油中加入适量的乙醇可减少汽车尾气的污染
B.把煤加工成蜂窝状可使煤的燃烧更加充分
C.天然气是比煤、石油更清洁的化石燃料
D.石油经分馏得到汽油、煤油、柴油等一系列产品是化学变化
10.下列物质中,其中颜色全部是黑色的一组是( )
A.Fe3O4、CuO、MnO2 B.Fe3O4、Cu、CuO
C.Fe2O3 Fe3O4 Fe D.Fe2O3、CuO、C
11.废旧电池的处理问题越来越受到人们的关注,其首要原因是( )
A.防止电池内泄露出来的液体腐蚀其它物品
B.回收电池的石墨电极
C.回收电池的金属外壳再利用
D.防止电池中汞、隔等金属离子对土壤和水造成污染
12.菜刀在下列五种情况下发生锈斑轻重程度顺序是( )
①切湿咸菜后放置 ②切酸菜后放置 ③切完菜后洗净擦干 ④切完菜后洗净擦干再涂上一层豆油 ⑤切完菜后用水冲洗。
A.⑤④③②① B.③②①④⑤ C.②①⑤③④ D.④③⑤①②
13.为了证明鸡蛋壳的成份里含有碳酸钙,笫一步最好先向鸡蛋壳上滴加( )
A.稀硫酸 B.石灰水 C.稀盐酸 D.食盐水
14.据
Fe+2AgNO==2Ag+Fe(NO3)2。该反应属于( )
A.化合反应 B.分解反应 C.置换反应 D.上述反应都不是
15.2008年奥运会“样云”火炬中燃料燃烧后不会对环境造成污染,体现了“绿色奥运”的理念。反应的化学方程式是:CxH8+5O2点燃3CO2+4H2O,其中x的值为( )
A.1 B.
16.当打开一个装有液态空气的容器盖,并将一根燃着的木条置于容器口上方时,观察到的现象是( )
A.熄灭 B.燃烧得更旺 C.先燃烧后熄灭 D.无明显变化
17.某同学对化学反应方程式A2+3B2==
A.C的化学式是AB3
B.若a克A2完全反应生成b克C,则同时消耗(b--a)克B2
C.若m克A2和n克B2恰好完全反应,则生成(m+n)克C
D.若A2和B2的相对分子质量分别为x和y,则C的相对分子质量为(x+y)
18.
A.化石燃料燃烧排放的二氧化硫是导致温室效应的主要物质
B.温室效应是导致地球温度升高的主要原因
C.冰川融化,造成海平面上升,给人类生存带来威胁
D.应减少化石燃料的使用、开发新能源、植树造林等
19.工业生产中常将两种金属放在一个容器中加热使之熔合,冷凝后得到具有金属特性的熔合物――合金,试根据下表所列金属的熔点和沸点的数据(其他条件均已满足),判断不能制得的合金是( )
金属
Na
K
Al
Cu
Fe
熔点(℃)
97.8
63.6
660
1083
1535
沸点(℃)
883
774
220
2595
2750
A.钾―钠合金 B.钾―铁合金 C.钠―铝合金 D.铁―铜合金
20.两份质量相同的碳酸钙,一份与足量的稀盐酸反应,另一份高温煅烧,则所得二氧化碳的质量是( )
A.与盐酸反应产生的多 B.高温分解产生的多 C.一样多 D.无法判断
二、填空及简答题(每空1分,共34分)
21.将下面5个选项分别填在横线上,每项只用一次:
A.缓慢氧化 B.疏松多孔 C.受空气和水共同作用 D.铁器与空气隔绝
E.没有水分存在铁不易生锈
(1)钢铁锈蚀条件_________________; (2)钢铁锈蚀的过程属于_________________
(3)铁锈的状态_________________; (4)使铁器保持干燥的原因是_________________;
(5)铁器表面喷漆的目的是_________________。
22.请运用质量守恒定律的相关知识完成填空。
(1)某物质隔绝空气加强热发生分解反应,生成CuO、H2O、CO2,由此推断该物质中含有_________________元素.
(2)CO2俗称“无形杀手”。用物质x可以测定空气受CO污染的程度,x与CO反应的化学方程式为X+5CO==I2+5CO2。根据生成的CO2的质量可测定CO的质量,请你写出X的化学式_________________。
(3)加热a g高锰酸钾反应一段时间后测得剩余物质的质量为bg。则生成氧气的质量是_________________。
23.人们的日常生活离不开金属,高科技新材料的开发和应用也需要金属。请回答:
(1)地壳中含量最多的金属元素是________________;使用最多的金属是_______________。
(2)根据下图的应用实例,试说出金属具有的两点物理性质:_____________、_____________

24.酒精灯是中学化学实验中最常用的加热仪器,请回答下列与酒精灯有关的问题:
(1)熄灭酒精灯时要用灯帽盖灭.这种灭火方法的主要原理是_________________。
(2)化学实验中,如果不慎碰倒酒精灯,洒出的酒精在桌上燃烧起来,你应采用的灭火方法是_________________。
25.某钢铁厂高炉炼铁的主要反应过程如下:

(1)请在方框内填入相应物质的化学式。
(2)写出步骤②③的化学方程式:②_____________________;③________________________。
(3)冶炼生铁时选择矿石是很重要的,现有赤铁矿(主要成分为Fe2O3)、磁铁矿(主要成分为Fe3O4、黄铁矿(主要成分为FeS2)、菱铁矿(主要成分为FeCO3)。你认为选择矿石的最佳种类是___________;你选择的理由是_________________________________。
26.在一个密闭容器中,有X、Y、Z、Q四种物质在一定条件下充分反应,测得反应前后各物质质量如下表
物质
X
Y
Z
Q
反应前质量/g
31
8
2
5
反应后质量/g
0
待测
42
3
则该密闭容器中发生的化学反应类型为______________________,参加反应的X与Y的质量比为_________________________________。
27.通过化学学习,我们已经认识了很多物质和化学反应。请用化学用语解释下列问题。
(1)常温下,铝在空气中能生成一层致密的氧化铝膜,其反应的化学方程式为_____________。
(2)市场上出售的补血麦片中常含有微量颗粒细小的还原铁粉,铁粉与人体胃液中的盐酸反应转化为亚铁盐,起到补血的作用,写出这个反应的化学方程式___________________。
(3)在古代,人们把在高温下烧红的生铁反复锤打,最终使生铁转化为钢。这也是成语“百炼成钢”又作“千锤百炼”的来历。请你写出上述转变中最关键的一步反应的化学方程式_________________________________。
28.在某些食品的包装袋内,有一个盛有白色颗粒状固体的小纸袋,上面写着“干燥剂,主要成分是生石灰”。生石灰能做干燥剂,其理由是_____________________________________;如果将小纸袋拿出来,放在空气中,经过一段时间后,发现纸袋内的白色颗粒粘在一起成为块状。用化学方程式解释这一现象____________________________________________。
29.有A、B、C、D四种物质,它们分别是四氧化三铁、水、稀硫酸、硫酸铜溶液这四种物质中的一种。另有甲、乙两种气体,它们分别是氧气、氢气这两种气体中的一种,各气体与物质间有如下所示的反应和变化关系:
①铁+甲(气)→B(黑色固体) ②铁+C→硫酸亚铁+乙(气)
③乙(气)+甲(气)→A ④铁+D→硫酸亚铁+红色铜
试推断A、B、C、D和甲、乙各是何物质,写出它们的化学式。
A__________;B__________;C__________;D__________;甲__________;乙__________。
三、实验探究题(每空1分,共18分)
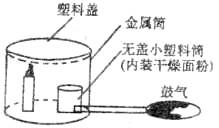
30.面粉加工厂的车间里若悬浮着较多的面粉粉尘,遇明火就有发生爆炸的危险。这是因为面粉粉尘与空气充分接触后,遇到明火急剧燃烧,在短时间内聚积大量的热,使气体的体积在有限的空间内迅速膨胀,从而引起爆炸。下面是模拟粉尘爆炸的一个实验:如下图所示,在无盖小塑料筒里加入干燥面粉,点燃蜡烛,用塑料盖盖住金属筒,迅速鼓入大量空气,不久,便会听到“砰”的一声,爆炸的气浪将塑料筒的塑料盖掀起。试问:
(1)在上述实验中,鼓入空气的作用是______________________________
(2)在下列情况下,不会发生爆炸的是____________________(填序号)。
①金属筒不加盖时 ②蜡烛没有点燃 ③无盖小塑料筒内装的是干燥煤粉
(3)面粉厂为了避免爆炸事故发生,应采取的安全措施是_____________________________ ____________________。(写出一种答案即可)
31.让我们和小亮一起走进化学实验室,共同来学习科学探究的方法。
小亮在实验室用一小块生铁与稀盐酸反应,观察到生铁表面出现____________________,同时发现反应后的液体中有少量黑色不溶物。
提出问题:这种黑色不溶物是什么呢?
猜与假设:这种黑色不溶物中可能含碳。
设计方案:将黑色固体灼烧,如果黑色固体中含有碳,就会有__________气体生成,要想进一步确定这种气体,可以用____________________来检验。
进行实验:小亮按设计方案进行实验,得到了预想的结果。
解释与结论:由此小亮得出结论:
(1)生铁中__________碳(填“含”或“不含”);
(2)碳与稀盐酸_____________反应(填“能”或“不能”),铁与稀盐酸____________反应(填“能”或“不能”)。
32.要除去铜屑中的少量铁屑,某同学设计了以下两个实验方案:

(1)写出两个实验方案中有关反应的化学方程式。
①______________________________;②______________________________。
(2)以上两个实验方案中,你愿意选择的是__________,理由是__________________________ ______________________________。
(3)你是否有更简便的方法?写出你的做法,并和同学们交流。__________________________
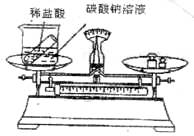
33.有人设计了如下图的实验来验证质量守恒定律:把装有稀盐酸的小试管放入盛有碳酸钠溶液的烧杯中,将烧杯放到托盘天平上,用砝码平衡。取下烧杯并将其倾斜,使两种溶液混合反应,再把烧杯放到天平上,观察天平是否平衡? ______________________________;你认为上述实验设计是否严密? __________;说明理由? ______________________________;应如何改进? ____________________
四、计算题(34小题3分,35小题5分,共8分)
34.将
35.要得到含杂质2%的生铁1000吨,需要含杂质20%的赤铁矿多少吨?
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com