
2008-2009学年度烟台市招远第一学期初四第一学段测评
化学试卷
说明:本试卷满分为100分,其中卷面占5分,时间90分钟。
第Ⅰ卷(选择题部分,共30分)
一、我会选择(本题共10个小题,每小题只有一个选项符合题意。每小题1分,共10分)
1.关于“可燃冰”的叙述正确的是
A.可燃冰是纯净物
B.在通常状况下,天然气和水可以结合成可燃冰
C.因为可燃冰燃烧后几乎不产生任何残渣或废弃物,被科学家誉为“未来能源”
D.可燃冰就是天然气冷却后得到的固体
2.下列说法正确的是
A.一定温度下,同一物质的饱和溶液的质量数一定比其不饱和溶液的大
B.碳酸钠的溶解度为
C.固体物质溶解度随温度的升高而升高
D.在一定温度下,搅拌可以改变硝酸钾的溶解度
3.下列有关物质用途的说法不正确的是
A.食盐是最好的调味品,如果没有盐,许多菜肴将会淡而无味
B.碳酸钠可用于洗涤剂
C.高锰酸钾可用于医药上消毒剂
D.碳酸钡可以用于做胃肠疾病透视用的钡餐
4.除去在氯化钠溶液中混有少量的氯化钙和盐酸,应加入的试剂是
A.石灰石粉末 B.生石灰 C.纯碱溶液 D.石灰水
5.小明写的化学方程式,你认为没有错误的是
A.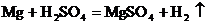 B.
B.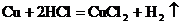
C.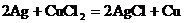 D.
D.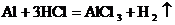
6.有三种金属X、Y、Z,它们之间的反应关系如下:
①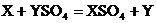 ②
②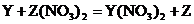
③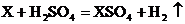 ④Z与硫酸不反应
④Z与硫酸不反应
则有关金属活动性的顺序判断正确的是
A.X>Z>Y B.X>Y>Z C.Y>Z>X D.Y>X>Z
7.钢铁制品在下列那种情况下最易发生腐蚀
A.干燥的空气中 B.潮湿的空气中 C.纯水中 D.食盐水中
8.化学反应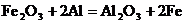 中,还原剂是
中,还原剂是
A.Fe2O3 B.Al C.Al2O3 D.Fe
9.下列生活生产常用的物质中不属于盐的是
A.食醋 B.发酵粉小苏打
C.做洗涤剂用的纯碱 D.做化肥用的碳酸氢铵
10.下列关于海水晒盐原理的分析,正确的是
A.利用阳光照射,使海水升温,从而使食盐结晶析出
B.利用海水在阳光下发生分解反应制得食盐
C.利用海风降温,从而使食盐结晶析出
D.利用阳光和风力使水分蒸发得到食盐
二、我能选择(20分)(本题包括10个小题,每小题1―2个选项符合题意,每小题2分,共20分。多选、错选均不得分,漏选1个扣1分)
11.根据下表中几种固体物质在水中的溶解度,判断下列说法不正确的是
溶解度
NaCl
36
38.4
KNO3
31.6
169
A.
B.
C.可以用冷却热饱和溶液的方法除去硝酸钾中混有的少量氯化钠
D.
12.某同学欲用实验证明铁、铜、汞的化学活动性顺序,他利用了铁片、铜片、硝酸汞溶液和稀盐酸四种物质,设计了下列实验方案,其中可行的是
A.①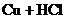 ②
②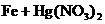 ③
③
B.① ②
②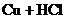 ③
③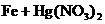
C.① ②
②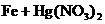 ③
③
D.① ②
②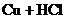 ③
③
13.下图是对实验绘制的相关物质变化图形,其中实验结果与图形对应准确的是
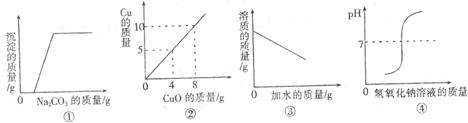
A.图①是向一定量的稀盐酸和氯化钙的混合溶液中不断加入碳酸钠溶液至过量
B.图②是用H2还原CuO来测定CuO中铜元素的含量
C.图③是向饱和的NaCl溶液中不断加水
D.图④是向
14.现欲将粗盐提纯,并用制得的精盐配制一定质量分数的氯化钠溶液。下列说法正确的是
A.粗盐溶解时,可边加粗盐边用玻璃棒搅拌加速溶解
B.蒸发滤液时,待蒸发皿中滤液蒸干时再停止加热
C.配制溶液需要经过计算、称量、溶解、装液等步骤
D.配制溶液时必备的仪器有托盘天平、酒精灯、试管、烧杯、玻璃棒等
15.如下图是A、B两固体物质的溶解度曲线,t
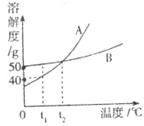
A.t
B.若B物质中混有少量A物质,可用蒸发溶剂的方法提纯B
C.由t
D.由t
16.海水淡化可采用膜分离技术。如下图所示,对淡化膜右侧的海水加压,水分子可以透过淡化膜进入左侧淡水池,而海水中的各种离子不能通过淡化膜,从而得到淡水。对加压后右侧海水成分变化进行分析,正确的是
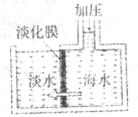
A.溶质质量增加 B.溶剂质量减少
C.溶液质量不变 D.溶质质量分数变大
17.下列鉴别纯碱(碳酸钠)和氯化钠的方法中,可行的是
A.取少量固体分别滴入碳酸钙,观察现象
B.取少量固体分别放入水中,观察是否溶解
C.取少量固体分别放入水中,再分别滴入澄清的石灰水,观察现象
D.取少量固体分别放入水中,再分别滴入氯化钡溶液
18.如下图实验装置所示:盛水的烧杯里放一支试管,试管中盛有石灰水,且底部有少量未溶解的氢氧化钙固体。若向烧杯中加入一块生石灰,下列描述正确的是
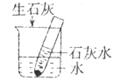
A.生石灰溶于水会放出热量 B.烧杯中所得溶液的溶质为氧化钙
C.试管底部的固体会增多 D.试管中溶液的溶质质量分数不变
19.甲、乙、丙三种物质在不同温度下的溶解度(g)见下表:

0
30
60
90
甲
13.3
45.8
110
202
乙
35.5
36.0
37.1
38.1
丙
0.18
0.16
0.12
0.08
下列有关说法正确的是
A.甲、乙、丙三种物质的溶解度大小顺序是甲>乙>丙
B.
C.升高温度可使丙的饱和溶液变为不饱和溶液
D.使甲物质从一定温度下的饱和溶液中析出,一般采用降温结晶的方法
20.将质量相等的A、B、C三种金属,同时分别放入三份溶质质量分数相同且足量的稀盐酸中,反应生成H2的质量与反应时间的关系如下图所示。根据图中所提供的信息,得出的结论正确的是

A.放出H2的质量是B>A>C B.金属活动性顺序是B>A>C
C.反应速率最快的是A D.反应速率最快的是B
第Ⅱ卷(非选择题部分,共65分)
三、我会填空(34分,每空1分)
21.(3分)广泛应用于火箭、导弹和飞机制造业的金属镁,就是利用从海水中提出的镁盐制取的,请你写出上述转化过程中发生的化学反应方程式(1)____________________;(2)____________________;(3)____________________。
22.(4分)下图为硝酸钾和氯化钠在水中的溶解度曲线。由图可知:

(1)当温度__________时,硝酸钾和氯化钠的溶解度相等。
(2)当温度__________时,氯化钠的溶解度小于硝酸钾的溶解度。
(3)图中P点所表示的硝酸钾溶液是__________(饱和/不饱和)的。
(4)当温度为
23.(5分)粗盐中含有少量泥沙,可通过__________、__________、__________等操作进行初步提纯,这三步操作中均用到一种常见仪器是__________,小丽同学在粗盐的提纯过程中,经过二次过滤,滤液仍然混蚀,其原因可能是____________________,此时采取的补救措施是____________________。
24.(5分)工业上采用氨碱法生产纯碱,其反应的化学反应原理为____________________;____________________。氨盐水比食盐水更容易吸收二氧化碳的原因是_____________ _____________,氨盐水吸收二氧化碳后,首先结晶析出的是__________,该现象说明了________________________________________。
25.(5分)不同的金属有各自的特性,钨常用来制作灯泡中的灯丝,是由于_______________,银常被用做印刷电路是因为____________,金常常用来制成金泊,是因为____________,标志着我国早期青铜铸造工艺的商代司母戊鼎,其制作材料是__________,黄铜的材料是铜锌合金,该合金在性质上与铜或锌在性质上有很大差异,原因是_______________。
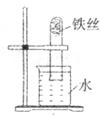
26.(6分)小明把一根用砂纸打磨过的铁丝弯成螺旋状放入试管中,如下图所示实验,放置1―2周后,装置中能出现的现象是:现象1:____________________________;现象2:____________________________。分析产生上述现象的原因:____________________ __________。我们在日常生活中随处可见以上现象的发生,请你任举两例:__________、__________。谈一谈防止该现象发生的措施有哪些?(只填写一种方法)
27.(2分)将质量相等的A、B两块金属,分别放入溶质质量分数相同的足量稀盐酸中,生成氢气的质量(m)与反应时间(t)的关系如下图所示(产物中A、B两种元素的化合价相同)。分析下图,填空(“>”或“<”)
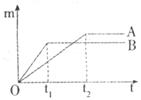
(1)金属活动性A__________B。
(2)相对原子质量A__________B。
28.(4分)每到冬天,市场上便有一种“热宝”出售,它是一个装有化学药品的小袋。使用时,撕去它的保护膜贴在身体上,便会产生热量。已知小袋中装有铁粉、碳粉和少量氯化钠。
(1)取小袋内物质,加入稀盐酸中,发生反应的化学方程式为:____________________。
(2)将袋内物质放在足量O2中燃烧,写出反应的化学方程式:①__________________;②____________________。
(3)将袋内物质加入到一定量的CuSO4溶液中,充分反应过滤,滤液中的溶质一定有__________。(填化学式)
四、我会解释(9分)
29.(7分)实验室用下图的实验装置来探究炼铁反应原理。
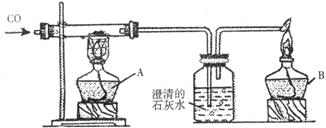
(1)操作步骤如下:①等试管冷却后停止通CO;②待试管内的红色粉末全部变黑后停止加热;③给氧化铁加热;④给试管内通入CO;⑤装入药品并固定试管;⑥检验装置气密性。正确的操作顺序为__________(填序号)
(2)点燃酒精灯时应先点燃________处(填“A”或“B”)的酒精灯,熄灭时________处(填“A”或“B”)酒精灯后熄灭,B处酒精灯的作用____________________。
(3)实验前为什么先通入一氧化碳,后再点燃A处的酒精灯?
(4)实验结束时为什么要等试管冷却后才停止通一氧化碳?
(5)装置的A酒精灯为什么要加烟罩?
30.(2分)金属的应用与它们的化学性质有着密切关系。小敏探究铝、铁、铜的金属活动性质,将铝片和铁片分别插入硫酸铜溶液中,一段时间后取出,铁片上有红色金属析出,铝片上没有明显变化,出现上述现象的原因是什么?
五、我会设计(22分)
31.(10分)粗盐经溶解、过滤、结晶等净化处理后,往往会含有一些可溶性杂质,如氯化镁、氯化钙和硫酸钠,这些杂质若不除,是不能直接用于生活和工业生产的。(请你参与设计方案除去其中的可溶性的杂质)
设计的步骤是:
(1)应先加入稍过量的__________溶液,目的是除去__________离子;
(2)后再加入稍过量的__________溶液,除去__________离子;
(3)再加入稍过量的__________溶液,除去__________离子;
(4)最后加入__________溶液,除去__________离子。
写出第4步发生反应的化学方程式____________________,____________________。
32.(6分)请补充完整金属活动性顺序表:K Ca Na ______ Al Zn Fe Sn Pb(H)Cu _____ Ag Pt Au。某校的当堂作业是:用两种不同的方法,设计实验来验证铁的金属活动性比铜强。写出实验步骤及实验现象,请你帮助完成该题。
方法
实验步骤
实验现象
方法一
方法二
33.(6分)你接触过纯碱吗?小明同学用湿润的手触摸厨房里的纯碱时,有滑腻感;用pH试纸测试纯碱水溶液的酸碱性,发现溶液呈碱性。小明想:纯碱的水溶液呈碱性,这是由钠离子引起的还是由碳酸根离子引起的呢?通过查阅资料
请你运用学过的有关知识和实验方法,设计一个实验方案,证明纯碱水溶液呈碱性是碳酸根离子引起的,而不是钠离子引起的。
供选用的实验用品:试管、胶头滴管;石蕊试液、5%碳酸钠溶液、5%碳酸钾溶液、5%氯化钠溶液。
实验步骤
实验现象
结论
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com