
2007-2008学年度烟台市莱阳第一学期初四期末考试
化学试卷
注意事项:
1.本试题分为选择题和非选择题两部分,满分l00分,考试时间60分钟.
2.请考生将密封线内的项目填写清楚.
3.本卷可能用到的相对原子质量:H:1 O:
一、选择题(下列各小题均有一个正确答案。请选出其序号填在下表的相应答案题栏中。本题包括15小题。每小题2分,共30分。)
1.下列叙述中,正确的是
A.凡是透明的液体均是溶液
B.35gNaCl溶于l
C.降温或蒸发溶剂有晶体析出后的溶液一定是饱和溶液
D.升高饱和溶液的温度,溶液的溶质质量分数一定变大
2.“生活离不开化学,化学来源于生活”。在家庭生活中,欲除去热水瓶胆内壁的水垢,其主要成份为CaCO3和MgCO3所用的方法既科学又经济方便且能除去水垢的是
A.加热至高温分解 B.用稀盐酸冲洗,再用水冲洗
C.用稀硫酸冲洗,再用水冲洗 D.用食醋冲洗,再用水冲洗
3.如图所示是甲、乙、丙三种物质的溶解度曲线,当他们接近饱和时,可以分别通过加溶质、蒸发溶剂、升温等方法变为饱和溶液的是( )
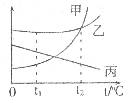
A.甲溶液 B.乙溶液
C.丙溶液 D.甲、乙混合溶液
4.日常生活中常用一些图标来警示或提示人们注意。以下是一些常用危险品标志,则装运乙醇的包装箱应贴的标志是

5.人体中胃酸的主要成分是盐酸,胃酸过多会引起人体不舒的许多症状。所以胃酸过多的病人常用药物治疗,以下物质从理论上讲不能用于治疗胃酸多药物的是
A.NaCl B.Al(OH)
6.人类的第二杀手――心脏血管疾病,给人们的身心健康造成极大的危害。这类疾病患者大多属于酸性体质,应经常食用碱性食品。根据以下表中的信息,这类患者应经常食用的食物为
食物
苹果
葡萄
牛奶
豆制品
pH
2.9~3.3
3.5~4.5
6.3~6.6
7.4~7.9
A.牛奶 B.苹果 C.豆制品 D.葡萄
7.“群众利益无小事,食品安全是太事”,保障食品安全对人体健康非常重要,它引起各级政府有关部门的高度重视。下列不会导致食品对人体健康有害的做法是
A.用干冰储藏易变质的食品
B.用报纸等印刷品直接包裹食品
C.用硫磺熏制辣椒、白木耳等食品
D.用含硝酸钠的工业用盐腌制蔬菜
8.“信息”、“材料”和“能量”被称为新科技革命的三大支柱。下列叙述不正确的是
A.核能、太阳能、氢能等是具有广阔开发前景的新能源
B.制造“神州五号”宇宙飞船,使用了大量新型材料
C.有机高分子材料的广泛应用,“有百利而无一害”
D.人类应与环境和谐相处,要合理开发和利用化石燃料等矿物资源
9.大海是大自然馈赠给人类的天然宝库,可从海水中提取大量的化工原料和其它资源。其中从海水中提炼金属镁需制取较纯净的氯化镁,其过程大致是贝壳(含CaCO3)煅烧后得到生石灰(CaO),将生石灰加到海水(含有MgCl2、MgSO4)池中得到Mg(OH)2沉淀,Mg(OH)2与盐酸反应得到MgCl2溶液。上述生活过程中没有涉及到的反应类型是
A.化合反应 B.分解反应 C.置换反应 D.复分解反应
10.有四瓶失去标签的溶液,它们分别是①Ba(OH)2溶液②K2SO4溶液③KCl溶液④FeCl3溶液,不用其它任何试剂将它们鉴别开来的合理顺序是
A.④①②③ B.②③①④ C.④②①③ D.③②④①
11.一定条件下,对同一反应而言,溶液中溶质的质量分数越大,反应速率越大。现用l
①氢氧化钠 ②水 ③氧化镁 ④硫酸钠溶液
A.只有② B.①③ C.②④ D.②③④
12.将相同质量的Na2CO3、K2CO3、MgCO3、CaCO3四种物质,分别跟足量稀盐酸反应,产生CO2最多的是
A.Na2CO3 B.K2CO
13.在不用指标示剂的条件下,欲将含有盐酸氯化钙溶液变为中性,应该选用的试剂是
A.石灰石粉末 B.生石灰粉末 C.澄清石灰水 D.硝酸银溶液
14.某溶液中存在Mg2+、Ag+、Ba2+三种金属离子,现用NaOH、Na2CO3、NaCl三种稀溶液使它们分别沉淀分离出来。要求每次只加一种溶液滤出一种沉淀,所加溶液顺序正确的是
A.Na2CO3、NaCl、NaOH B.NaOH、NaCl、Na2CO3
C.NaCl、NaOH、Na2CO3 D.NaCl、Na2CO3、NaOH
15.下列从原料到制取较纯的最终产物的实验设计中,理论上正确、操作可行、经济上合理的是
A.Cu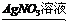 Cu(NO3)2
Cu(NO3)2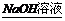 Cu(OH)2
Cu(OH)2
B.Cu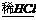 CuCl2溶液
CuCl2溶液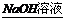 Cu(OH)2
Cu(OH)2
C.Fe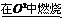 Fe2O3
Fe2O3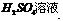 Fe2(SO4)3
Fe2(SO4)3
D.CaCO3
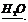 Ca
Ca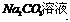 NaOH溶液
NaOH溶液
二、填空题:(本题包括7个小题,共26分。)
16.有碳、氧、钙、氢四种元素,请选用四种元素中的一种或几种,写出符合下列要求的物质的化学式:
(1)从人类的生存环境和新能源开发的前景考虑,比较理想的气体燃料是_______
(2)相对分子质量最小、人类生存所必需的氧化物是_______
(3)常用于某些饮料中,也可作为新型燃料的常温下呈液态的物质是_______
(4)常用作建筑材料,俗称为熟石灰的物质是_______
(5)常用作家庭调味酸的物质是_______
(6)常被人们称为“沼气”或“瓦斯”的主要成分的物质是_______
17.青少年正处在生长发育期,应注意营养均衡,膳食合理。而有些青少年不爱吃蔬菜、水果,影响生长发育,这主要是由于下列物质中的_______ (填序号)不足而引起的。①油脂②蛋白质③维生素
18.向铁粉和铜粉的混合物中加入硝酸银溶液,充分反应后过滤。
(1)若向过滤后的固体中加入稀硫酸,有气体生成,则滤液中的金属阳离子是_______;
(2)若向滤液中加入稀盐酸,有白色沉淀生成,则滤液中的金属阳离子是_______,滤出的固体物质是_______。
19.食品中含有许多有机物,它们为人体提供各种营养成分。根据下列要求回答问题(用物质的名称表示):
(1)人们从水果等食品中摄人的微量有机物是_______;
(2)人们从馒头类食品中主要获取的有机物是_______,它在一定条件下可转化为有甜味的白色粉末状有机物是_______
(3)人体必需的重要营养成分之一,且是构成人体细胞的基础物质是_______;
(4)能为人体储备丰富热能的有机物是_______;
20.环境问题越来越引起全世界的关注和重视,当今人们最关注的三大环境问题分别是_______、_______、_______。
21.人类发明并使用氟利昂(主要用作制冷剂)若干年后,科学家发现氟利昂进入大气层后,在紫外线照射下,分解出氯原子能消耗臭氧,其破坏臭氧层的循环示意图如下:
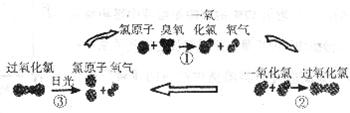
(1)请写出臭氧的化学式______________。
(2)上述三步反应中属于化合反应的是(填序号) ______________。
(3)经过上述①②③的反应过程后,反应物氯原子的个数是否发生变化? _______。
(4)诺贝尔奖获得者
22.甲和乙两种物质的溶解曲线如图所示:

(1)
(2)
(3)当
(4)
三、简答题(本题包括2个小题,共12分。)
23.除去下列物质中的杂质,请把操作方法的序号填写在相应的空格内:
A.加适量的水加热溶解、冷却、过滤 B.加水溶解、过滤、洗涤、干燥
C.加适量盐酸、蒸发结晶 D.加适量水、过滤、蒸发结晶
E.加适量稀盐酸、过滤 F.加适量水溶解、蒸发结晶、趁热过滤
①碳酸钙中混有少量硝酸钾_______;
②氯化钠中混有少量碳酸钠_______;
③白糖中混有少量砂粒_______;
④氯化钠中混有少量的硝酸钾_______;
⑤硝酸钾中混有少量的氯化钠_______;
⑥铜粉中混有铁粉_______。
24.据《家庭医生报》报道,不少市售面粉添加一种叫做“吊白块”的漂白剂,它在加热时分解为甲醛和二氧化硫,这两种物质对人体均有害。甲醛是一种无色刺激性气味的气体,易溶于水,对人体肴中等毒性,长期接触甲醛的人群,口、鼻、喉及肺部肿瘤的发生率会显著增加。
据以上信息回答以下问题:
(1)甲醛的两条物理性质:
(2)甲醛的化学式为CH2O,它属于无机物还是有机物?
(3)推断“吊白块”的组成元素有哪几种?
四、实验探究题(本题包括2个小题,共l6分。)
25.某河流下游的一条内河面上漂浮着大量死鱼,小亮闻讯后,取回水样和同学们一起探究。
(1)观察水质的能见度,然后过滤。过滤时无需用到以下仪器中的_______ (用序号表示)。
A.漏斗 B.烧杯 C.玻璃棒 D.铁架台 E.酒精灯
(2)取过滤后的水样,用两种不同类型的物质来检验该水样是否呈酸性,他们选用的可能是________、________ (要求:两种不同类型的试剂)。
请你任选上述两种物质的一种,设计一个实验进行验证。
实验步骤
实验现象
实验结论
(3)若测得水样呈酸性,向此水样中加入Ba(NO3)2溶液,有白色沉淀生成,则该水样中含有的一种物质可能是________,该反应的化学方程式为________。
26.下图是实验室制取气体的发生装置图,请根据此装置图回答下列问题:
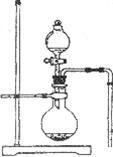
(1)利用图中装置,你能够制备的常见气体有哪几种?
(2)请写出你所能制取气体的相应化学方程式。
(3)说出能用此装置制取上述气体简单理由。
五、计算题。(本题包括2个小题,共16分。)
27.向溶质的质量分数为17%的硝酸银溶液中逐滴滴入稀盐酸,测得滴入稀盐酸的的质量与生成沉淀的质量关系如下图所示,则恰好完全反应时所得溶液中溶质的质量分数为
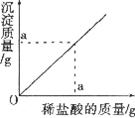
28.某校研究性学习小组在实验室中,要用未知溶质质量分数的硫酸铜溶液测定一种含杂质的铁的纯度。他们的做法是用
(1)参加反应的铁的质量是多少克?
(2)硫酸铜溶液中溶质的质量分数是多少?
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com