
2008-2009学年度德州市夏津初三年级练兵
物理、化学试卷化学部分
可能用到的相对原子质量:H一
第Ⅰ卷
一、在每小题给出的四个选项中,只有一项是符合题目要求的。
13.小刚同学在家所做的下列家庭小实验中,没有发生化学变化的是
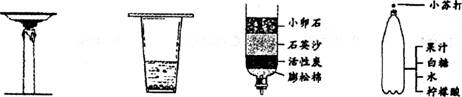
A.用蜡烛制取炭黑B.鸡蛋壳加入食醋中C.用简易净水器净水D.自制汽水
14.二氧化硫是一种易溶于水,密度比空气大的有毒气体,且和水发生反应生成酸,在我国酸雨的类型主要是硫酸型酸雨。下列收集SO2的装置中合理的是
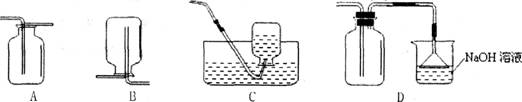
15.某同学郊游时不慎被蜜蜂蜇伤。蜜蜂的刺液是酸性的,该同学随身携带的下列物品可以用来涂抹在蜇伤处以减轻疼痛的是
A.苹果汁(pH约为3) B.肥皂水(pH约为l0)
C.矿泉水(pH约为7) D.牛奶(pH约为6.5)
16.向一无色溶液中滴入数滴无色酚酞试液,溶液变红,说明该溶液一定是
A.酸性溶液 B.酸的水溶液 C.碱性溶液 D.碱的水溶液
17.碱石灰干燥剂是由固体NaOH和CaO组成的混合物,能用它来干燥的气体有
A.O2 B.HCl C.CO2 D.SO2
18.焚烧生活垃圾会产生有毒物质“二恶英”――C12H4O2Cl4,下列有关“二恶英”的叙述不正确的是
A.它是一种有机化合物 B.它的每个分子中有22个原子
C.C、H、O、Cl元素的质量比为6:2:l:2 D.碳元素的质量分数最大
19.将甲、乙两种银白色金属片分别放入硫酸铜溶液中,甲表面析出金属铜,乙没有明显现象。据此判断,三种金属的金属活动性顺序是
A.甲>乙>铜 B.乙>铜>甲 C.铜>甲>乙 D.甲>铜>乙
20.在有机化合物中,有一大类物质的分子组成具有Cm(H2O)n的特征,我们称它为糖类。例如:淀粉(C6H10O5)n是一种糖类,可以把它写成C6n(H2O)5n的形式。下列物质中属于糖类的是
①蔗糖C12H22O11 ②纤维素(C6H10O5)n ③苯酚C6H6O
④葡萄糖C6H12O6 ⑤氨基乙酸C2H5O2N
A.①②④ B.②③④ C.②④⑤ D.④⑤
第Ⅱ卷(非选择题 共34分)
二、填空题(本大题共6小题,共28分)
1.(5分)写出符合下列要求的物质的化学式:①能作为气体燃料单质的是_____________; ②能与HO2反应的氧化物_____:③与血红蛋白结合使人中毒的气体是___________;
④金刚石和石墨的化学式__________;⑤能形成酸雨污染空气的有毒气体是__________,
2.(4分)如图为a、b两物质的溶解度曲线,请依图回答下列问题:
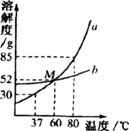
(1)M点的完整含义为_____________,
(2)要想从b物质的溶液中获得较多b晶体,最好用_____________法。
(3)在
3.(4分)小亮在化学晚会上观看了“瓶吞鸡蛋”的魔术(如下图1),看到鸡蛋被吞进瓶内。该反应的化学方程式是__________________________。
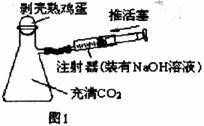
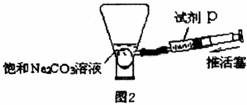
小亮思考:瓶能吞蛋,能不能吐蛋呢?他进行了如右图2的实验,结果鸡蛋吐了出来。他加入的试剂P是_____________,反应的化学方程式是_____________,吐蛋的原因是:__________________________。
4.(7分)下图为实验室制取气体的装置图,回答下列问题:
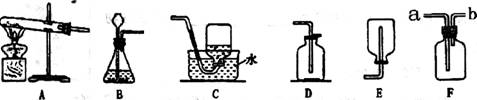
(1)用高锰酸钾制取氧气时选用的发生装置为_____________ (填编号、下同),若要收集较纯净的氧气,应选择_____________.若用F装置收集,则导管应从__________端通入。
(2)利用B图气体发生装置能够制备的常见气体有_____________ (至少填写2种)。
写出制备上述气体的化学方程式: _____________: __ ____。
(3)氨气密度比空气小,且易溶于水,水溶液呈碱性。实验室通常用固体氯化铵与熟石灰混合加热制得,制取氨气时应选择的装置组合是_____________。
5.(5分)二氧化硫的性质与CO2有些相似,能与NaOH溶液反应生成亚硫酸钠和水。某化学兴趣小组的同学,欲利用下图装置和药品制取该气体,并对该气体与水在通常情况下能否发生化学反应进行探究。他们设计的探究过程如下,请你协助他们完成探究实验。
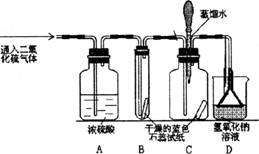
(1)装置B内的石蕊试纸的颜色始终没有变化,这说明__________________________。
(2)装置C中胶头滴管中的蒸馏水在该气体生成之前滴到蓝色石蕊试纸上,未见试纸发生颜色变化。当有该气体通过时,试纸的颜色变红,此现象说明_________________。
(3)装置D的作用是_____________,反应的方程式为__________________________。
(4)结论:二氧化硫与水在通常情况下发生化学反应,生成一种______。(填酸、碱、盐)
6.(3分)某硝酸铵化肥的外包装如下图。请根据包装上的标签计算:

(1)NH4NO3的相对分子质量________________
(2)NH4NO3中各氮氢氧元素的原子个数比_______________
(3)通过计算判断此氮肥样品是_______________ (填纯净物或者混合物)。
三、计算题(6分)
原煤所含硫元素在燃烧过程中产生二氧化硫会造成大气污染。据统计,全世界每年人类活动排放到大气中的二氧化硫超过一亿五千万吨。其中三分之二来自煤炭的燃烧。某煤厂向原煤中加入适量生石灰制成“环保煤”,以减少二氧化硫的排放。削弱二氧化硫对大气的污染。燃烧时吸收二氧化硫的化学方程式是2CaO+2SO2+O2 2CaSO4。该厂现有含硫3.2%的原煤l000吨,问:
2CaSO4。该厂现有含硫3.2%的原煤l000吨,问:
(1)这些原煤中含有硫元素多少吨?
(2)如果这些原煤不经“加工处理”直接燃烧,可生成多少二氧化硫?
(3)如果将这些原煤全部制成“环保煤”,理论上需要含杂质10%的生石灰多少吨?
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com