
科目:czhx 来源: 题型:038
(08哈尔滨)(5分)某同学欲配制溶质质量分数为3%的过氧化氢溶液作为消毒液。现有一瓶标签已破损的过氧化氢溶液,为测定瓶内溶液中溶质的质量分数,取该溶液34g于烧杯中,加入一定量的二氧化锰,完全反应后,称得烧杯内剩余物质的总质量是33.8g,将杯内剩余物质过滤、洗涤、干燥后得滤渣3g。请根据要求回答下列问题:
(1)加入二氧化锰后发生反应的化学方程式为__________________________
(2)生成氧气的质量是 _________________
(3)根据氧气的质量列出求解过氧化氢质量(x)的比例式为_______________
(4)瓶内过氧化氢溶液中溶质的质量分数是 ______________
(5)若取一定量的瓶内溶液配制成溶质质量分数为3%的过氧化氢溶液100g,需加入水的质量是______________

科目:czhx 来源: 题型:
(08哈尔滨)(5分)某同学欲配制溶质质量分数为3%的过氧化氢溶液作为消毒液。现有一瓶标签已破损的过氧化氢溶液,为测定瓶内溶液中溶质的质量分数,取该溶液34g于烧杯中,加入一定量的二氧化锰,完全反应后,称得烧杯内剩余物质的总质量是33.8g,将杯内剩余物质过滤、洗涤、干燥后得滤渣3g。请根据要求回答下列问题:
(1)加入二氧化锰后发生反应的化学方程式为__________________________
(2)生成氧气的质量是 _________________
(3)根据氧气的质量列出求解过氧化氢质量(x)的比例式为_______________
(4)瓶内过氧化氢溶液中溶质的质量分数是 ______________
(5)若取一定量的瓶内溶液配制成溶质质量分数为3%的过氧化氢溶液100g,需加入水的质量是______________

科目:czhx 来源: 题型:
某同学欲配制溶质质量分数为3%的过氧化氢溶液作为消毒液。现有一瓶标签已破损的过氧化氢溶液,为测定瓶内溶液中溶质的质量分数,取该溶液34g于烧杯中,加入一定量的二氧化锰,完全反应后,称得烧杯内剩余物质的总质量是33.8g,将杯内剩余物质过滤、洗涤、干燥后得滤渣3g。请根据要求回答下列问题:
(1)加入二氧化锰后发生反应的化学方程式为__________________________
(2)生成氧气的质量是 _________________
(3)根据氧气的质量列出求解过氧化氢质量(x)的比例式为_______________
(4)瓶内过氧化氢溶液中溶质的质量分数是 ______________
(5)若取一定量的瓶内溶液配制成溶质质量分数为3%的过氧化氢溶液100g,需加入水的质量是 ______________

科目:czhx 来源: 题型:038
某同学欲配制溶质质量分数为3%的过氧化氢溶液作为消毒液。现有一瓶标签已破损的过氧化氢溶液,为测定瓶内溶液中溶质的质量分数,取该溶液34g于烧杯中,加入一定量的二氧化锰,完全反应后,称得烧杯内剩余物质的总质量是33.8g,将杯内剩余物质过滤、洗涤、干燥后得滤渣3g。请根据要求回答下列问题:
(1)加入二氧化锰后发生反应的化学方程式为__________________________
(2)生成氧气的质量是 _________________
(3)根据氧气的质量列出求解过氧化氢质量(x)的比例式为_______________
(4)瓶内过氧化氢溶液中溶质的质量分数是 ______________
(5)若取一定量的瓶内溶液配制成溶质质量分数为3%的过氧化氢溶液100g,需加入水的质量是 ______________

科目:czhx 来源: 题型:038
某同学欲配制溶质质量分数为3%的过氧化氢溶液作为消毒液。现有一瓶标签已破损的过氧化氢溶液,为测定瓶内溶液中溶质的质量分数,取该溶液34g于烧杯中,加入一定量的二氧化锰,完全反应后,称得烧杯内剩余物质的总质量是33.8g,将杯内剩余物质过滤、洗涤、干燥后得滤渣3g。请根据要求回答下列问题:

(1)加入二氧化锰后发生反应的化学方程式为________________
(2)生成氧气的质量是 _________________
(3)根据氧气的质量列出求解过氧化氢质量(x)的比例式_____________
(4)瓶内过氧化氢溶液中溶质的质量分数是 ______________
(5)若取一定量的瓶内溶液配制成溶质质量分数为3%的过氧化氢溶液100g,需加 入水的质量是 ______________
科目:czhx 来源: 题型:
某同学欲配制溶质质量分数为3%的过氧化氢溶液作为消毒液。现有一瓶标签已破损的过氧化氢溶液,为测定瓶内溶液中溶质的质量分数,取该溶液34g于烧杯中,加入一定量的二氧化锰,完全反应后,称得烧杯内剩余物质的总质量是33.8g,将杯内剩余物质过滤、洗涤、干燥后得滤渣3g。请根据要求回答下列问题:

(1)加入二氧化锰后发生反应的化学方程式为__________________________
(2)生成氧气的质量是 _________________
(3)根据氧气的质量列出求解过氧化氢质量(x)的比例式为_______________
(4)瓶内过氧化氢溶液中溶质的质量分数是 ______________
(5)若取一定量的瓶内溶液配制成溶质质量分数为3%的过氧化氢溶液100g,需加入水的质量是 ______________
科目:czhx 来源: 题型:
科目:czhx 来源: 题型:
| A、5.1% | B、5.4% | C、4.8% | D、5.0% |
科目:czhx 来源:新课程同步练习 化学 九年级下册 题型:013
某同学欲配制溶质质量分数为8%的食盐溶液80 g,在用托盘天平称量食盐时,他把食盐和砝码的位置放颠倒了(1 g以下用游码),那么实际上他所配制的食盐溶液的溶质质量分数为
A.>8%
B.<8%
C.=8%
D.无法确定
科目:czhx 来源:不详 题型:问答题
科目:czhx 来源:同步题 题型:计算题

科目:czhx 来源:2008-2009学年山东省莱芜市莱城区八年级(上)期末化学试卷(解析版) 题型:解答题
科目:czhx 来源:2008年黑龙江省哈尔滨市初中毕业升学统一考试、化学试卷 题型:038
某同学欲配制溶质质量分数为3%的过氧化氢溶液作为消毒液.现有一瓶标签已破损的过氧化氢溶液,为测定瓶内溶液中溶质的质量分数,取该溶液34 g于烧杯中,加入一定量的二氧化锰,完全反应后,称得烧杯内剩余物质的总质量是33.8 g,将杯内剩余物质过滤、洗涤、干燥后得滤渣3 g请根据要求回答下列问题:

(1)加入二氧化锰后发生反应的化学方程式为________
(2)生成氧气的质量是________
(3)根据氧气的质量列出求解过氧化氢质量(x)的比例式为________
(4)瓶内过氧化氢溶液中溶质的质量分数是________
(5)若取一定量的瓶内溶液配制成溶质质量分数为3%的过氧化氢溶液100 g,需加入水的质量是________
科目:czhx 来源:2010年山东省济宁市曲阜师大附中九年级化学质量检查试卷(解析版) 题型:选择题
科目:czhx 来源: 题型:单选题
科目:czhx 来源: 题型:填空题
科目:czhx 来源: 题型:单选题
科目:czhx 来源:2013年江苏省南京市鼓楼区中考二模化学试卷(带解析) 题型:填空题
某化学兴趣小组的同学在实验室配制质量分数为8%的氢氧化钠溶液,并用其证明与某盐酸发生了中和反应。
(1)配制100g质量分数为8%的氢氧化钠溶液。
①计算:需要氢氧化钠固体的质量为 g,水的体积为 mL(水的密度近似看作1g/cm3)。
②称量:调节托盘天平平衡,将一个烧杯放在托盘天平的 盘,称量其质量。然后按需要添加砝码、移动游码,再将氢氧化钠固体加入烧杯中,直至天平平衡。该步骤中用烧杯而不用纸称量氢氧化钠的原因是 。
③溶解:用量筒量取所需的水,倒入盛有氢氧化钠固体的烧杯里,搅拌,使其溶解,并冷却至室温。
④把配好的溶液装入试剂瓶,塞好橡皮塞并贴上标签。
(2)某兴趣小组同学为证明NaOH溶液与稀盐酸发生了中和反应,从不同角度设计了如下实验方案,并进行实验。
【实验方案】
方案一:先用pH试纸测定NaOH溶液的pH,再滴加盐酸,并不断振荡溶液,同时测定混合溶液的pH,如果测得的pH逐渐变小且最终小至小于7,则证明NaOH溶液与稀盐酸发生了化学反应。
①用pH试纸测定NaOH溶液pH时,正确的操作是: 。
②简述强调“测得的pH小于7”的理由: 。
方案二:化学反应中通常伴随有能量的变化,可借助反应前后的温度变化来判断反应的发生。如果NaOH溶液与稀盐酸混合前后温度有变化,则证明发生了化学反应。该组同学在没使用温度计的情况下,通过下图所示装置完成了实验。则该组同学根据 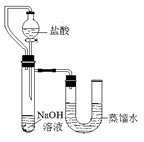
科目:czhx 来源:2013年江苏省南京市鼓楼区中考二模化学试卷(解析版) 题型:填空题
某化学兴趣小组的同学在实验室配制质量分数为8%的氢氧化钠溶液,并用其证明与某盐酸发生了中和反应。
(1)配制100g质量分数为8%的氢氧化钠溶液。
①计算:需要氢氧化钠固体的质量为 g,水的体积为 mL(水的密度近似看作1g/cm3)。
②称量:调节托盘天平平衡,将一个烧杯放在托盘天平的 盘,称量其质量。然后按需要添加砝码、移动游码,再将氢氧化钠固体加入烧杯中,直至天平平衡。该步骤中用烧杯而不用纸称量氢氧化钠的原因是 。
③溶解:用量筒量取所需的水,倒入盛有氢氧化钠固体的烧杯里,搅拌,使其溶解,并冷却至室温。
④把配好的溶液装入试剂瓶,塞好橡皮塞并贴上标签。
(2)某兴趣小组同学为证明NaOH溶液与稀盐酸发生了中和反应,从不同角度设计了如下实验方案,并进行实验。
【实验方案】
方案一:先用pH试纸测定NaOH溶液的pH,再滴加盐酸,并不断振荡溶液,同时测定混合溶液的pH,如果测得的pH逐渐变小且最终小至小于7,则证明NaOH溶液与稀盐酸发生了化学反应。
①用pH试纸测定NaOH溶液pH时,正确的操作是: 。
②简述强调“测得的pH小于7”的理由: 。
方案二:化学反应中通常伴随有能量的变化,可借助反应前后的温度变化来判断反应的发生。如果NaOH溶液与稀盐酸混合前后温度有变化,则证明发生了化学反应。该组同学在没使用温度计的情况下,通过下图所示装置完成了实验。则该组同学根据
