
科目:gzhx 来源: 题型:阅读理解

| 11m-3b |
| 11m |
| 11m-3b |
| 11m |
m-
| ||
| m |
m-
| ||
| m |
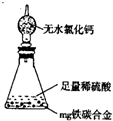
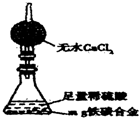 (5)经过大家的讨论,决定采用下图装置(干燥管中试剂为无水氯化钙,锥形瓶中为mg铁炭合金和足量稀硫酸.)和其他常用实验仪器测定某些数据即可.为了快速测算出铁的质量分数,最简便的实验操作是
(5)经过大家的讨论,决定采用下图装置(干燥管中试剂为无水氯化钙,锥形瓶中为mg铁炭合金和足量稀硫酸.)和其他常用实验仪器测定某些数据即可.为了快速测算出铁的质量分数,最简便的实验操作是科目:gzhx 来源: 题型:
科目:gzhx 来源: 题型:
科目:gzhx 来源: 题型:阅读理解
| ||
| ||
| ||
| ||
| 11m-3b |
| 11m |
| 11m-3b |
| 11m |
科目:gzhx 来源: 题型:
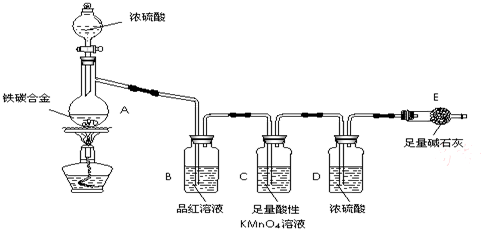
科目:gzhx 来源: 题型:阅读理解
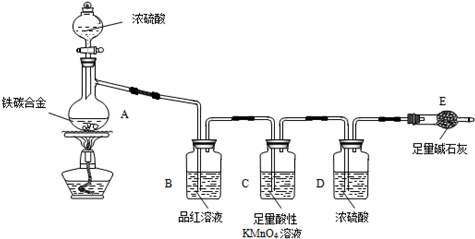
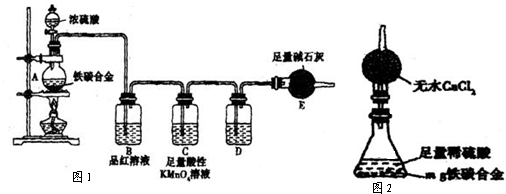
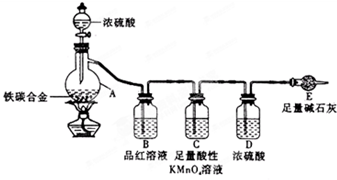 某化学兴趣小组为了测定某铁碳合金中铁的质量分数,并探究浓硫酸的某些性质,设计了如图所示的实验装置和实验方案(夹持仪器已省略),请据此项回答相应问题.
某化学兴趣小组为了测定某铁碳合金中铁的质量分数,并探究浓硫酸的某些性质,设计了如图所示的实验装置和实验方案(夹持仪器已省略),请据此项回答相应问题.| △ |
| ||
| ||
| 3b |
| 11a |
| 3b |
| 11a |
科目:gzhx 来源: 题型:
| 实验步骤 | 向3-4mL 1mol/L的CaCl2溶液中滴入1mol/L的Na2SO4溶液至反应完全 |
| 实验现象 | 产生白色沉淀 |
| 离子方程式 | (1)Ca2++SO42-=CaSO4↓ (1)Ca2++SO42-=CaSO4↓ |
| 小组讨论交流 | 向上述反应后的清液中滴入适量1mol/L的Na2CO3 溶液会出现什么现象 |
| 假设出现的实验现象,说明理由 | 假设:Ⅰ无现象 理由:反应没有限度,Ca2+沉淀完全 假设:Ⅱ (2)产生白色沉淀 (2)产生白色沉淀 ,理由:反应存在限度,溶液中尚有较多Ca2+ 反应存在限度,溶液中尚有较多Ca2+ |
| 证明你的假设 | 现象:产生大量的白色沉淀 |
| 离子方程式 | (3)Ca2++CO32-=CaCO3↓ (3)Ca2++CO32-=CaCO3↓ |
| 解释 | (4)加入CO32-产生了大量的白色沉淀,说明Ca2++SO42-  CaSO4↓反应是可逆反应,存在反应限度,所以Ca2+不能反应完,才出现这种现象 CaSO4↓反应是可逆反应,存在反应限度,所以Ca2+不能反应完,才出现这种现象(4)加入CO32-产生了大量的白色沉淀,说明Ca2++SO42-  CaSO4↓反应是可逆反应,存在反应限度,所以Ca2+不能反应完,才出现这种现象 CaSO4↓反应是可逆反应,存在反应限度,所以Ca2+不能反应完,才出现这种现象 |
科目:gzhx 来源: 题型:阅读理解
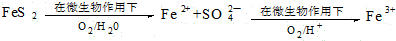
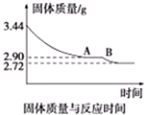
科目:gzhx 来源: 题型:
科目:gzhx 来源: 题型:
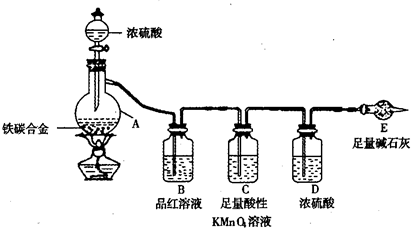
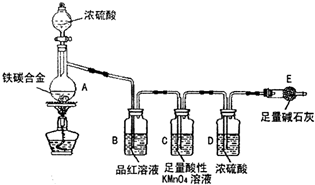 某化学兴趣小组为了测定某铁碳合金(看成铁和碳两种单质的混合物)中铁的质量分数,并探究浓硫酸的某些性质,设计了如图所示的装置(夹持仪器已省略)和方案进行实验.
某化学兴趣小组为了测定某铁碳合金(看成铁和碳两种单质的混合物)中铁的质量分数,并探究浓硫酸的某些性质,设计了如图所示的装置(夹持仪器已省略)和方案进行实验.科目:gzhx 来源: 题型:
(9分)某化学课外小组为了探究CaCl2溶液和Na2SO4溶液反应有没有限度,设计了如下活动过程,请完成表中空格:(已知CaSO4在水中微溶,CaCO3在水中难溶)
| 实验步骤 | 向3—4 mL 1 mol/L的CaCl2溶液中滴入1mol/L的Na2SO4溶液至反应完全 |
| 实验现象 | 产生白色沉淀 |
| 离子方程式 | (1) |
| 小组讨论交流 | 向上述反应后的清液中滴入适量1mol/L的Na2CO3 溶液会出现什么现象 |
| 假设出现的实验现象,说明理由 | 假设:Ⅰ 无现象 理由:反应没有限度,Ca2+沉淀完全 假设:Ⅱ(2) ,理由:(3) |
| 证明你的假设 | 现象:产生大量的白色沉淀 |
| 离子方程式 | (4) |
| 解释出现假设Ⅱ现象的原因 | (5) |
科目:gzhx 来源:2011-2012学年甘肃省张掖二中高一下学期期中考试化学试卷 (带解析) 题型:实验题
某化学课外小组为了探究CaCl2溶液和Na2SO4溶液反应有没有限度,设计了如下活动过程,请完成表中空格:(已知CaSO4在水中微溶,CaCO3在水中难溶)
| 实验步骤 | 向3—4 mL 1 mol/L的CaCl2溶液中滴入1mol/L的Na2SO4溶液至反应完全。 |
| 实验现象 | 产生白色沉淀 |
| 离子方程式 | (1) |
| 小组讨论交流 | 向上述反应后的清液中滴入适量1mol/L的Na2CO3溶液会出现什么现象 |
| 假设出现的实验现象,说明理由 | 假设Ⅰ: 无现象; 理由:反应没有限度,Ca2+沉淀完全 假设Ⅱ:(2) ,理由:(3) |
| 证明你的假设 | 现象:产生大量的白色沉淀 |
| 离子方程式 | (4) |
| 实验结论 | (5) |
科目:gzhx 来源:2013届湖北省荆州中学高三第二次质量检测化学试卷(带解析) 题型:实验题
(10分)现有ag铁碳合金,某化学兴趣小组为了测定铁碳合金中铁的质量分数,设计了下图所示的实验装置和实验方案(夹持仪器已省略),请回答相应问题。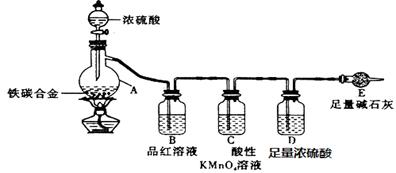
(1)未点燃酒精灯前,A、B均无明显现象,其原因是:____ _。
(2)点燃酒精灯一段时间后,A、B中可观察到明显的现象。写出碳与浓硫酸加热反应的化学方程式_____________________________________。
(3)待A中不再逸出气体时停止加热,拆下E并称重。E增重b g。铁碳合金中铁的质量分数为_____________________(写表达式)。能用该方法测定的前提现象是 。
(4)某同学认为上述方法较复杂,使用下图所示的装置和其它常用实验仪器测定某些数据即可。为了快速和准确的计算出铁的质量分数,最简便的实验操作是_______(填写代号)。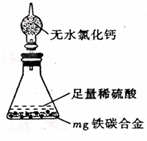
A.用排水法测定H2的体积
B.反应结束后,过滤、洗涤、干燥、称量残渣的质量
C.测定反应前后装置和药品的总质量。
科目:gzhx 来源: 题型:
现有某铁碳合金,某化学兴趣小组为了测定铁碳合金中铁的质量分数,并探究浓硫酸的某些性质,设计了下图所示的实验装置和实验方案(夹持仪器已省略),请你参与此项活动并回答相应问题。(由实验装置引起的实验误差忽略不计)。
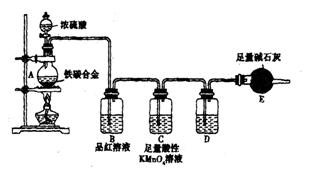
Ⅰ.探究浓硫酸的某些性质
(1)称量E的质量;按照图示连续装置,检查装置的气密性。
(2)将mg铁碳合金样品放入A中,再加入适量的浓硫酸。未点燃酒精灯前,A、B均无明显现象,其原因是: 。点燃酒精灯一段时间后,B中可观察到的明显现象是 。
C中足量的酸性KMnO4溶液所起的作用是 。D中盛放的试剂是 。
(3)反应一段时间后,从A中逸出气体的速率仍然较快,除因反应温度较高外,还可能的原因是 。
Ⅱ.测定铁的质量分数
(4)待A中不再逸出气体时,停止加热,拆下E并称重,E增重bg,则铁碳合金中铁的质量分数为 (写表达式)。某同学认为:依据此实验测得的数据,计算合金中铁的质量分数可能会偏低,你认为可能的原因是 。
(5)经过大家的讨论,决定采用右图装置和其他常用实验仪器测定某些数据即可,为了快速和准确地计算出铁的质量分数,最简便的实验操作是 (填写代号)。
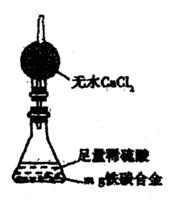
①用排水法测定H2的体积
②反应结束后,过滤、洗涤、干燥、称量残渣的质量
③测定反应前后装置和药品的总质量
科目:gzhx 来源:2011-2012年度上海市吴淞中学高二第一学期期末考试化学试卷 题型:实验题
某化学兴趣小组为了测定某铁碳合金中铁的质量分数,并探究浓硫酸的某些性质,设计了下图所示的实验装置和实验方案(夹持仪器已省略),请据此项回答相应问题。
Ⅰ探究浓硫酸的某些性质
(1)按图示连接装置,检查装置的气密性,称量E的质量。
(2)将a g铁碳合金样品放入A中,再加入适量的浓硫酸。仪器A的名称为____________,
未点燃酒精灯前,A、B均无明显现象,其原因是:____ ___。
(3)点燃酒精灯一段时间后,A、B中可观察到明显现象。
A中开始发生反应的化学方程式为:2Fe +6H2SO4 Fe2(SO4)3 + 3SO2↑ +6H2O
Fe2(SO4)3 + 3SO2↑ +6H2O
和______________________________________ (写化学方程式)。
B中的现象是_________,由此可得到浓硫酸具有_______性,C装置的作用 。
(4)随着反应的进行,A中还可能发生某些离子反应。写出相应的离子方程式__ __。
(5)反应一段时间后,从A中逸出气体的速率仍然较快,除因温度较高,反应放热外,还可能的原因是_____________________________________。
Ⅱ测定铁的质量分数
(6)待A中不再逸出气体时,停止加热,拆下E并称重。E增重b g。
铁碳合金中铁的质量分数为_____________________(写表达式),为使实验数据更为精确,可在装有碱石灰的干燥管后加入________________________________。
科目:gzhx 来源: 题型:
(18分)现有某铁碳合金,某化学兴趣小组为了测定铁碳合金中铁的质量分数,并探究浓硫酸的某些性质,设计了下图所示的实验装置和实验方案(夹持仪器已省略),请你参与此项活动并回答相应问题。
Ⅰ 探究浓硫酸的某些性质
(1)按图示的连接装置,检查装置的气密性,称量E的质量。
(2)将a g铁碳合金样品放入A中,再加入适量的浓硫酸。仪器A的名称为________。
未点燃酒精灯前,A、B均无明显现象,其原因是:____ 。
(3)点燃酒精灯一段时间后,A、B中可观察到明显的现象。
写出A中发生反应的化学方程式___________________________(只写一个)。
B中的现象是______________,由此可得到浓硫酸具有____________性。
(4)随着反应的进行,A中还可能发生某些离子反应。写出相应的离子方程式________________________________(只写一个)。
(5)反应一段时间后,从A中逸出气体的速率仍然较快,除因温度较高,反应放热外,还可能的原因是_____________________________________。
Ⅱ 测定铁的质量分数
(6)待A中不再逸出气体时,停止加热,拆下E并称重。E增重b g。
铁碳合金中铁的质量分数为_____________________(写表达式)。
(7)某同学认为上述方法较复杂,使用下图所示的装置和其它常用实验仪器测定某些数据即可。为了快速和准确的计算出铁的质量分数,最简便的实验操作是_________________(填写代号)。
A.用排水法测定H2的体积
B.反应结束后,过滤、洗涤、干燥、称量残渣的质量
C.测定反应前后装置和药品的总质量
科目:gzhx 来源:2010-2011学年山东省高三上学期期末复习(二)(理综)化学部分 题型:填空题
现有某铁碳合金,某化学兴趣小组为了测定铁碳合金中铁的质量分数,并探究浓硫酸的某些性质,设计了下图所示的实验装置和实验方案(夹持仪器已省略),请你参与此项活动并回答相应问题。(由实验装置引起的实验误差忽略不计)。
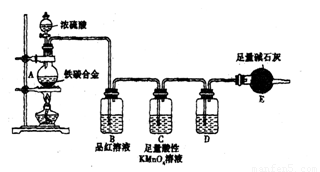
Ⅰ.探究浓硫酸的某些性质
(1)称量E的质量;按照图示连续装置,检查装置的气密性。
(2)将mg铁碳合金样品放入A中,再加入适量的浓硫酸。未点燃酒精灯前,A、B均无明显现象,其原因是: 。点燃酒精灯一段时间后,B中可观察到的明显现象是 。
C中足量的酸性KMnO4溶液所起的作用是 。D中盛放的试剂是 。
(3)反应一段时间后,从A中逸出气体的速率仍然较快,除因反应温度较高外,还可能的原因是 。
Ⅱ.测定铁的质量分数
(4)待A中不再逸出气体时,停止加热,拆下E并称重,E增重bg,则铁碳合金中铁的质量分数为 (写表达式)。某同学认为:依据此实验测得的数据,计算合金中铁的质量分数可能会偏低,你认为可能的原因是 。
(5)经过大家的讨论,决定采用右图装置和其他常用实验仪器测定某些数据即可,为了快速和准确地计算出铁的质量分数,最简便的实验操作是 (填写代号)。
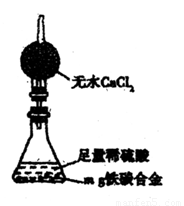
①用排水法测定H2的体积
②反应结束后,过滤、洗涤、干燥、称量残渣的质量
③测定反应前后装置和药品的总质量
科目:gzhx 来源:2013届辽宁省大连协作体高一4月月考化学试卷 题型:实验题
(10分)某化学课外小组为了探究CaCl2溶液和Na2SO4溶液反应有没有限度,设计了如下活动过程,请完成表中空格:(已知CaSO4在水中微溶,CaCO3在水中难溶)
|
实验步骤 |
向3—4 mL 1 mol/L的CaCl2溶液中滴入1mol/L的Na2SO4溶液至反应完全 |
|
实验现象 |
产生白色沉淀 |
|
离子方程式 |
(1) |
|
小组讨论交流 |
向上述反应后的清液中滴入适量1mol/L的Na2CO3 溶液会出现什么现象 |
|
假设出现的实验现象,说明理由 |
假设:Ⅰ 无现象 理由:反应没有限度,Ca2+沉淀完全 假设:Ⅱ(2) ,理由:(3) |
|
证明你的假设 |
现象:产生大量的白色沉淀 |
|
离子方程式 |
(4) |
|
解释 |
(5) |
科目:gzhx 来源:2010年广西柳州二中高三第三次模拟考试(理科综合)化学部分 题型:实验题
(16分)现有某铁碳合金,某化学兴趣小组为了测定铁碳合金中铁的质量分数,并探究浓硫酸的某些性质,设计了下图所示的实验装置和实验方案(夹持仪器已省略),请你回答相应问题。
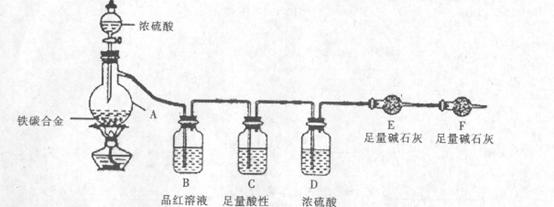
I探究浓硫酸的某些性质
(1)按图示的连接装置,检查装置的气密性,称量E的质量。将mg铁碳合金样品放人A中,再加入适量的浓硫酸。仪器A的名称为 。
(2)未点燃酒精灯前,A、B均无明显现象,其原因是: 。
(3)点燃酒精灯一段时间后,A、B中可观察到明显的现象。B中的现象是 ,由此可得到浓硫酸具有 性。
(4)反应一段时间后,从A中逸出气体的速率仍然较快,除因温度较高,反应放热外,还可能的原因是
Ⅱ测定铁碳合金中铁的质量分数
(5)待A中不再逸出气体时,停止加热,拆下E并称重。E增重b g。铁碳合金中铁的质量分数为 (写表达式),若撤掉装置D,会造成测定结果 (填“偏高”、“不变’’或“偏低”)。
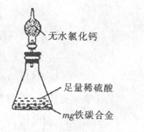
(6)某同学认为上述方法较复杂,使用右图所示的装置和其它常用实验仪器测定某些数据即可。该同学的实验方案是:(只需简要写出操作步骤及需要测定的数据,不必计算)。 。
科目:gzhx 来源:2014届江西省等四校高一下学期联考化学试卷(解析版) 题型:实验题
(9分)某化学课外小组为了探究CaCl2溶液和Na2SO4溶液反应有没有限度,设计了如下活动过程,请完成表中空格:(已知CaSO4在水中微溶,CaCO3在水中难溶)
|
实验步骤 |
向3—4 mL 1 mol/L的CaCl2溶液中滴入1mol/L的Na2SO4溶液至反应完全 |
|
实验现象 |
产生白色沉淀 |
|
离子方程式 |
(1) |
|
小组讨论交流 |
向上述反应后的清液中滴入适量1mol/L的Na2CO3 溶液会出现什么现象 |
|
假设出现的实验现象,说明理由 |
假设:Ⅰ 无现象 理由:反应没有限度,Ca2+沉淀完全 假设:Ⅱ(2) ,理由:(3) |
|
证明你的假设 |
现象:产生大量的白色沉淀 |
|
离子方程式 |
(4) |
|
解释出现假设Ⅱ现象的原因 |
(5) |