
科目:gzhx 来源: 题型:
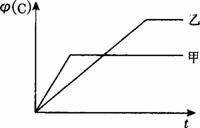
A.研究压强对化学反应速率的影响时,甲的压强较大
B.研究压强对化学平衡的影响时,x>3
C.研究温度对化学反应速率的影响时,乙的温度较高
D.研究温度对化学平衡的影响时,a<0
科目:gzhx 来源:物理教研室 题型:013
下列关于压强对化学反应速率的影响的说法中正确的是
[ ]
A.对于任何化学反应,增大压强都可加快它们的反应速率
B.对于气体反应,增大压强相当于增加反应物浓度,所以反应速率加快
C.对于固态或非固态反应物,由于压强对它们的体积改变很小,可以认为压强与它们的反应速率无关
D.增大压强可以加快合成氨的反应速率
科目:gzhx 来源: 题型:013
下列关于压强对化学反应速率的影响的说法中正确的是
[ ]
A.对于任何化学反应,增大压强都可加快它们的反应速率
B.对于气体反应,增大压强相当于增加反应物浓度,所以反应速率加快
C.对于固态或非固态反应物,由于压强对它们的体积改变很小,可以认为压强与它们的反应速率无关
D.增大压强可以加快合成氨的反应速率
科目:gzhx 来源: 题型:单选题
科目:gzhx 来源: 题型:阅读理解
| 实验 编号 |
室温下,试管中所加试剂及用量/mL | 室温下,溶液褪至无色所需时间/min | |||
| 0.6mol/L H2C2O4溶液 |
H2O | 0.2mol/L KMnO4溶液 |
3mol/L H2SO4溶液 | ||
| 1 | 3.0 | 2.0 | 3.0 | 2.0 | 4.0 |
| 2 | 3.0 | 3.0 | 2.0 | 2.0 | 5.2 |
| 3 | 3.0 | 4.0 | 1.0 | 2.0 | 6.4 |
| 实验 编号 |
室温下,试管中所加试剂及用量/mL | 再向试管中加入少量固体 | 室温下,溶液褪至无色所需时间/min | |||
| 0.6mol/L H2C2O4溶液 |
H2O | 0.2mol/L KMnO4溶液 |
3mol/L H2SO4溶液 | |||
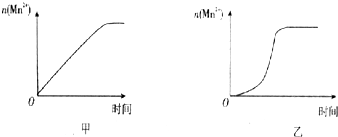
| 4 | 3.0 | 2.0 | 3.0 | 2.0 | MnSO4 MnSO4 (填写所加甲固体的化学式) |
t |
科目:gzhx 来源:2013-2014学年辽宁省抚顺市六校联合体高三上学期期中考试化学试卷(解析版) 题型:填空题
氮及其化合物与人类各方面有着密切的联系。Ⅰ现有一支15mL的试管,充满NO倒置于水槽中,向试管中缓缓通入一定量氧气,当试管内液面稳定时,剩余气体3mL。则通入氧气的体积可能为 mL。
Ⅱ目前,消除氮氧化物污染有多种方法。
(1)用CH4催化还原氮氧化物可以消除氮氧化物的污染。已知:
①CH4(g)+4NO2(g)= 4NO(g)+CO2(g)+2H2O(g) △H=-574kJ/mol
②CH4(g)+4NO(g)= 2N2(g)+CO2(g)+2H2O(g) △H=-1160kJ/mol
③H2O(g)= H2O(l) △H=-44kJ/mol
写出CH4(g)与NO2(g)反应生成N2(g) 、CO2(g)和H2O(l)的热化学方程式 。
(2)用活性炭还原法处理氮氧化物,有关反应为:
某研究小组向恒容密闭容器加入一定量的活性炭和NO,恒温(T0C)条件下反应,反应进行到不同时间测得各物质的浓度如下:
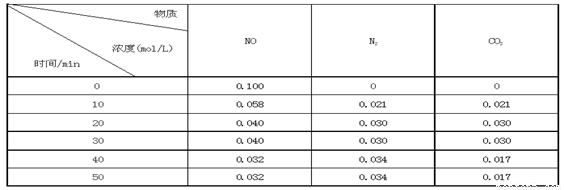
①不能作为判断反应达到化学平衡状态的依据是_______ ;(选填字母代号)
A.容器内CO2的浓度保持不变
B.v正(N2)=2 v正(NO)
C.容器内压强保持不变
D.混合气体的密度保持不变
E.混合气体的平均相对分子质量保持不变
②前20分钟,平均反应速率v(NO)= 。v(NO)=(0.1- 0.04)/ 20 = 0.003mol·L-1· min-1
③在T0C时,该反应的平衡常数为_______(保留两位小数);
④在30 min,改变某一条件反应重新达到平衡,则改变的条件是_______ 。
(3)科学家正在研究利用催化技术将超音速飞机尾气中的NO和CO转变成CO2和N2,其反应为:
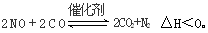
研究表明:在使用等质量催化剂时,增大催化剂的比表面积可提高化学反应速率。为了分别验证温度、催化剂的比表面积对化学反应速率的影响规律,某同学设计了三组实验,部分实验条件已经填在下表中。
|
实验编号 |
T(0C) |
NO初始浓度 (mol/L) |
CO初始浓度 (mol/L) |
催化剂的比 表面积(m2/g) |
|
Ⅰ |
280 |
1.20×10-3 |
5.80×10-3 |
82 |
|
Ⅱ |
a |
b |
c |
124 |
|
Ⅲ |
350 |
d |
e |
124 |
上表中:a=_______,b=________,e=________ 。
科目:gzhx 来源: 题型:
下列说法:
![]() (1)在一定条件下,可逆反应(也是放热反应)N2+3H2
(1)在一定条件下,可逆反应(也是放热反应)N2+3H2![]() 2NH3能够发生,某容器内充入一定量的N2和H2,当单独改变某个条件时:
2NH3能够发生,某容器内充入一定量的N2和H2,当单独改变某个条件时:
![]() ①加催化剂,v(正)、v(逆)都发生变化,且变化倍数相等
①加催化剂,v(正)、v(逆)都发生变化,且变化倍数相等
![]() ②加压,v(正)、v(逆)都增大
②加压,v(正)、v(逆)都增大
![]() ③降温,v(正)、v(逆)都减小,且v(正)减小倍数一定大于v(逆)减小倍数
③降温,v(正)、v(逆)都减小,且v(正)减小倍数一定大于v(逆)减小倍数
![]() ④增加N2的浓度,v(正)、v(逆)都增大
④增加N2的浓度,v(正)、v(逆)都增大
![]() (2)NO和CO都是汽车尾气里的有害气体,它们能缓慢起反应生成N2和CO2.对此:
(2)NO和CO都是汽车尾气里的有害气体,它们能缓慢起反应生成N2和CO2.对此:
![]() ⑤使用催化剂不改变化学反应速率 ⑥升高温度能加快化学反应速率
⑤使用催化剂不改变化学反应速率 ⑥升高温度能加快化学反应速率
![]() ⑦降低压强能加快化学反应速率 ⑧改变压强对化学反应速率无影响
⑦降低压强能加快化学反应速率 ⑧改变压强对化学反应速率无影响
![]() (3)下列说法中:
(3)下列说法中:
![]() ⑨一定条件下增大反应物的量,会加快化学反应速率
⑨一定条件下增大反应物的量,会加快化学反应速率
![]() ⑩升高温度对放热反应会减慢反应速率,对吸热反应会加快反应速率
⑩升高温度对放热反应会减慢反应速率,对吸热反应会加快反应速率
![]() 11加大压强一定会加快反应速率
11加大压强一定会加快反应速率
![]() 12使用催化剂降低反应的活化能,所以会加快反应速率
12使用催化剂降低反应的活化能,所以会加快反应速率
![]() 正确组合是 ( )
正确组合是 ( )
![]() A.①②④⑥12 B.②③⑤⑦⑨ C.④⑤⑨⑩12 D.全部
A.①②④⑥12 B.②③⑤⑦⑨ C.④⑤⑨⑩12 D.全部
科目:gzhx 来源: 题型:013
下列说法:
(1)在一定条件下,可逆反应(也是放热反应)N2+3H2![]() 2NH3能够发生,某容器内充入一定量的N2和H2,当单独改变某个条件时:
2NH3能够发生,某容器内充入一定量的N2和H2,当单独改变某个条件时:
①加催化剂,v(正)、v(逆)都发生变化,且变化倍数相等
②加压,v(正)、v(逆)都增大
③降温,v(正)、v(逆)都减小,且v(正)减小倍数一定大于v(逆)减小倍数
④增加N2的浓度,v(正)、v(逆)都增大
(2)NO和CO都是汽车尾气里的有害气体,它们能缓慢起反应生成N2和CO2。对此:
⑤使用催化剂不改变化学反应速率
⑥升高温度能加快化学反应速率
⑦降低压强能加快化学反应速率
⑧改变压强对化学反应速率无影响
(3)下列说法中:
⑨一定条件下增大反应物的量,会加快化学反应速率
⑩升高温度对放热反应会减慢反应速率,对吸热反应会加快反应速率
⑾加大压强一定会加快反应速率
⑿使用催化剂降低反应的活化能,所以会加快反应速率
正确组合是( )
A.①②④⑥⑿ B.②③⑤⑦⑨ C.④⑤⑨⑩⑿ D.全部
科目:gzhx 来源:物理教研室 题型:013
(1)在一定条件下,可逆反应(也是放热反应)N2+3H2![]() 2NH3能够发生,某容器内充入一定量的N2和H2,当单独改变某个条件时:
2NH3能够发生,某容器内充入一定量的N2和H2,当单独改变某个条件时:
①加催化剂,v(正)、v(逆)都发生变化,且变化倍数相等
②加压,v(正)、v(逆)都增大
③降温,v(正)、v(逆)都减小,且v(正)减小倍数一定大于v(逆)减小倍数
④增加N2的浓度,v(正)、v(逆)都增大
(2)NO和CO都是汽车尾气里的有害气体,它们能缓慢起反应生成N2和CO2。对此:
⑤使用催化剂不改变化学反应速率
⑥升高温度能加快化学反应速率
⑦降低压强能加快化学反应速率
⑧改变压强对化学反应速率无影响
(3)下列说法中:
⑨一定条件下增大反应物的量,会加快化学反应速率
⑩升高温度对放热反应会减慢反应速率,对吸热反应会加快反应速率
⑾加大压强一定会加快反应速率
⑿使用催化剂降低反应的活化能,所以会加快反应速率
正确组合是( )
A.①②④⑥⑿ B.②③⑤⑦⑨ C.④⑤⑨⑩⑿ D.全部
科目:gzhx 来源: 题型:阅读理解
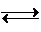 CO(g)+3H2(g)△H=+206.1kJ•mol-1.
CO(g)+3H2(g)△H=+206.1kJ•mol-1.| CH4 | H2O | CO | H2 |
| 3.0mol•L-1 | 8.5mol•L-1 | 2.0mol•L-1 | 2.0mol•L-1 |
| 实验序号 | 温度/℃ | 压强/kPa | CH4初始浓度/mol•L-1 | H2O初始浓度/mol•L-1 | K |
| 1 | 360 | P | 2.00 | 6.80 | K1 |
| 2 | t | 101 | 2.00 | 6.80 | K2 |
| 3 | 360 | 101 | 2.00 | 6.80 | K3 |
| ||
| x |
| 2 |
科目:gzhx 来源: 题型:
| 高温 |
| 高温 |
| 高温 |
| 实验 组别 |
温度℃ | 起始量/mol | 平衡/mol | 达平衡所 需时间/min | ||||
| H2O | CO | H2 | CO2 | H2 | CO2 | |||
| 1 | 650 | 2 | 4 | 0 | a | 1.6 | 2.4 | 5 |
| 2 | 900 | 1 | 2 | 0 | b | 0.4 | 1.6 | 3 |
| 高温 |
| 组别 | 温度 | 催化剂 | … |
| 1 | |||
| 2 | |||
科目:gzhx 来源: 题型:阅读理解
| 催化剂 |
| 时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| c(NO)(mol/L) | 1.00×10-3 | 4.50×10-4 | 2.50×10-4 | 1.50×10-4 | 1.00×10-4 | 1.00×10-4 |
| c(CO)(mol/L) | 3.60×10-3 | 3.05×10-3 | 2.85×10-3 | 2.75×10-3 | 2.70×10-3 | 2.70×10-3 |
| c(N2)c2(CO2) |
| c2(NO)c2(CO) |
| c(N2)c2(CO2) |
| c2(NO)c2(CO) |
| 实验 编号 |
T(℃) | NO初始浓度 (mol/L) |
CO初始浓度 (mol/L) |
催化剂的比表面积(m2/g) |
| Ⅰ | 280 | 1.20×10-3 | 5.80×10-3 | 82 |
| Ⅱ | 280 280 |
1.20×10-3 1.20×10-3 |
1.20×10-3 1.20×10-3 |
124 |
| Ⅲ | 350 | 5.80×10-3 5.80×10-3 |
5.80×10-3 5.80×10-3 |
124 |
科目:gzhx 来源: 题型:
| c(CO)c(H2) |
| c(H2O) |
| c(CO)c(H2) |
| c(H2O) |
科目:gzhx 来源: 题型:
A.通常,温度升高,反应速率常数增大,化学反应速率提高
B.化学反应的活化能越大,温度对化学反应速率的影响越大
C.温度升高,降低化学反应的活化能,化学反应速率提高
D.升高相同温度,对不同化学反应的反应速率的影响程度是一样的
科目:gzhx 来源:2014届内蒙古巴市高一下学期期末考试化学试卷(解析版) 题型:选择题
NO和CO都是汽车尾气中的有害物质,它们能缓慢地起反应,生成N2和CO2,对此反应的下列叙述中正确的是( )
A.使用催化剂不能加快反应速率
B.降低压强能加快反应速率
C.升高温度能加快反应速率
D.改变压强对化学反应速率无影响
科目:gzhx 来源:2011-2012年江苏赣榆县厉庄中学高一下学期第一次检测化学试卷(解析版) 题型:选择题
NO和CO都是汽车尾气中的有害物质,它们能缓慢地起反应,生成N2和CO2,对此反应的下列叙述中正确的是( )
A.使用催化剂不能加快反应速率
B.降低压强能加快反应速率
C.升高温度能加快反应速率
D.改变压强对化学反应速率无影响
科目:gzhx 来源:2010-2011年云南省高二下学期期末考试化学试卷 题型:实验题
(13分)I.某校化学实验小组探究浓度对化学反应速率的影响,并测定(NH4)2S2O8和KI反应的化学反应速率。进行如下实验探究:
【实验原理】
(NH4)2S2O8和KI反应的离子方程式为:S2O82- + 2I-= 2SO42- + I2 (1)
平均反应速率的计算式为v(S2O82-)=  。
。
实验时,向KI、Na2S2O3和淀粉指示剂混合溶液中加入(NH4)2S2O8溶液,不断搅拌。
在反应(1)进行的同时,发生反应:2S2O32-+ I2 = S4O62-+ 2I- (2)
反应(1)生成的I2立即与S2O32-反应,生成无色的S4O62-和I-。S2O32-耗尽时,反应(1)继续生成的I2才与淀粉作用呈现蓝色。从加入(NH4)2S2O8溶液到出现蓝色的时间为Δt。
【实验内容】
(1)实验小组设计的实验记录表和数据记录如下,请将表中字母表示的空格填上。
|
实 验 编 号 |
① |
② |
③ |
④ |
⑤ |
|
|
试剂 用量 (mL) |
0.20 mol·L-1 (NH4)2S2O8溶液 |
20.0 |
10.0 |
b |
20.0 |
20.0 |
|
0.20 mol·L-1 KI溶液 |
20.0 |
20.0 |
20.0 |
10.0 |
5.0 |
|
|
0.010 mol·L-1 Na2S2O3溶液 |
a |
8.0 |
8.0 |
8.0 |
8.0 |
|
|
0.2% 淀粉溶液 |
2.0 |
2.0 |
2.0 |
2.0 |
2.0 |
|
|
0.20 mol·L-1KNO3溶液 |
0 |
0 |
0 |
10.0 |
c |
|
|
0.20 mol·L-1(NH4)2SO4溶液 |
0 |
10.0 |
15.0 |
0 |
0 |
|
|
20 ℃时,反应时间Δt(s) |
32 |
67 |
130 |
66 |
135 |
|
|
为了使溶液的离子强度和总体积保持不变,减少的(NH4)2S2O8溶液或KI溶液的用量,分别用(NH4)2SO4溶液或KNO3溶液补足;溶液混合后体积不变 |
(2)为了使反应充分进行,减少数据误差,实验过程中应该不断进行的操作是 。
(3)第①组实验的v(S2O82-)= mol·(L·s)-1。
(4)根据上表数据分析,可以得到的结论有(写出一条即可)
。
II.实验小组查资料得知,向含有Na2CO3的Na2S溶液中通入SO2,可以制备上述实验所需的Na2S2O3。反应如下:Na2CO3 + SO2= Na2SO3 + CO2;2Na2S + 3SO2 = 2Na2SO3 + 3S↓;
Na2SO3 + S= Na2S2O3。该小组根据上述原理设计下图所示装置制备Na2S2O3。

(1)实验应避免有害气体排放到空气中。装置①、②中盛放的试剂依次是
① ;
② 。
(2)实验过程中,随着气体的通入,装置①中有气泡产生,还有大量黄色固体析出,继续通入气体,可以观察到的现象是 。
(3)反应结束后,从制得的Na2S2O3稀溶液中得到Na2S2O3·5H2O晶体的主要操作包括: 。
科目:gzhx 来源: 题型:阅读理解
I.某校化学实验小组探究浓度对化学反应速率的影响,并测定![]() 和KI反应的化学反应速率。进行如下实验探究:
和KI反应的化学反应速率。进行如下实验探究:
【实验原理】
![]() 和KI反应的离子方程式为:
和KI反应的离子方程式为:
![]() (1)
(1)
平均反应速率的计算式为![]() 。
。
实验时,向![]() 、
、![]() 和淀粉指示剂混合溶液中加入
和淀粉指示剂混合溶液中加入![]() 溶液,不断搅拌。
溶液,不断搅拌。
在反应(1)进行的同时,发生反应:
![]() (2)
(2)
反应(1)生成的![]() 立即与
立即与![]() 反应,生成无色的
反应,生成无色的![]() 和
和![]() 。
。![]() 耗尽时,反应(1)继续生成的
耗尽时,反应(1)继续生成的![]() 才与淀粉作用呈现蓝色。从加入
才与淀粉作用呈现蓝色。从加入![]() 溶液到出现蓝色的时间为
溶液到出现蓝色的时间为![]() 。
。
【实验内容】
(1)实验小组设计的实验记录表和数据记录如下,请将表中字母表示的空格填上。
| 实验编号 | ① | ② | ③ | ④ | ⑤ | |
| 试剂 用量 (mL) | 0.20 mol·L | 20.0 | 10.0 | b | 20.0 | 20.0 |
| 0.20 mol·L | 20.0 | 20.0 | 20.0 | 10.0 | 5.0 | |
| 0.010 mol·L | a | 8.0 | 8.0 | 8.0 | 8.0 | |
| 0.2%淀粉溶液 | 2.0 | 2.0 | 2.0 | 2.0 | 2.0 | |
| 0.20 mol·L | 0 | 0 | 0 | 10.0 | c | |
| 0.20 mol·L | 0 | 10.0 | 15.0 | 0 | 0 | |
| 20℃时,反应时间 | 32 | 67 | 130 | 66 | 135 | |
| 为了使溶液的离子强度和总体积保持不变,减少的(NH4)2S2O8溶液或KI溶液的用量,分别用(NH4)2SO4溶液或KNO3溶液补足;溶液混合后体积不变 | ||||||
(2)为了使反应充分进行,减少数据误差,实验过程中应该不断进行的操作是 。
(3)第①组实验的![]() mol·(L·s)
mol·(L·s)![]() 。
。
(4)根据上表数据分析,可以得到的结论有(写出一条即可) 。
II.实验小组查资料得知,向含有NaCO3的Na2S溶液中通入SO2,可以制备上述实验所需的Na2S2O3。反应如下:
![]()
![]()
![]()
该小组根据上述原理设计如图19所示装置制备![]() 。
。
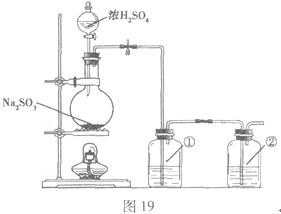
(1)实验应避免有害气体排放到空气中。装置①、②中盛放的试剂依次是① ;② 。
(2)实验过程中,随着气体的通入,装置①中有大量黄色固体析出,继续通入气体,可以观察到的现象是 。
(3)反应结束后,从制得的![]() 稀溶液中得到
稀溶液中得到![]() 晶体的主要操作包括: 。
晶体的主要操作包括: 。