
科目:gzhx 来源:广东省汕头市2007年普通高校招生模拟考试化学试卷 题型:013
|
二元酸H2A在水中发生电离:H2A | |
| [ ] | |
A. |
NaHA:c(Na+)>c(HA?/SUP>)> H++A2?/SUP>,c(OH?/SUP>)>c(H+) |
B. |
NaHA:c(Na+)=c(A2?/SUP>)+c(HA?/SUP>) |
C. |
Na2A:c(Na+)>c(A2?/SUP>)>c(OH?/SUP>)>c(H+) |
D. |
H2A:c(H+)=c(HA?/SUP>)+2c(A2?/SUP>)+c(OH?/SUP>) |
科目:gzhx 来源:2005年普通高等学校招生全国统一考试、化学 题型:021
|
关于小苏打水溶液的表述正确的是 | |
A. |
c(Na+)=c(HCO3?/SUP>)+c(CO32?/SUP>)+c(H2CO3) |
B. |
c(Na+)+c(H+)=c(HCO3?/SUP>)+c(CO32?/SUP>)+c(OH?/SUP>) |
C. |
HCO3?/SUP>的电离程度大于HCO3?/SUP>的水解程度 |
D. |
存在的电离有:NaHCO3=Na++HCO3?/SUP>,HCO3?IMG SRC="http://thumb.1010pic.com/pic7/pages/62A2/0016/0019/f4f289bed42553be14f0bec39e8cda36/A/Image4.gif" width=34 HEIGHT=8>H++CO32?/SUP>,H2O |
科目:gzhx 来源:甘肃省张掖中学2007届高三年级模拟训练、化学试卷 题型:013
|
下列反应的离子方程式正确的是 | |
| [ ] | |
A. |
Fe3O4与稀硝酸反应:Fe3O4+8H+ |
B. |
电解饱和食盐水:2Cl-+2H2O |
C. |
Ca(HCO3)2与过量Ca(OH)2溶液反应:Ca2++2HCO3?/SUP>+2OH?IMG SRC="http://thumb.1010pic.com/pic7/pages/62A2/0154/0009/68bfcc9ff085c76dd7e7c9ace66a977a/A/Image1.gif" width=36 HEIGHT=6>CaCO3↓+CO32?/SUP>+2H2O |
D. |
Na2S溶液呈碱性:S2?/SUP>+2H2O |
科目:gzhx 来源:2006年五月理科综合模拟化学部分、(第一套) 题型:013
|
已知某酸H2A在水中的电离方程式是:H2A H++HA?/SUP>、HA?IMG SRC="http://thumb.1010pic.com/pic7/pages/62A2/0008/0112/55ccc2554c1f06a87f43d83d3ab36c6a/A/Image150.gif" width=44 HEIGHT=15>H++A2?/SUP>,那么在0.1 mol·L—1的Na2A溶液中,下列微粒浓度关系不正确的是 | |
| [ ] | |
A. |
c(A2?/SUP>)+c(HA?/SUP>)+c(H2A)=0.1 mol·L—1 |
B. |
c(OH?/SUP>)=c(H+)+c(HA?/SUP>) |
C. |
c(Na+)+c(H+)=c(OH?/SUP>)+c(HA?/SUP>)+2c(A2?/SUP>) |
D. |
c(Na+)=2c(A2?/SUP>)+2c(HA?/SUP>) |
科目:gzhx 来源: 题型:
2007年度http://today.ks5u.com诺贝尔化学奖获得者格哈德·埃特尔建立了合成氨反应机理,T=673K时,各步反应的能量变化如图所示,图中的能量单位为kJ·mol-1。(注:图中“吸”表示在催化剂表面的吸附)请回答下列问题:
(1)合成氨反应的机理为
① ;
![]()
![]()
![]() ②N2 N2吸 2N 2N吸
②N2 N2吸 2N 2N吸
③ ;
![]() ④NH吸+H吸 NH2吸;
④NH吸+H吸 NH2吸;
![]()
![]() ⑤NH2吸+H吸 NH3吸 NH3。
⑤NH2吸+H吸 NH3吸 NH3。
(2)T=673K时,合成氨反应的热化学方程为 。
(3)液氨与水颇为相像,它能溶解多种无机及有机分子,其电离方程式可表示为:
![]() 2NH3 NH+4+NH-2(某温度http://today.ks5u.com下其离子积常数为10-30)。液氨中的pNH4与水中的pH类似,则该温度http://today.ks5u.com下液氨的pNH4= 。
2NH3 NH+4+NH-2(某温度http://today.ks5u.com下其离子积常数为10-30)。液氨中的pNH4与水中的pH类似,则该温度http://today.ks5u.com下液氨的pNH4= 。
(4)盐酸肼(N2H4Cl2)是一种重要的化工原料,属于离子化合物,易溶于水,溶液呈酸性,水解原理与NH4Cl类似。写出盐酸肼第一步水解反应的离子方程式 。
(5)肼(N2H4)又称联氨,是一种可燃性的液体,可用作火箭燃料。已知在101kPa时,N2H4在氧气中完全燃烧生成氮气,肼—空气燃料电池是一种碱性燃料电池,电解质溶液是20%~30%的KOH溶液。肼—空气燃料电池放电时:
负极的电极反应式是 。
科目:gzhx 来源:广东省汕头市2007年普通高校招生模拟考试化学试卷 题型:013
|
下列离子方程式表示正确的是 | |
| [ ] | |
A. |
铜片加入稀硝酸中:Cu+NO3?/SUP>+4H+ |
B. |
过量SO2通入次氯酸钙溶液中:Ca2++2ClO?/SUP>+SO2+H2O |
C. |
等体积、等物质的量浓度的NaHCO3和Ba(OH)2两溶液混合:HCO3?/SUP>+Ba2++OH?IMG SRC="http://thumb.1010pic.com/pic7/pages/62A2/0165/0006/7b95aa800ad08891908bdcd80bf96b18/A/Image4.gif" width=32 HEIGHT=3>BaCO3↓+H2O |
D. |
铁作电极电解饱和食盐水:2Cl?/SUP>+2H2O |
科目:gzhx 来源:江苏省邗江中学2006~2007学年度第一学期高三化学期中试卷(旧人教) 旧人教 题型:013
|
下列反应的离子方程式正确的是 | |
| [ ] | |
A. |
Fe3O4与稀硝酸反应:Fe3O4+8H+ |
B. |
电解饱和食盐水:2Cl-+2H2O |
C. |
Ca(HCO3)2与过量Ca(OH)2溶液反应:Ca2++2HCO3?/SUP>+2OH?IMG SRC="http://thumb.1010pic.com/pic7/pages/62A2/0200/0009/63acbeeedb5f41aed182511a7af49814/A/Image2.gif" width=36 HEIGHT=6>CaCO3↓+CO32?/SUP>+2H2O |
D. |
Na2S溶液呈碱性:S2?/SUP>+2H2O |
科目:gzhx 来源:2013届海南省高二上学期期末考试理科化学试卷(解析版) 题型:选择题
已知一定温度下2X(g) + Y (g)  mZ(g)
ΔH= -a kJ·mol-1 (a>0),现有甲乙两容积相等且固定不变的密闭容器,在保持该温度下,向密闭容器甲中通入2molX和1molY,达到平衡状态时,放出热量bkJ;向密闭容器乙中通入1molX和0.5molY,达到平衡状态时,放出热量ckJ,且b>2c,则a、b、m的值或关系正确的是( )[来源:Z§xx§k.Com]
mZ(g)
ΔH= -a kJ·mol-1 (a>0),现有甲乙两容积相等且固定不变的密闭容器,在保持该温度下,向密闭容器甲中通入2molX和1molY,达到平衡状态时,放出热量bkJ;向密闭容器乙中通入1molX和0.5molY,达到平衡状态时,放出热量ckJ,且b>2c,则a、b、m的值或关系正确的是( )[来源:Z§xx§k.Com]
A.m=4 B.a=b C.b<a D.m等于2或1
科目:gzhx 来源: 题型:
阻垢剂可防止工业用水过程中无机物沉积结构,经由下列反应路线可得知到E和R两种阻垢剂(部分反应条件略去)
(1)阻垢剂E的制备
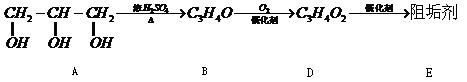
①A可由人类重要的营养物质 水解制得(填“糖类”、“油脂”或“蛋白质”)
②B与新制的![]() 反应生成D,其化学方程式为 。
反应生成D,其化学方程式为 。
③D经加聚反应生成E,E的结构简式为 。
(2)阻垢剂R的制备
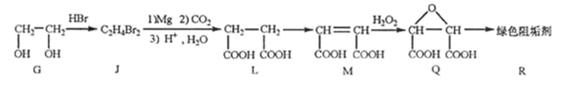
①G→J为取代反应,J的结构简式为 。www.k@s@5@u.com 高#考#资#源#网
②由L制备M的反应步骤依次为:
![]()
、 (用化学方程式表示)。
③1mol Q的同分异构体T(碳链无支链)与足量![]() 溶液作用产生2mol
溶液作用产生2mol ![]() ,T的结构简式为 (只写一种)。
,T的结构简式为 (只写一种)。
科目:gzhx 来源:2012届河南省焦作市高三第一次质量检测理综化学部分(带解析) 题型:填空题
(15分)中学化学常见部分元素原子结构及性质如下表所示:
| 序号 | 元素 | 结构及性质 |
| ① | A | A单质是生活中常见金属,它有两种氯化物,相对分子质量相差35.5 |
| ② | B | B原子K、L、M层电子数之比是1:4:1 |
| ③ | C | C是活泼非金属元素,其单质常温下呈气态但化学性质稳定 |
| ④ | D | D单质被誉为“信息革命的催化剂”,是常用的半导体材料[来源:Z*xx*k.Com] |
| ⑤ | E | 通常情况下,E没有正化合价,A、C、F都能与E形成二种或二种以上化合物 |
| ⑥ | F | F在周期表中可以排在ⅠA族,也有人提出排在ⅦA族 |
科目:gzhx 来源:2014届浙江省高一下学期第一次质量检测化学试卷(解析版) 题型:选择题
关于元素性质或特点的说法正确的是
A.最外层电子数≥4的元素均为非金属元素,
B.最外层电子数=2的元素均为第ⅡA族元素,
C.第m主族的非金属元素X的气态氢化物化学式为HmX,
D.在元素周期表中金属和非金属元素分界处可以找到半导体材料。[来源:Z+xx+k.Com]
科目:gzhx 来源: 题型:
短周期元素X、Y、Z、M、N原子序数依次增大,有关信息如下:
| 元素 | 有关信息 |
| X | 最外层电子数是次外层的2倍 |
| Y | 元素主要化合价为—2价 |
| Z | 其单质及化合物的焰色为黄色[来源:Zxxk.Com] |
| M | 与X同主族,其单质为半导体材料 |
| N |
|
(1)XY2的电子式是 ;Z2Y2中所含化学键类型是 ;XY2与Z2Y2反应的化学方程式是 。
(2)恒容条件下,一定量的NY2、Y2发生反应:2NY2(g)+Y2(g)![]() 2NY3(g)。温度分别为T1和T2时,NY3的体积分数随时间变化如右图,该反应的△H 0(填“>”“<”或“=”,下同);若T1、T2时刻反应的化学平衡常数分别为K1、K2,则K1 K2。
2NY3(g)。温度分别为T1和T2时,NY3的体积分数随时间变化如右图,该反应的△H 0(填“>”“<”或“=”,下同);若T1、T2时刻反应的化学平衡常数分别为K1、K2,则K1 K2。

(3)X的非金属性比M (填“强”或“弱”),能证明此结论的事实是 (用离子方程式表示)。
科目:gzhx 来源: 题型:
(11分)Fenton法常用于处理含难降解有机物的工业废水,通常是在调节好pH和Fe2+浓度的废水中加入H2O2,所产生的羟基自由基能氧化降解污染物。现运用该方法降解有机污染物p-CP,探究有关因素对该降解反应速率的影响。
[实验设计]控制p-CP的初始浓度相同,恒定实验温度在298K或313K(其余实验条件见下表),设计如下对比试验。http://photo.blog.sina.com.cn/showpic.html- blog>
(1)完成以下实验设计表(表中不要留空格)。
| 实验 编号 | 实验目的 | T/K | pH | c/10-3mol·L-1 | |
| H2O2 | Fe2+ | ||||
| ① | 为以下实验作参照 | 298 | 3 | 6.0 | 0.30 |
| ② | 探究温度对降解反应速率的影响 |
|
|
|
|
| ③ |
| 298 | 10 | 6.0 | 0.30 |
[数据处理]实验测得p—CP的浓度随时间变化的关系如下图。
(2)请根据上图实验①曲线,计算降解反应在50~150s内的平均反应速率;v(p—CP)= mol·L-1·s-1。
[解释与结论]
(3)实验①、②表明温度升高,该降解反应速率增大。但温度过高时(如接近100℃)反而导致降解反应速率减小,请从Fenton法所用试剂H2O2的角度分析原因: 。
(4)实验③得出的结论是:pH等于10时, 。
[思考与交流]
(5)实验时需在不同时间从反应器中取样,并使所取样品中反应立即停止下来。根据上图中的信息,给出一种迅速停止反应的方法:
科目:gzhx 来源:2010-2011学年江西省高三上学期期中考试化学卷 题型:填空题
(9分)现有A、B、C三种均含同一种元素的无机物,它们之间的转化关系如下图所示(部分产物已略去):
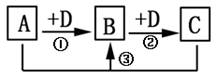
(1)若A、D为非金属单质:
①当M(A)>M(D)时,D为: ;
②当M(D)>M(A)时,A为: ;
(2)若A为非金属单质,D为金属单质时,A为: ;[来源:Z.xx.k.Com]
(3)若D为非金属单质,A、B、C为卤化物时,写出①的化学反应方程式: 。
科目:gzhx 来源:2010年黑龙江省高三上学期第二次月考(化学) 题型:选择题
在浓盐酸中H3AsO3与SnCl2反应的离子方程式为:3SnCl2+12Cl-+2H3AsO3+6H+===2As+3SnCl+6M,关于该反应的说法中正确的组合是 ( ) [来源:Zxxk.Com]
①氧化剂是H3AsO3 ②还原性:Cl->As ③每生成7.5 g As,还原剂失去的电子为0.3 mol ④M为OH- ⑤SnCl是氧化产物
A.①③⑤ B.①②④⑤ C.①②③④ D.①③
科目:gzhx 来源:2010年春季武汉睿升学校高一期中考试化学卷 题型:填空题
(16分)下图是元素周期表的前四周期的结构,请回答
| A | | | |||||||||||||||
| | | | | B | C | D | | | |||||||||
| E | | F | | | | G | | ||||||||||
| | | | | | | | H | | | | | | | | | | |
科目:gzhx 来源:2010—2011学年山东省济南外国语学校高二入学检测化学试卷 题型:填空题
(17分)(1)AgNO3的水溶液呈 (填“酸”、“中”、“碱”)性,原因是(用离子方程式表示): ;实验室在配制AgNO3的溶液时,常将AgNO3固体先溶于较浓的 中,然后再用蒸馏水稀释到所需的浓度。若用惰性电极电解AgNO3的水溶液,请写出电池反应的离子方程式
(2)常温下,某纯碱(Na2CO3)溶液中滴入酚酞,溶液呈红色。在分析该溶液遇酚酞呈红色原因时,甲同学认为是配制溶液所用的纯碱样品中混有NaOH所至;乙同学认为是溶液中Na2CO3电离出的CO32—水解所至。请你设计一个简单的实验方案给甲和乙两位同学的说法以评判(包括操作、现象和结论)
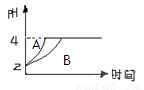
(3)常温下,取pH=2的盐酸和醋酸溶液各100mL,向其中分别加入适量的Zn粒,反应过程中两溶液的pH变化如图所示。则图中表示醋酸溶液中pH变化曲线的是 (填“A”或“B”)。设盐酸中加入的Zn质量为m1,醋酸溶液中加入的Zn质量为m2。则m1 m2(选填“<”、“=”、“>”)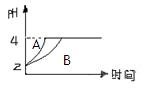
(4)钢铁很容易生锈而被腐蚀,每年因腐蚀而损失的钢材占世界钢铁年产量的四分之一。
①钢铁腐蚀主要是吸氧腐蚀,该腐蚀过程中的电极反应式为:
负极:
正极: ;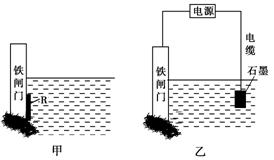
②为了降低某水库的铁闸门被腐蚀的速率,可以采用图甲所示的方案,其中焊接在铁闸门上的固体材料R可以采用________。
| A.铜 | B.钠 | C.锌 | D.石墨 |
 http://photo.blog.sina.com.cn/showpic.html - blogid=515359c40100g2ml&url=http://static3.photo.sina.com.cn/orignal/515359c4g79a1c1001942&690
http://photo.blog.sina.com.cn/showpic.html - blogid=515359c40100g2ml&url=http://static3.photo.sina.com.cn/orignal/515359c4g79a1c1001942&690科目:gzhx 来源:2012届山东省高二入学检测化学试卷 题型:填空题
(17分)(1)AgNO3的水溶液呈 (填“酸”、“中”、“碱”)性,原因是(用离子方程式表示): ;实验室在配制AgNO3的溶液时,常将AgNO3固体先溶于较浓的 中,然后再用蒸馏水稀释到所需的浓度。若用惰性电极电解AgNO3的水溶液,请写出电池反应的离子方程式
(2)常温下,某纯碱(Na2CO3)溶液中滴入酚酞,溶液呈红色。在分析该溶液遇酚酞呈红色原因时,甲同学认为是配制溶液所用的纯碱样品中混有NaOH所至;乙同学认为是溶液中Na2CO3电离出的CO32—水解所至。请你设计一个简单的实验方案给甲和乙两位同学的说法以评判(包括操作、现象和结论)
(3)常温下,取pH=2的盐酸和醋酸溶液各100mL,向其中分别加入适量的Zn粒,反应过程中两溶液的pH变化如图所示。则图中表示醋酸溶液中pH变化曲线的是 (填“A”或“B”)。设盐酸中加入的Zn质量为m1, 醋酸溶液中加入的Zn质量为m2。则m1 m2(选填“<”、“=”、“>”)
(4)钢铁很容易生锈而被腐蚀,每年因腐蚀而损失的钢材占世界钢铁年产量的四分之一。
①钢铁腐蚀主要是吸氧腐蚀,该腐蚀过程中的电极反应式为:
负极:
正极: ;
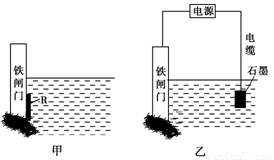
②为了降低某水库的铁闸门被腐蚀的速率,可以采用图甲所示的方案,其中焊接在铁闸门上的固体材料R可以采用________。
A.铜 B.钠 C.锌 D.石墨
③图乙所示的方案也可以降低铁闸门的腐蚀速率,其中铁闸门应该连接在直流电源的________极。
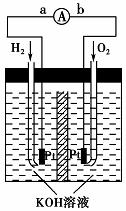
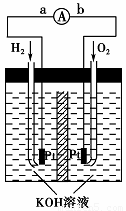
(5)氢氧燃料电池是符合绿色化学理念的新型发电装置。下图为电池示意图,该电池电极表面镀一层细小的铂粉,铂吸附气体的能力强,性质稳定,请回答:
 http://photo.blog.sina.com.cn/showpic.html
- blogid=515359c40100g2ml&url=http://static3.photo.sina.com.cn/orignal/515359c4g79a1c1001942&690
http://photo.blog.sina.com.cn/showpic.html
- blogid=515359c40100g2ml&url=http://static3.photo.sina.com.cn/orignal/515359c4g79a1c1001942&690
①氢氧燃料电池的能量转化主要形式是 ,在导线中电子流动方向为 (用a、b表示)。
②负极反应式为 。
③电极表面镀铂粉的原因为 。
科目:gzhx 来源:2010-2011学年云南省高三1月月考(理综)化学部分 题型:填空题
有机物A的分子式为C9H10O2,A在光照条件下生成的一溴代物B,可发生如下转化关系(无机产物略):([ O ]指发生氧化反应)

其中K与FeCl3溶液能发生显色反应,且环上的一元取代物只有两种结构。
已知:① 当羟基与双键碳原子相连时,易发生如下转化:
RCH=CHOH à RCH2CHO。
② —ONa连在烃基上不被氧化。
请回答下列问题:
(1)F与I中具有相同的官能团,检验该官能团的试剂是 。[来源:Zxxk.Com]
(2)上述变化中属于水解反应的是 (填编号)。
(3)写出结构简式:G ;M 。
(4)写出下列反应的化学方程式:反应① ;K与NaHCO3溶液反应 。
(5)写出同时符合下列要求的A的同分异构体的结构简式 。
I.含有苯环 II.能发生银镜反应和水解反应
III.在稀的NaOH溶液中,1mol该同分异构体能与1mol NaOH反应