
科目:gzhx 来源: 题型:


科目:gzhx 来源: 题型:


科目:gzhx 来源:2011届福建省三明二中高三第二次模拟考试(理综)化学试题 题型:填空题
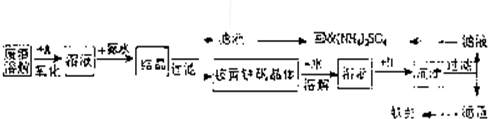
工业上利用硫酸渣(含Fe2+、Fe3+的硫酸盐及少量CaO和MgO)制备高档颜料铁红(Fe2O3 )和回收(NH4)2SO4,具体生产流程如下:
|
| A.氨水 | B.氢氧化钠 | C.盐酸 | D.硫酸 |
科目:gzhx 来源:2013届江苏省泰州中学高三上学期期中考试化学试卷(带解析) 题型:填空题
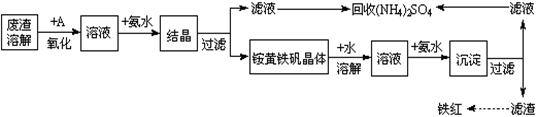
(12分)工业上利用硫酸渣(含Fe2+、Fe3+的硫酸盐及少量CaO和MgO)制备高档颜料铁红(Fe2O3)和回收(NH4)2SO4,具体生产流程如下:
(1)在废渣溶解时需要使用酸,应选用__________,为了提高废渣的浸取率,可采用的措施有哪些?
_____________________________________________________________(至少写出两点)。
(2)物质A是一种氧化剂,工业上最好选用_____________(供选择使用的有:空气、Cl2、MnO2),其理由是 (至少写出两点)。
(3)“结晶”反应的化学方程式为__________________________________________________。
(4)上述生产流程中多处采用了过滤操作,实验室中完成相应的操作需要用到的玻璃仪器有烧杯及____________________________________________。
科目:gzhx 来源:2010-2011学年广东省高三第五次综合测试(理综)化学试题 题型:填空题
工业上利用硫酸渣(含Fe2+、Fe3+的硫酸盐及少量CaO和MgO)制备高档颜料铁红(Fe2O3 )和回收(NH4)2SO4,具体生产流程如下:
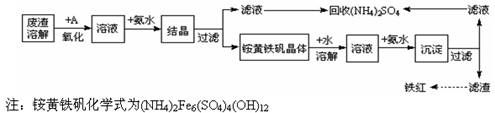
(1)在废渣溶解操作时,应选用__________溶解(填字母)。
A、氨水 B、氢氧化钠 C、盐酸 D、硫酸
(2)物质A是一种氧化剂,工业上最好选用 (供选择使用的有:空气、Cl2、MnO2),其理由是 。
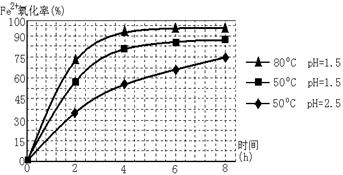
(3)根据下图有关数据,你认为工业上氧化操作时应控制的条件是: 。
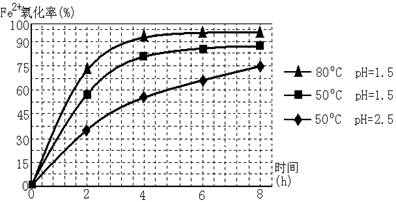
(4)“结晶”反应的化学方程式为_________________ ____________________。
(5)简述检验“滤液”中含有NH4+的实验方法: 。
科目:gzhx 来源:2012-2013学年江苏省高三上学期期中考试化学试卷(解析版) 题型:填空题
(12分)工业上利用硫酸渣(含Fe2+、Fe3+的硫酸盐及少量CaO和MgO)制备高档颜料铁红(Fe2O3)和回收(NH4)2SO4,具体生产流程如下:
|
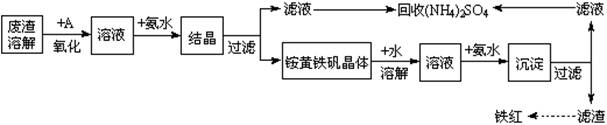
(1)在废渣溶解时需要使用酸,应选用__________,为了提高废渣的浸取率,可采用的措施有哪些?
_____________________________________________________________(至少写出两点)。
(2)物质A是一种氧化剂,工业上最好选用_____________(供选择使用的有:空气、Cl2、MnO2),其理由是 (至少写出两点)。
(3)“结晶”反应的化学方程式为__________________________________________________。
(4)上述生产流程中多处采用了过滤操作,实验室中完成相应的操作需要用到的玻璃仪器有烧杯及____________________________________________。
科目:gzhx 来源: 题型:
工业上利用硫酸渣(含Fe2+、Fe3+的硫酸盐及少量CaO和MgO)制备高档颜料铁红(Fe2O3)和回收(NH4)2SO4,具体生产流程如下:
![]()
(1)在废渣溶解操作时,应选用__________溶解(填字母)。
A、氨水 B、氢氧化钠 C、盐酸 D、硫酸
(2)物质A是一种氧化剂,工业上最好选用 (供选择使用的有:空气、Cl2、MnO2),其理由是 。
(3)根据下图有关数据,你认为工业上氧化操作时应控制的条件是:
。
(4)“结晶”反应的化学方程式为
。
(5)简述检验“滤液”中含有NH4+的实验方法:
。
科目:gzhx 来源: 题型:
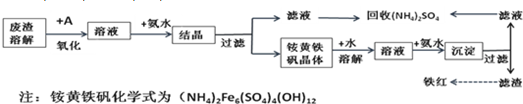
工业上利用硫酸渣(含Fe2+、Fe3+的硫酸盐及少量CaO和MgO)制备高档颜料铁红(Fe2O3 )和回收(NH4)2SO4,具体生产流程如下:
(1)在废渣溶解操作时,应选用__________溶解(填字母)。
A、氨水 B、氢氧化钠 C、盐酸 D、硫酸
(2)物质A是一种氧化剂,工业上最好选用 (供选择使用的有:空气、Cl2、MnO2),其理由是 。
(3)根据下图有关数据,你认为工业上氧化操作时应控制的条件是: 。
(4)“结晶”反应的化学方程式为_________________ ____________________。
(5)简述检验“滤液”中含有NH4+的实验方法: 。
科目:gzhx 来源:2010年广东省茂名市高考化学二模试卷(解析版) 题型:解答题
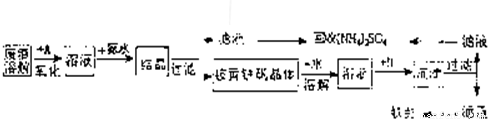


科目:gzhx 来源:模拟题 题型:填空题

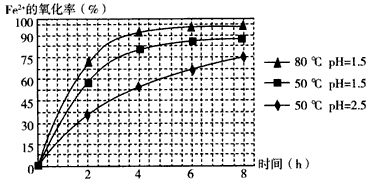
科目:gzhx 来源:茂名二模 题型:问答题



科目:gzhx 来源: 题型:解答题

科目:gzhx 来源: 题型:解答题


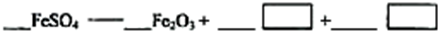
科目:gzhx 来源: 题型:
| A、Na2O2用作呼吸面具的供氧剂 | B、实验室用浓盐酸和MnO2制备Cl2 | C、工业上利用硫酸吸收氨气制备氮肥 | D、自来水厂用ClO2杀菌消毒 |
科目:gzhx 来源:2013届湖南省怀化市高三上学期期末考试化学试卷(带解析) 题型:单选题
下列应用不涉及氧化还原反应的是
| A.Na2O2用作呼吸面具的供氧剂 | B.实验室用浓盐酸和MnO2制备Cl2 |
| C.工业上利用硫酸吸收氨气制备氮肥 | D.自来水厂用C lO2杀菌消毒 |
科目:gzhx 来源:2012-2013学年湖南省怀化市高三上学期期末考试化学试卷(解析版) 题型:选择题
下列应用不涉及氧化还原反应的是
A.Na2O2用作呼吸面具的供氧剂 B.实验室用浓盐酸和MnO2制备Cl2
C.工业上利用硫酸吸收氨气制备氮肥 D.自来水厂用C lO2杀菌消毒
科目:gzhx 来源: 题型:单选题
科目:gzhx 来源:2013-2014学年山东省淄博市高三3月模拟考试理综化学试卷(解析版) 题型:填空题
工业上利用软锰矿(主要成分为MnO2,同时含少量铁、铝等的化合物)制备硫酸锰的常见流程如下:
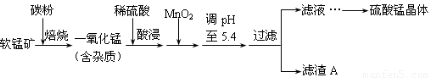
部分金属阳离子以氢氧化物形式完全沉淀时溶液的pH见下表:
沉淀物 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 | Mn(OH)2 |
pH | 5.2 | 3.2 | 9.7 | 10.4 |
(1)一氧化锰用硫酸酸浸时发生的主要反应的离子方程式为____________________。酸浸后加入MnO2将溶液中的Fe2+氧化成Fe3+,其目的是___________。
(2)滤渣A的成分除MnO2外,还有_______________。
(3)MnO2是制造碱性锌锰电池的基本原料,放电时负极的电极反应式为________。工业上以石墨为电极电解酸化的MnSO4溶液生产MnO2,阳极的电极反应式为_________,当阴极产生4.48L(标况)气体时,MnO2的理论产量为______g。
(4)锰的三种难溶化合物的溶度积:Ksp(MnCO3)=1.8×10-11,Ksp[Mn(OH)2]=1.9×10-13,Ksp(MnS)=2.0×10-13,则上述三种难溶物的饱和溶液中,Mn2+浓度由大到小的顺序是_______>_______>_______(填写化学式)。
科目:gzhx 来源: 题型:阅读理解
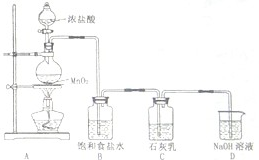 海水占地球总蓄水量的97.2%,若把海水淡化和化工生产结合起来,既可以解决淡水资源缺乏的问题,又可以充分利用海洋资源.
海水占地球总蓄水量的97.2%,若把海水淡化和化工生产结合起来,既可以解决淡水资源缺乏的问题,又可以充分利用海洋资源.
| ||
| ||
| ||
| ||