
题目列表(包括答案和解析)
| ||
| ||
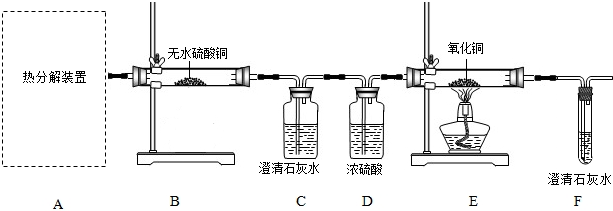
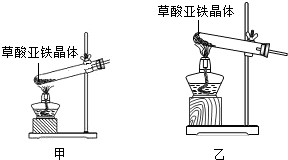
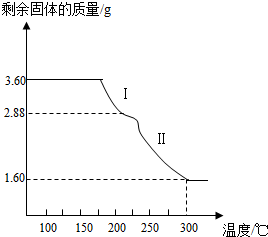
| 钠是一种非常活拨的金属,遇空气中的氧或水等物质均会发生化学反应。工业上给密封状态下电解池中的熔融的NaCl通入直流电,NaCl发生分解得到金属钠和氯气。请完成下列各题: (1)下列二种物质是由什么粒子构成的:钠___________,氯气__________; (2)下列微粒结构示意图各表示的是什么微粒,写出其化学符号: A_________; B_____________; |
 |
| (3)写出工业上电解制钠的化学方程式____________;该过程中钠元素的化合价是怎样变化的?__________; (4)NaCl是由钠离子和氯离了构成的离子化合物。从微观角度分析电解过程中发生的化学变化,并正确推断:钠离子__________变成钠原子,氯原子____________变成氯原子,所以,在电解池中正极(+)上得到的是 _________,负极(-)上得到的是___________。 (5)金属钠敞放在空气中会发生氧化,生成一种名叫过氧化钠的固体。过氧化钠与过氧化氢有类似结构。写出钠氧化的化学方程式__________ 。该反应的基本类型为__________反应。 (6)过氧化钠有如下特性:2Na2O2 + 2CO2 ==2Na2CO3 + O2↑,故过氧化钠可用于潜艇潜航时的制氧剂。该反应是否属于基本类型反应?____________。 |

| ||
| ||
水是宝贵的自然资源,在工农业生产和日常生活中有着极其广泛的应用。
(1)自来水的生产过程大体如下图:
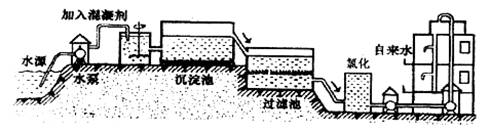
上图过滤池中有活性炭层,该过程中发生 变化。氯化时,通常通入一定量氯气,它与水反应生成盐酸和次氯酸。实验室配制![]() 溶液时不宜使用自来水,其原因是(用化学方程式表示) 。高锰酸钾(
溶液时不宜使用自来水,其原因是(用化学方程式表示) 。高锰酸钾(![]() )是一种理想的水处理剂,高铁酸钾中铁元素的化合价是 。
)是一种理想的水处理剂,高铁酸钾中铁元素的化合价是 。
(2)电解水时,加入少量![]() 可以增强水的导电性。现将0.1g
可以增强水的导电性。现将0.1g![]() 溶解在99.9g水里,接通直流电源后,与电源正极相连的一端放出的气体是 ,当溶液中
溶解在99.9g水里,接通直流电源后,与电源正极相连的一端放出的气体是 ,当溶液中![]() 的质量分数变为0.2%时,有 水被分解。
的质量分数变为0.2%时,有 水被分解。
(3)在河旁有甲、乙、丙、丁四座工厂(位置如右图所示),每个工厂排出的废液只含有![]() 、
、![]() 、
、![]() 、
、![]() 中的一种。某环保小组对河水监测时发现:甲处河水呈无色;乙处河水呈红褐色;丙处河水由浑变清;丁处产生气泡,河水澄清。请回答:
中的一种。某环保小组对河水监测时发现:甲处河水呈无色;乙处河水呈红褐色;丙处河水由浑变清;丁处产生气泡,河水澄清。请回答:
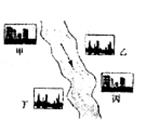
①甲工厂排出的废液是一种碱性物质,检验该物质呈碱性可选用的试剂是 。
②乙处河水呈红褐色的化学方程式是 。
③丁处产生气泡的化学方程式是 。
水是宝贵的自然资源,在工农业生产和日常生活中有着极其广泛的应用。
自来水的生产过程大体如下图

(1)上图过滤池中有活性炭层,活性炭起____作用,该过程中发生________变化。氯化时,通常通入一定量氯气,它与水反应生成盐酸和次氯酸。实验室配制![]() 溶液时不宜使用自来水。其原因是(用化学方程式表示)_____________________。高铁酸钾(
溶液时不宜使用自来水。其原因是(用化学方程式表示)_____________________。高铁酸钾(![]() )是一种理想的水处理剂,高铁酸钾中铁元素的化合价是__________。
)是一种理想的水处理剂,高铁酸钾中铁元素的化合价是__________。
(2)电解水时,加入少量![]() 可以增强水的导电性。现将O.1
可以增强水的导电性。现将O.1![]()
![]() 溶解在99.9
溶解在99.9 ![]() 水里。接通直流电源后,与电源正极相连的一端放出的气体是________,当溶液中
水里。接通直流电源后,与电源正极相连的一端放出的气体是________,当溶液中![]() 的质量分数变为0.2%时,有_______水被分解。
的质量分数变为0.2%时,有_______水被分解。
(3)在河旁有甲、乙、丙、丁四座工厂(位置如下图所示),每个工厂排出的废液含有![]() 、
、![]() 、
、![]() 、
、![]() 中的一种。某环保小组对河水监测时发现:甲处河水呈无色;乙处河水呈红褐色;丙处河水由浑变清;丁处产生气泡,河水澄清。请回答:
中的一种。某环保小组对河水监测时发现:甲处河水呈无色;乙处河水呈红褐色;丙处河水由浑变清;丁处产生气泡,河水澄清。请回答:

①甲工厂排出的废液是一种碱性物质,检验该物质呈碱性可选用的试剂是_____。
②乙处河水呈红褐色的化学方程式是______________
③丁处产生气泡的化学方程式是______________
④保护水资源,我们应该采取的措施是_______________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com