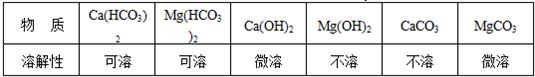
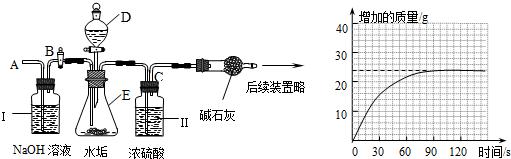
根据下列装置图,按要求回答有关问题:
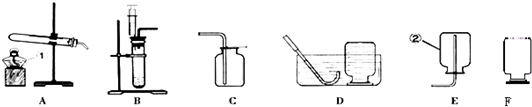
(1)写出图中带有标号仪器的名称:①
酒精灯
酒精灯
、②
集气瓶
集气瓶
.
(2)若实验室用加热氯酸钾制取干燥的氧气,应选用的装置组合为
AC
AC
(填序号),检验氧气已经收集满的方法是
将带火星的小木条放在集气瓶口,若木条复燃则收集满了
将带火星的小木条放在集气瓶口,若木条复燃则收集满了
.
(3)若实验室用过氧化氢溶液制取氧气,应选用的发生装置是
B
B
(填序号),为了加快双氧水的分解速度,一般在试管中加入药品
二氧化锰
二氧化锰
,反应的符号表达式为
.
(4)实验室常用无水醋酸钠和碱石灰的混合固体在加热条件下制取甲烷气体,发生装置可选择
A
A
(填序号).甲烷气体一般采用装置D进行收集,收集满后集气瓶的放置方式如图F所示,据此可推断甲烷一定具备的物理性质是:
难溶于水
难溶于水
、
密度比空气小
密度比空气小
.
(5)小元同学准确称取7.9g纯净的高锰酸钾加热制取氧气,他在试管口放一团棉花,其作用是
防止高锰酸钾粉末冲出,进入导管
防止高锰酸钾粉末冲出,进入导管
;用排水法收集氧气的合适时机是
气泡连续均匀冒出时
气泡连续均匀冒出时
;实验结束后,他收集到氧气580mL(标准状况).
意外发现:根据计算,7.9g高锰酸钾完全分解,应生成氧气560mL(标准状况).小元通过数据分析,意外发现收集到的氧气体积和理论计算的氧气体积不相符合,并且在实验中还意外发现锰酸钾能溶于水,二氧化锰不溶于水.
提出假设:小元取实验后的少量固体残渣再次加热,经检验又产生了氧气.根据小元发现的问题和上述实验结果可以做出如下假设:
假设1:二氧化锰也可以受热分解产生氧气;假设2:锰酸钾也可以受热分解产生氧气
假设3:
二氧化锰和锰酸钾都可以分解产生氧气
二氧化锰和锰酸钾都可以分解产生氧气
(只填一种)
设计实验:小元用最初加热所得的残渣及必要的实验用品,设计了如下实验流程验证假设2.请在下面实验流程方框中的相应位置填写各步骤的实验操作名称.

请简要叙述步骤5的操作
取少量干燥后的固体于试管中充分加热,再将带火星的小
木条伸入试管中
取少量干燥后的固体于试管中充分加热,再将带火星的小
木条伸入试管中
.
得出结论:若观察到
带火星木条复燃
带火星木条复燃
,则假设2成立.