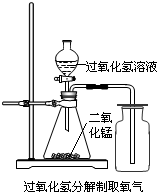
(2004?北碚区)实验室中,常采用分解过氧化氢溶液(二氧化锰作催化剂)或加热高锰酸钾的方法制取氧气.
(1)写出用上述两种方法分别制取氧气的化学反应方程式:
、
.
(2)用过氧化氢分解制取氧气的装置如图所示:
图中收集氧气的方法叫做
向上排空气法
向上排空气法
.可用此方法收集氧气的原因是
O2的密度比空气密度略大
O2的密度比空气密度略大
(3)用该方法收集氧气时,检验集气瓶中氧气是否集满的方法是
C
C
.
A.把点燃的木条伸入瓶内
B.把带火星的木条伸人瓶内
C.把带火星的木条放在瓶口
(4)如果锥形瓶中的反应很剧烈,应该采取的安全措施是
①
①
(填编号).
①减慢液体滴加的速度 ②换用体积较小的锥形瓶 ③加热锥形瓶
(5)请计算,制取3.2g氧气,理论上需高锰酸钾的质量为
31.6
31.6
g;需质量分数为30%过氧化氢溶液的质量为
22.7
22.7
g.
(6)某化学试剂公司报价:高锰酸钾30.50元/kg,30%过氧化氢溶液21.70元/kg.请从实验操作和生产成本两方面考虑,用
分解过氧化氢
分解过氧化氢
方法制取氧气更好(二氧化锰价格低、耗量少,忽略不计).这种方法的主要优点是
①实验室用H2O2制取02不需加热,②制取相同质量(3.2g)O2时购买H2O2(约0.49元)比KMnO4(约0.96元)价格低
①实验室用H2O2制取02不需加热,②制取相同质量(3.2g)O2时购买H2O2(约0.49元)比KMnO4(约0.96元)价格低
.

 (2004?北碚区)实验室中,常采用分解过氧化氢溶液(二氧化锰作催化剂)或加热高锰酸钾的方法制取氧气.
(2004?北碚区)实验室中,常采用分解过氧化氢溶液(二氧化锰作催化剂)或加热高锰酸钾的方法制取氧气. 实验室常采用分解过氧化氢溶液(二氧化锰作催化剂)的方法制取氧气,如图所示.
实验室常采用分解过氧化氢溶液(二氧化锰作催化剂)的方法制取氧气,如图所示.
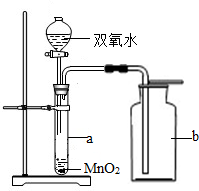 实验室中常采用分解过氧化氢(H2O2)溶液(用二氧化锰作催化剂)或加热高锰酸钾的方法制取氧气.请回答下列问题:
实验室中常采用分解过氧化氢(H2O2)溶液(用二氧化锰作催化剂)或加热高锰酸钾的方法制取氧气.请回答下列问题: 实验室中常采用分解过氧化氢溶液(二氧化锰作催化剂)或加热高锰酸钾的方法制取氧气.
实验室中常采用分解过氧化氢溶液(二氧化锰作催化剂)或加热高锰酸钾的方法制取氧气.