
题目列表(包括答案和解析)

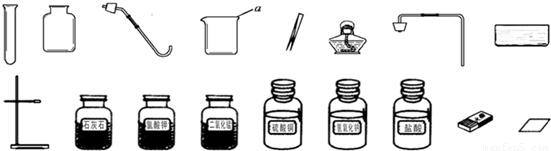
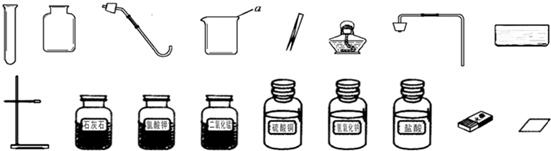
 表示氯原子
表示氯原子 表示钠原子
表示钠原子 表示氧原子
表示氧原子
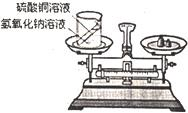 24、在学习了质量守恒定律后,小明和小华来到实验室,他们用右图所示的实验装置,验证了氢氧化钠溶液和硫酸铜溶液反应是符合质量守恒定律的.
24、在学习了质量守恒定律后,小明和小华来到实验室,他们用右图所示的实验装置,验证了氢氧化钠溶液和硫酸铜溶液反应是符合质量守恒定律的.| 阳离子\阴离子 | SO42- | N03- | PO43- | Cl- | C032- |
| Cu2+ | 溶 | 溶 | 不 | 溶 | 不 |
| 实验过程 | 实验现象 | 结论 |
向氢氧化钠溶液中滴加盐酸(或稀硫酸) |
有气泡产生 |
变质 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com