
题目列表(包括答案和解析)
小明和小华进入盐酸与锌反应制取氢气的实验研究。小明用较稀的盐酸,小华用较浓的盐酸。他们分别取等质量的锌粒与足量盐酸在烧杯中反应,并将烧杯中物质总质量随反应时间的变化情况绘制成右图。
试回答下列问题:
(1)烧杯中物质总质量减小的原因是 ;
(2)表示小明实验结果的是图中的曲线 (①或②);
(3)请说明图中的曲线②与曲线①不同的原因是 。
| ||
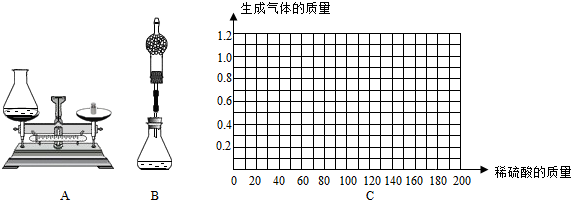
| 样品 | 第1份 | 第2份 | 第3份 | 第4份 |
| 取样品质量(g) | 50.0 | 50.0 | 50.0 | 50.0 |
| 取稀硫酸质量(g) | 40.0 | 80.0 | 120.0 | 160.0 |
| 产生气体质量(g) | 0.4 | 0.8 | 1.0 | 1.0 |
 Ti+2MgCl2.该反应说明金属钛的活动性比镁______(填“强”或“弱”).
Ti+2MgCl2.该反应说明金属钛的活动性比镁______(填“强”或“弱”).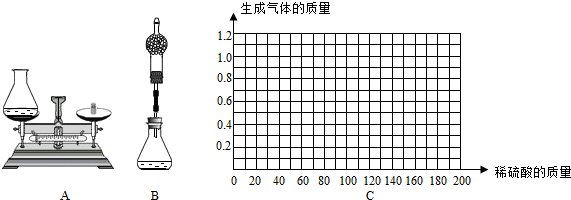
| 样品 | 第1份 | 第2份 | 第3份 | 第4份 |
| 取样品质量(g) | 50.0 | 50.0 | 50.0 | 50.0 |
| 取稀硫酸质量(g) | 40.0 | 80.0 | 120.0 | 160.0 |
| 产生气体质量(g) | 0.4 | 0.8 | 1.0 | 1.0 |
 Ti+2MgCl2。该反应说明金属钛的活动性比镁 (填“强”或“弱”)。
Ti+2MgCl2。该反应说明金属钛的活动性比镁 (填“强”或“弱”)。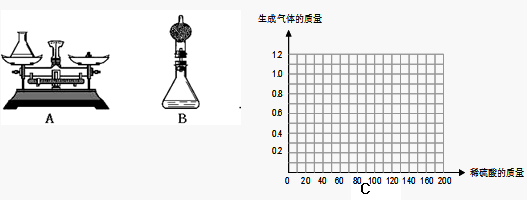
 质量差。请你说明小海进行改进的理由是: 。
质量差。请你说明小海进行改进的理由是: 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com