
题目列表(包括答案和解析)
(1)将2.0 mol/L CuSO4溶液和1.0 mol/L H2SO4溶液等体积混合(假设混合前后溶液体积不发生变化),所得混合液中C(CuSO4)= mol/L,C(SO42-)= mol/L。
(2)往100 mL 2 mol/L 的AlCl3溶液中逐滴加入 NaOH 溶液 100 mL 时,产生沉淀为7.8 g。试求所加 NaOH 溶液的物质的量浓度。
(1)将2.0 mol/L CuSO4溶液和1.0 mol/L H2SO4溶液等体积混合(假设混合前后溶液体积不发生变化),所得混合液中C(CuSO4)= mol/L,C(SO42-)= mol/L。
(2)往100 mL 2 mol/L 的AlCl3溶液中逐滴加入 NaOH 溶液 100 mL 时,产生沉淀为7.8 g。试求所加 NaOH 溶液的物质的量浓度。
某研究小组将一批废弃的线路板经浓硝酸和稀硫酸处理后得到一混合溶液,其中含有Cu2+、Fe2+、Fe3+、Al3+等金属离子,并设计了以下两种流程以分别制取CuSO4·5H2O晶体和AlCl3
溶液: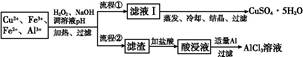
已知:相关金属离子开始沉淀至完全沉淀时的pH范围为:
| 离子 | Fe3+ | Fe2+ | Al3+ | Cu2+ |
| pH范围 | 2.2~3.2 | 5.5~9.0 | 4.1~5.0 | 5.3~6.6 |
某研究小组将一批废弃的线路板经浓硝酸和稀硫酸处理后得到一混合溶液,其中含有Cu2+、Fe2+、Fe3+、Al3+等金属离子,并设计了以下两种流程以分别制取CuSO4·5H2O晶体和AlCl3
溶液:
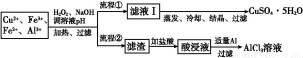
已知:相关金属离子开始沉淀至完全沉淀时的pH范围为:
离子 | Fe3+ | Fe2+ | Al3+ | Cu2+ |
pH范围 | 2.2~3.2 | 5.5~9.0 | 4.1~5.0 | 5.3~6.6 |
请回答下列问题:
(1)加入H2O2的作用是 ,欲使制取的CuSO4·5H2O晶体较为纯净,pH至少应调至 。
(2)写出H2O2与Fe2+反应的离子方程式: 。
(3)流程②中加入适量Al粉起的作用是 。
(4)根据你所学的化学知识,由AlCl3溶液(不添加其他化学试剂)能否制得无水AlCl3 (填“能”或“不能”),原因是 。
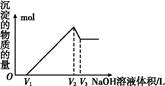
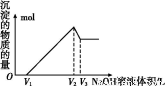
(5)取体积为V(L)的酸浸液,向其中滴加a mol·L-1的NaOH溶液,生成沉淀的物质的量与所加的NaOH溶液的体积(L)关系如图。请用V1、V2、V3表示所取的酸浸液中n(Fe3+)∶n(Al3+)= 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com