(2012?西城区二模)某小组同学欲探究NH
3催化氧化反应,按图1装置进行实验.
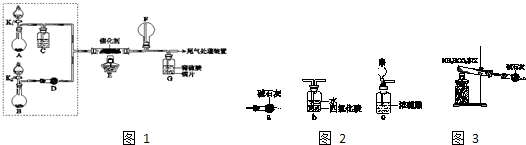
A、B装置可选药品:浓氨水、H
2O
2、蒸馏水、NaOH固体、MnO
2(1)NH
3催化氧化的化学方程式是
.
(2)装置B中产生气体的原因有(结合化学用语解释)
在氨水中存在平衡:NH3+H2O?NH3?H2O?NH4++OH-,加入NaOH固体,OH-浓度增加,平衡向左移动,NaOH固体溶于水放出大量热,均有利于NH3逸出
在氨水中存在平衡:NH3+H2O?NH3?H2O?NH4++OH-,加入NaOH固体,OH-浓度增加,平衡向左移动,NaOH固体溶于水放出大量热,均有利于NH3逸出
.
(3)甲乙两同学分别按上述装置进行实验.一段时间后,装置G中溶液都变成蓝色.
①甲观察到装置F中有红棕色气体,生成红棕色气体的化学方程式是
2NO+O2═2NO2
2NO+O2═2NO2
.
②乙观察到装置F中只有白烟生成,白烟的成分是(写化学式)
NH4NO3
NH4NO3
.
③用离子方程式解释装置G中溶液变成蓝色的原因:
3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O
3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O
.
(4)如图2,为帮助乙实现在装置F中也观察到红棕色气体,可在原实验的基础上进行改进.
①甲认为可调节K
1和K
2控制A、B装置中的产气量,应(填“增加”或“减少”)
增加
增加
装置A中的产气量,或(填“增加”或“减少”)
减少
减少
装置B中的产气量.
②乙认为可在装置E、F间增加一个装置,该装置可以是(填序号)
abc
abc
.
(5)为实现该反应,也可用图3所示的装置替换上述
装置中虚线框部分,化合物X为
Na2O2
Na2O2
. NH
4HCO
3的作用是
NH4HCO3分解放出NH3;同时放出的CO2和H2O与Na2O2反应生成O2
NH4HCO3分解放出NH3;同时放出的CO2和H2O与Na2O2反应生成O2
.

 4NO + 6H2O ,其中作为还原剂的物质是 (填化学式);若反应中生成了0.2 mol NO,则转移 mol电子,
4NO + 6H2O ,其中作为还原剂的物质是 (填化学式);若反应中生成了0.2 mol NO,则转移 mol电子, 4NO + 6H2O ,其中作为还原剂的物质是 (填化学式);若反应中生成了0.2 mol NO,则转移 mol电子,
4NO + 6H2O ,其中作为还原剂的物质是 (填化学式);若反应中生成了0.2 mol NO,则转移 mol电子, (2013?日照二模)CO、NO、NO2、SO2等都是污染大气的有害气体,对其进行回收利用是节能减排的重要课题.
(2013?日照二模)CO、NO、NO2、SO2等都是污染大气的有害气体,对其进行回收利用是节能减排的重要课题.

