
题目列表(包括答案和解析)
| 第1份 | 第2份 | 第3份 | 第4份 | |
| 加入BaCl2 溶液的质量/g | 15 | 20 | 25 | 30 |
| 反应得到的沉淀的质量/g | 1.398 | 1.864 | 2.330 | 2.330 |

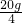 ×ω 10g×10%
×ω 10g×10% CaO+CO2↑,这一化学反应要________(填“产生”或“吸收”)热量.
CaO+CO2↑,这一化学反应要________(填“产生”或“吸收”)热量.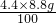
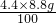 8.8g
8.8g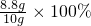 =88%
=88%解:氧气的质量是:34g+2g-34.4g=1.6g 1分
设反应的过氧化氢的质量为X
![]() 1分
1分
68 32
x 1.6g
![]() ……1分
……1分
![]()
=3.4g……1分
![]()
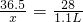
 K2MnO4+MnO2+O2↑
K2MnO4+MnO2+O2↑ 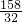 =
=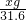
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com