
ƒø¡–±Ì(∞¸¿®¥∞∏∫ÕΩ‚Œˆ)
£®12∑÷£©
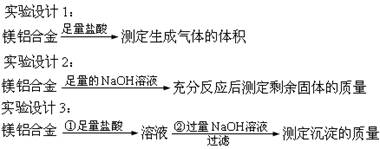
∫¨√æ3£•£≠5£•µƒ√次∫œΩ£¨œ÷“—≥…Œ™¬÷¥¨÷∆‘Ï°¢ªØπ§…˙≤˙°¢ª˙–µ÷∆‘ϵ»––“µµƒ÷ÿ“™‘≠≤ƒ¡œ°£œ÷”–“ªøÈ“—÷™÷ ¡øµƒ√次∫œΩ£¨”˚≤‚∂®∆‰÷–√浃÷ ¡ø∑÷ ˝£¨º∏ŒªÕ¨—߅˺∆¡À“‘œ¬»˝÷÷≤ªÕ¨µƒ µ—È∑Ω∞∏£∫
ªÿ¥œ¬¡–Œ £∫
£®1£©…œ ˆ∑Ω∞∏÷–£¨ƒÐ≤‚≥ˆMgµƒ÷ ¡ø∑÷ ˝µƒ∑Ω∞∏ « £®ÃÓ–¥¥˙∫≈£¨œ¬Õ¨£©
A£Æ µ—ȅ˺∆1 B£Æ µ—ȅ˺∆2 C£Æ µ—ȅ˺∆3 D£Æ∂ºø…“‘
£®2£©…œ ˆ∑Ω∞∏÷–µƒªØ—ß∑¥”¶ÃÂœ÷¡ÀMg°¢Alµƒ–‘÷ «
A£Æ—ıªØ–‘ B£Æªπ‘≠–‘ C£ÆÀ·–‘ D£ÆºÓ–‘
£®3£©ƒ≥Õ¨—߅˺∆¡À”“Õº◊∞÷√°£∏√◊∞÷√ ∫œµƒ µ—ȅ˺∆ « 

”√∏√◊∞÷√≤‚∂®√次∫œΩ÷–√浃÷ ¡ø∑÷ ˝£¨À˘–˵ƒ µ—È≤Ÿ◊˜ «
°£
A£Æ”√≈≈ÀÆ∑®≤‚∂®H2µƒÃª˝
B£Æ∑¥”¶Ω· ¯∫Û£¨π˝¬À°¢œ¥µ”°¢∏…‘Ô°¢≥∆¡ø≤–‘¸µƒ÷ ¡ø
C£Æ≥∆¡ø∑¥”¶«∞∫Û£¨◊∞÷√∫Õ“©∆∑µƒ◊Ð÷ ¡ø
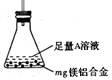
£®4£©»Ù∞¥ µ—ȅ˺∆3Ω¯–– µ—È°£Ω´m g√次∫œΩ£¨»Ð”⁄π˝¡ø—ŒÀ·÷–£¨‘Ÿº”»Îπ˝¡øµƒNaOH»Ð“∫£¨ø…µ√µΩ∞◊…´≥¡µÌ£¨∏√≥¡µÌŒÔ÷ « £®ÃÓªØ—ß Ω£©£ªΩ´¥À≥¡µÌœ¥æª°¢∏…‘Ô∫Û£¨≥∆µ√÷ ¡øŒ™w g°£«Û∫œΩ÷–√浃÷ ¡ø∑÷ ˝ £ª

£®12∑÷£©
∫¨√æ3£•£≠5£•µƒ√次∫œΩ£¨œ÷“—≥…Œ™¬÷¥¨÷∆‘Ï°¢ªØπ§…˙≤˙°¢ª˙–µ÷∆‘ϵ»––“µµƒ÷ÿ“™‘≠≤ƒ¡œ°£œ÷”–“ªøÈ“—÷™÷ ¡øµƒ√次∫œΩ£¨”˚≤‚∂®∆‰÷–√浃÷ ¡ø∑÷ ˝£¨º∏ŒªÕ¨—߅˺∆¡À“‘œ¬»˝÷÷≤ªÕ¨µƒ µ—È∑Ω∞∏£∫
ªÿ¥œ¬¡–Œ £∫
£®1£©…œ ˆ∑Ω∞∏÷–£¨ƒÐ≤‚≥ˆMgµƒ÷ ¡ø∑÷ ˝µƒ∑Ω∞∏ « £®ÃÓ–¥¥˙∫≈£¨œ¬Õ¨£©
A£Æ µ—ȅ˺∆1 B£Æ µ—ȅ˺∆2 C£Æ µ—ȅ˺∆3 D£Æ∂ºø…“‘
£®2£©…œ ˆ∑Ω∞∏÷–µƒªØ—ß∑¥”¶ÃÂœ÷¡ÀMg°¢Alµƒ–‘÷ «
A£Æ—ıªØ–‘ B£Æªπ‘≠–‘ C£ÆÀ·–‘ D£ÆºÓ–‘
£®3£©ƒ≥Õ¨—߅˺∆¡À”“Õº◊∞÷√°£∏√◊∞÷√ ∫œµƒ µ—ȅ˺∆ «
A£Æ µ—ȅ˺∆1 B£Æ µ—ȅ˺∆2 C£Æ µ—ȅ˺∆3
”√∏√◊∞÷√≤‚∂®√次∫œΩ÷–√浃÷ ¡ø∑÷ ˝£¨À˘–˵ƒ µ—È≤Ÿ◊˜ «
°£
A£Æ”√≈≈ÀÆ∑®≤‚∂®H2µƒÃª˝
B£Æ∑¥”¶Ω· ¯∫Û£¨π˝¬À°¢œ¥µ”°¢∏…‘Ô°¢≥∆¡ø≤–‘¸µƒ÷ ¡ø
C£Æ≥∆¡ø∑¥”¶«∞∫Û£¨◊∞÷√∫Õ“©∆∑µƒ◊Ð÷ ¡ø
£®4£©»Ù∞¥ µ—ȅ˺∆3Ω¯–– µ—È°£Ω´m g√次∫œΩ£¨»Ð”⁄π˝¡ø—ŒÀ·÷–£¨‘Ÿº”»Îπ˝¡øµƒNaOH»Ð“∫£¨ø…µ√µΩ∞◊…´≥¡µÌ£¨∏√≥¡µÌŒÔ÷ « £®ÃÓªØ—ß Ω£©£ªΩ´¥À≥¡µÌœ¥æª°¢∏…‘Ô∫Û£¨≥∆µ√÷ ¡øŒ™w g°£«Û∫œΩ÷–√浃÷ ¡ø∑÷ ˝ £ª
£®12∑÷£©
∫¨√æ3£•£≠5£•µƒ√次∫œΩ£¨œ÷“—≥…Œ™¬÷¥¨÷∆‘Ï°¢ªØπ§…˙≤˙°¢ª˙–µ÷∆‘ϵ»––“µµƒ÷ÿ“™‘≠≤ƒ¡œ°£œ÷”–“ªøÈ“—÷™÷ ¡øµƒ√次∫œΩ£¨”˚≤‚∂®∆‰÷–√浃÷ ¡ø∑÷ ˝£¨º∏ŒªÕ¨—߅˺∆¡À“‘œ¬»˝÷÷≤ªÕ¨µƒ µ—È∑Ω∞∏£∫

ªÿ¥œ¬¡–Œ £∫
£®1£©…œ ˆ∑Ω∞∏÷–£¨ƒÐ≤‚≥ˆMgµƒ÷ ¡ø∑÷ ˝µƒ∑Ω∞∏ « £®ÃÓ–¥¥˙∫≈£¨œ¬Õ¨£©
A£Æ µ—ȅ˺∆1 B£Æ µ—ȅ˺∆2 C£Æ µ—ȅ˺∆3 D£Æ∂ºø…“‘
£®2£©…œ ˆ∑Ω∞∏÷–µƒªØ—ß∑¥”¶ÃÂœ÷¡ÀMg°¢Alµƒ–‘÷ «
A£Æ—ıªØ–‘ B£Æªπ‘≠–‘ C£ÆÀ·–‘ D£ÆºÓ–‘
£®3£©ƒ≥Õ¨—߅˺∆¡À”“Õº◊∞÷√°£∏√◊∞÷√ ∫œµƒ µ—ȅ˺∆ «

A£Æ µ—ȅ˺∆1 B£Æ µ—ȅ˺∆2 C£Æ µ—ȅ˺∆3
”√∏√◊∞÷√≤‚∂®√次∫œΩ÷–√浃÷ ¡ø∑÷ ˝£¨À˘–˵ƒ µ—È≤Ÿ◊˜ «
°£
A£Æ”√≈≈ÀÆ∑®≤‚∂®H2µƒÃª˝
B£Æ∑¥”¶Ω· ¯∫Û£¨π˝¬À°¢œ¥µ”°¢∏…‘Ô°¢≥∆¡ø≤–‘¸µƒ÷ ¡ø
C£Æ≥∆¡ø∑¥”¶«∞∫Û£¨◊∞÷√∫Õ“©∆∑µƒ◊Ð÷ ¡ø
£®4£©»Ù∞¥ µ—ȅ˺∆3Ω¯–– µ—È°£Ω´m g√次∫œΩ£¨»Ð”⁄π˝¡ø—ŒÀ·÷–£¨‘Ÿº”»Îπ˝¡øµƒNaOH»Ð“∫£¨ø…µ√µΩ∞◊…´≥¡µÌ£¨∏√≥¡µÌŒÔ÷ « £®ÃÓªØ—ß Ω£©£ªΩ´¥À≥¡µÌœ¥æª°¢∏…‘Ô∫Û£¨≥∆µ√÷ ¡øŒ™w g°£«Û∫œΩ÷–√浃÷ ¡ø∑÷ ˝ £ª
£®15∑÷£©ƒø«∞£¨»´ ¿ΩÁµƒƒ¯œ˚∑—¡øΩˆ¥Œ”⁄Õ≠°¢¬¡°¢«¶°¢–ø£¨æ””–…´Ω Ùµ⁄ŒÂŒª°£ƒ¯––“µ∑¢’π‘Ã≤ÿ◊≈æÞ¥Ûµƒ«±¡¶°£ƒ¯ªØ∫œŒÔ÷–µƒ»˝—ıªØ∂˛ƒ¯ «“ª÷÷÷ÿ“™µƒµÁ◊”‘™º˛≤ƒ¡œ∫Õ∂˛¥ŒµÁ≥ÿ≤ƒ¡œ°£π§“µ…œø…¿˚”√∫¨ƒ¯∫œΩ∑œ¡œ£®≥˝ƒ¯Õ‚£¨ªπ∫¨”–Fe°¢Cu°¢Ca°¢Mg°¢Cµ»‘”÷ £©÷∆»°≤ðÀ·ƒ¯£¨»ª∫Û∏þŒ¬Ï—…’≤ðÀ·ƒ¯¿¥÷∆»°»˝—ıªØ∂˛ƒ¯°£
“—÷™£∫¢Ÿ≤ðÀ·µƒ∏∆°¢√æ°¢ƒ¯—Œæ˘ƒ—»Ð”⁄ÀÆ£¨«“»ÐΩ‚∂»£∫NiC2O4> NiC2O4°§H2O> NiC2O4°§2H2O
¢⁄≥£Œ¬œ¬£¨Ksp[(Fe(OH))3]=4.0°¡10-38,lg5=0.7
∏˘æ𜬡–𧓒¡˜≥ÃÕºªÿ¥Œ £∫
£®1£©º”6%µƒH2O2 ±£¨Œ¬∂»≤ªƒÐô∏þ£¨∆‰ƒøµƒ « °£»ÙH2O2‘⁄“ªø™ ºÀ·»Ð ±±„”ΗŒÀ·“ª∆º”»Î£¨ª·‘Ï≥…À·»Ðπ˝¬À∫Ûµƒ¬À“∫÷–‘ˆº”“ª÷÷Ω Ù¿Î◊”£¨”√¿Î◊”∑Ω≥Ã Ω±Ì æ’‚“ª«Èøˆ °£
£®2£©¡˜≥Ã÷–”–“ª≤Ω «µ˜pH£¨ πFe3+◊™ªØŒ™Fe(OH)3≥¡µÌ£¨≥£Œ¬œ¬µ±»Ð“∫÷–c (Fe3+)=0.5°¡10-5mol/L ±£¨»Ð“∫µƒpH= °£
£®3£©¡˜≥Ã÷–º”»ÎNH4Fµƒƒøµƒ « °£
£®4£©Ω´◊Ó∫ÛÀ˘µ√µƒ≤ðÀ·ƒ¯æßÑ⁄ø’∆¯÷–«ø»»µΩ400°Ê£¨ø……˙≥…»˝—ıªØ∂˛ƒ¯∫ÕŒÞ∂æ∆¯Ã£¨–¥≥ˆ∏√∑¥”¶µƒªØ—ß∑Ω≥Ã Ω °£
£®5£©π§“µ…œªπø…”√µÁΩ‚∑®÷∆»°»˝—ıªØ∂˛ƒ¯£¨”√NaOH»Ð“∫µ˜Ω⁄NiCl2»Ð“∫µƒpH÷¡7.5£¨‘Ÿº”»Î ¡øNa2SO4Ω¯––µÁΩ‚£¨µÁΩ‚≤˙…˙µƒCl2∆‰80%µƒø…Ω´∂˛º€ƒ¯—ıªØŒ™»˝º€ƒ¯°£–¥≥ˆCl2—ıªØNi(OH)2…˙≥…»˝—ıªØ∂˛ƒ¯µƒ¿Î◊”∑Ω≥Ã Ω £ªΩ´amol∂˛º€ƒ¯»´≤ø◊™ªØŒ™»˝º€ƒ¯ ±£¨Õ‚µÁ¬∑÷–Õ®π˝µÁ◊”µƒŒÔ÷ µƒ¡ø « °£
£®6£©Ω¸ƒÍ¿¥ƒ¯«‚µÁ≥ÿ∑¢’π∫ÐøÏ£¨À¸ø…”…NiO(OH)∏˙LaNi5H6(LaNi5H6÷–∏˜‘™ÀÿªØ∫œº€æ˘ø…ø¥◊˜ «¡„)◊È≥…£∫6NiO(OH)+LaNi5H6 LaNi5+6Ni(OH)2°£∏√µÁ≥ÿ∑≈µÁ ±£¨∏∫º´∑¥”¶ « °£
LaNi5+6Ni(OH)2°£∏√µÁ≥ÿ∑≈µÁ ±£¨∏∫º´∑¥”¶ « °£
π˙º —ß–£”≈—° - ¡∑œ∞≤·¡–±Ì - ‘¡–±Ì
∫˛±± °ª•¡™Õ¯Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®∆Ωî | Õ¯…œ”–∫¶–≈œ¢æŸ±®◊®«¯ | µÁ–≈’©∆≠柱®◊®«¯ | …Ê¿˙ ∑–ÈŒÞ÷˜“”–∫¶–≈œ¢æŸ±®◊®«¯ | …Ê∆Û«÷»®æŸ±®◊®«¯
Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®µÁª∞£∫027-86699610 柱®” œ‰£∫58377363@163.com