
题目列表(包括答案和解析)


下列叙述是某同学做完铜一锌一硫酸原电池的实验后得出的结论和认识,你认为正确的是
A.构成原电池正极和负极的材料必须是两种金属
B.在该原电池中,铜作负极
C.铜锌原电池工作时,若有13g锌溶解,则电路中就有0.4moI电子通过
D.电子通过硫酸溶液由锌流向铜,在铜电极上被氢离子得到而放出氢气
迄今为止,由化学能转变的热能或电能仍然是人类使用的主要的能源。
I.请仔细观察下列两种电池的构造示意图,完成下列问题:
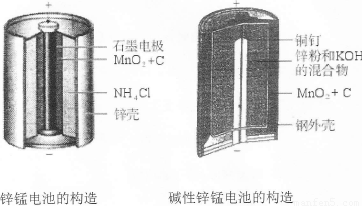
(1)碱性锌锰电池比普通锌锰电池(干电池)性能好,放电电流大。试从影响反应速率的因素分析其原因是 。
(2)碱性锌锰电池的总反应式:Zn+2MnO2+2H2O=2MnOOH+Zn(OH)2,则负极的电极反应式为 。
Ⅱ.下面是一个将化学能与电能相互转化的装置。回答下列问题:
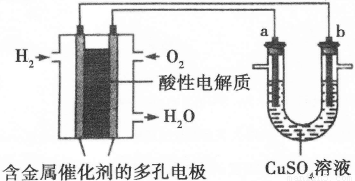
(1)写出通入O2一极的电极反应方程式为 。
(2)a电极是 极,能否写出其电极反应方程式 (填“能”或“不能”),若“能”写出其电极反应方程式,若“不能”说明其理由 。
(3)下列说法不正确的是( )
A.此装置用于电镀铜时,电解一段时间,硫酸铜溶液的浓度不变
B.U型管中,OH—在a极放电
C.若a为纯净金属,b为粗制金属,该装置可用于粗制金属的精炼
D.电子经导线流入b电极
Ⅲ.某同学运用所学知识,自选材料设计实验,实现了在通常条件下不能发生的反应:Cu+H2SO4(稀)=CuSO4+H2↑。请在下面框中画出能够实验这一反应的装置图,并在图中进行必要的标注。

下列是某同学对某些概念的理解和判断,下列各判断或说法正确的是 ( )
A.胶体:分散质颗粒直径在1nm ~ 100nm之间的分散系,能产生丁达尔现象
B.氧化反应:元素化合价在反应后升高
C.酸性氧化物:与水反应生成酸的物质
D.物质的量:衡量物质微粒个数的单位
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com