
题目列表(包括答案和解析)
(1)目前上海大部分城市居民所使用的燃料主要是管道煤气,浦东新区居民开始使用东海天然气作为民用燃料。管道煤气的主要成分是CO、H2和少量烃类,天然气的主要成分是CH4。它们的燃烧反应如下:
2CO+O2![]() 2CO2 2H2+O2
2CO2 2H2+O2![]() 2H2O CH4+2O2
2H2O CH4+2O2![]() CO2+2H2O
CO2+2H2O
根据以上化学方程式判断:燃烧相同体积的管道煤气和天然气,消耗空气体积较大的是____________。因此燃烧管道煤气的灶具如需改烧天然气,灶具的改进方法是______________进风口(填“增大”或“减小”),如不作改进可能产生的不良结果是________________________。
(2)管道煤气中含有的烃类,除甲烷外,还有少量乙烷、丙烷、丁烷等,它们的某些性质见下表:
| 乙烷 | 丙烷 | 丁烷 |
熔点/℃ | -183.3 | -189.7 | -138.4 |
沸点/℃ | -88.6 | -42.1 | -0.5 |
试根据以上某个关键数据解释冬天严寒的季节有时管道煤气火焰很小,并且呈断续状态的原因是_____________________________________________________________________。
目前上海大部分城市居民所使用的燃料主要是管道煤气,浦东新区居民开始使用东海天然气作为民用燃料。管道煤气的主要成分是CO、H2和少量烃类,天然气的主要成分是CH4。它们的燃烧反应如下:
2CO+O2![]() 2CO2 2H2+O2
2CO2 2H2+O2![]() 2H2O CH4+2O2
2H2O CH4+2O2![]() CO2+2H2O
CO2+2H2O
根据以上化学方程式判断:
(1)燃烧相同体积的管道煤气和天然气,消耗空气体积较大的是________。因此燃烧管道煤气的灶具如需改烧天然气,灶具的改进方法是________进风口(填“增大”或“减小”),如不作改进可能产生的不良结果是________________。
(2)管道煤气中含有的烃类,除甲烷外,还有少量乙烷、丙烷、丁烷等,它们的某些性质见下表:
| 乙烷 | 丙烷 | 丁烷 |
熔点(℃) | -183.3 | -189.7 | -138.4 |
沸点(℃) | -88.6 | -42.1 | -0.5 |
试根据以上某个关键数据解释冬天严寒的季节有时管道煤气火焰很小,并且呈断续状态的原因是____________________________________________________________。
A.2Al+2NaOH+6H2O![]() 2Na[Al(OH)4]+3H2↑
2Na[Al(OH)4]+3H2↑
B.2H2+O2![]() 2H2O
2H2O
C.Mg3N2+6H2O![]() 3Mg(OH)2+2NH3↑
3Mg(OH)2+2NH3↑
D.CH4+2O2![]() CO2+2H2O
CO2+2H2O
化学反应在工农业生产中有着重要的应用。按要求回答下列问题:
(1)利用化学反应可以制备许多物质。
①实验室用铜制备NO的离子方程式为___________________。
②可用Al和Fe2O3制Fe,该反应的化学方程式为___________________。
③海水提溴过程中,向浓缩的海水中通入氯气,再用热空气吹出生成的溴,然后用碳酸钠溶液吸收溴,溴歧化为Br-和BrO3-。这两步反应的离子方程式分别为__________、___________。
(2)化学反应能为人类生产生活提供能源。
①由反应CH4
+2O2 CO2
+2H2O,可以设计出以NaOH溶液为电解质溶液的燃料电池,该电池工作时负极的电极反应式为:______________。
CO2
+2H2O,可以设计出以NaOH溶液为电解质溶液的燃料电池,该电池工作时负极的电极反应式为:______________。
②2011年山东高考化学中曾提到钠硫高能电池,右图是该电池的结构示意图,该电池的工作温度为320℃左右,电池反应为2Na+xS=Na2Sx。该电池负极为________(填化学式),正极的电极反应式为 。用该电池作电源进行粗铜精炼时,当得到64g精铜时,理论上该电池负极消耗的质量为_____g。

(10分,每空2分)现有反应:①CO+CuO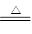 Cu+CO2 ②MgO+2HCl====MgCl2+H2O
Cu+CO2 ②MgO+2HCl====MgCl2+H2O
③Fe+2AgNO3====2Ag+Fe(NO3)2 ④CH4+2O2 CO2+2H2O
CO2+2H2O
⑤NH4HCO3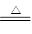 NH3↑+CO2↑+H2O
NH3↑+CO2↑+H2O
试完成:
(1)上述反应中属于置换反应的有_____________。属于复分解反应的有_____________。
(2)属于氧化还原反应的有_____________。
(3)反应③中被还原的元素是_____________。反应④中被氧化的元素是_____________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com