
题目列表(包括答案和解析)
| A、溶解度(S) | B、摩尔质量(M) | C、物质的量浓度(c) | D、溶质的质量分数(w) |
(Ⅰ)实验目的:研究铁与浓硫酸的反应
(Ⅱ)实验药品:铁钉(表面无铁锈)、浓硫酸、酸性高锰酸钾溶液、品红溶液、氧化铜、硫酸铜溶液
(Ⅲ)实验装置(按从左到右的方向将A装置与B等装置相连):
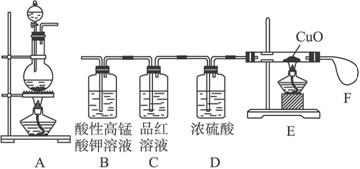
(Ⅳ)实验步骤(请将表中空格补充完整):
实验内容和步骤 | 实验现象 | 结论 |
①连接好装置,检查装置的气密性 |
|
|
②将铁钉加入到烧瓶中,再向其中滴加浓硫酸 | 未见明显现象 | 原因为: ______________ |
③点燃A、E处酒精灯 | 片刻后,烧瓶中溶液有颜色变化,并有气泡产生烧瓶中产生 | 气体的化学方程式为:_____________________ |
(Ⅴ)反思评价
在实验过程中,该同学观察到B装置中溶液颜色逐渐变浅,C装置中溶液颜色未见明显变化。再过一段时间后,E装置中氧化铜粉末由黑色转变为红色,气球F逐渐鼓起,此时C装置中溶液颜色仍未见明显变化。试回答下列问题。
①E装置中氧化铜由黑色变红的原因,可用化学反应方程式表示为:____________________。
②为探究铁钉与浓硫酸在不加热情况下是否发生了反应,请你帮该同学设计实验,填写下表内容:
试剂 | 操作方法 | 现象及结论 |
|
|
|

| ||
| ||
(12分)学习卤代烃性质时,我们知道溴乙烷在不同溶剂中与氢氧化钠发生不同类型的反应,生成不同的反应产物。我们可以通过实验的方法去验证反应的产物:
(1)在溴乙烷与氢氧化钠的乙醇溶液的 (反应类型)中可以观察到有气体生成。某同学用如下图所示装置对该气体进行验证,他所观察到的现象是 ;
(2)盛水试管的作用是 ;
(3)除了用酸性高锰酸钾溶液外,还可以用 试剂检验该气体,其反应原理是 (用化学方程式表示)。
(4)另一位同学取少量溴乙烷与氢氧化钠水溶液反应后的混合溶液,向其中滴加硝酸银溶液,加热,产生少量沉淀。该同学由此得出溴乙烷与氢氧化钠水溶液反应,生成了溴化钠。老师和同学都认为这样不合理。若请你用实验验证该反应中生成了溴化钠,你与该同学实验方案不同的实验方法是 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com